–£–ї—М—В—А–∞–Ј–≤–Ї—Г–Ї–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Є –≤–љ—Г—В—А–µ–љ–љ–Є—Е –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П—Е –Є —В—А–∞–≤–Љ–∞—Е
- Details
- Category: –£–ї—М—В—А–∞–Ј–≤—Г–Ї –≤ —Е–Є—А—Г—А–≥–Є–Є
–£–ї—М—В—А–∞–Ј–≤–Ї—Г–Ї–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Є –≤–љ—Г—В—А–µ–љ–љ–Є—Е –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П—Е –Є —В—А–∞–≤–Љ–∞—Е
1. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–∞–≤–Њ–≥–Њ –≤–µ—А—Е–љ–µ–≥–Њ –Ї–≤–∞–і—А–∞–љ—В–∞
–Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ—А–∞–≤–Њ–≥–Њ –≤–µ—А—Е–љ–µ–≥–Њ –Ї–≤–∞–і—А–∞–љ—В–∞ –≤–µ–і–µ—В—Б—П –њ–Њ–Є—Б–Ї –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –≥–µ–њ–∞—В–Њ—А–µ–љ–∞–ї—М–љ–Њ–Љ –Ї–∞—А–Љ–∞–љ–µ –Є –њ—А–∞–≤–Њ–є –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є.
–Я–Њ–Є—Б–Ї –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –Ї–∞—А–Љ–∞–љ–µ –Ь–Њ—А–Є—Б–Њ–љ–∞
–Я—А–Є –њ–Њ–Є—Б–Ї–µ —Б–≤–Њ–±–Њ–і–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В –љ–∞—З–Є–љ–∞—В—М —Б –Ї–∞—А–Љ–∞–љ–∞ –Ь–Њ—А–Є—Б–Њ–љ–∞, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –≥–µ–њ–∞—В–Њ—А–µ–љ–∞–ї—М–љ—Л–є –Ї–∞—А–Љ–∞–љ —П–≤–ї—П–µ—В—Б—П —Б–∞–Љ—Л–Љ —А–∞–љ–љ–Є–Љ –Є –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ –Љ–µ—Б—В–Њ–Љ —Б–Ї–Њ–њ–ї–µ–љ–Є—П –Ї—А–Њ–≤–Є –њ—А–Є —В—Г–њ–Њ–є –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є —В—А–∞–≤–Љ–µ.
–Т –Њ–і–љ–Њ–Љ –Ї—А—Г–њ–љ–Њ–Љ –Љ—Г–ї—М—В–Є—Ж–µ–љ—В—А–Њ–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є (10300 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —В—Г–њ–Њ–є –Є –њ–µ–љ–µ—В—А–Є—А—Г—О—Й–µ–є —В—А–∞–≤–Љ–Њ–є) –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ –≥–µ–њ–∞—В–Њ—А–µ–љ–∞–ї—М–љ—Л–є –Ї–∞—А–Љ–∞–љ –±—Л–ї –њ–Њ–ї–Њ–ґ–Є—В–µ–ї–µ–љ —З–∞—Й–µ, —З–µ–Љ —Б–њ–ї–µ–љ–Њ—А–µ–љ–∞–ї—М–љ—Л–є –Ї–∞—А–Љ–∞–љ –њ—А–Є –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є —Б–µ–ї–µ–Ј–µ–љ–Ї–Є. –Ґ–∞–Ї–ґ–µ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ –Ї–∞—А–Љ–∞–љ–∞ –Ь–Њ—А–Є—Б–Њ–љ–∞ —П–≤–ї—П–µ—В—Б—П –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –ї–µ–≥–Ї–Є–Љ –Є –±—Л—Б—В—А—Л–Љ.
–Я–∞—Ж–Є–µ–љ—В –љ–∞—Е–Њ–і–Є—В—Б—П –≤ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є –ї–µ–ґ–∞ –љ–∞ —Б–њ–Є–љ–µ. –Ф–∞—В—З–Є–Ї —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В—Б—П –њ–Њ —Б—А–µ–і–љ–µ-–њ–Њ–і–Љ—Л—И–µ—З–љ–Њ–є –ї–Є–љ–Є–Є –љ–∞ —Г—А–Њ–≤–љ–µ 11-12 —А–µ–±–µ—А, –њ—А–Є–Љ–µ–љ—П—П –Ї–Њ—А–Њ–љ–∞—А–љ—Л–є —Б–Ї–∞–љ, –Ј–∞—В–µ–Љ —Б –њ–Њ–Љ–Њ—Й—М—О –љ–∞–Ї–ї–Њ–љ–Њ–≤ (–Љ–µ–і–Є–∞–ї—М–љ–Њ –Є–ї–Є –ї–∞—В–µ—А–∞–ї—М–љ–Њ) –Є —Б–Ї–Њ–ї—М–ґ–µ–љ–Є–є –і–∞—В—З–Є–Ї–Њ–Љ (–Ї—А–∞–љ–Є–∞–ї—М–љ–Њ –Є–ї–Є –Ї–∞—Г–і–∞–ї—М–љ–Њ) –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ–Њ–ї—Г—З–Є—В—М –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–µ –Ї–∞—А–Љ–∞–љ–∞ –Ь–Њ—А–Є—Б–Њ–љ–∞ –і–ї—П –њ–Њ–Є—Б–Ї–∞ –Ї—А–Њ–≤–Є –≤ –љ–µ–Љ.
–Ъ—А–Њ–Љ–µ –Њ–±—Й–µ–њ—А–Є–љ—П—В–Њ–≥–Њ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ —Б–Ї–∞–љ–∞ –њ–Њ —Б—А–µ–і–љ–µ –њ–Њ–і–Љ—Л—И–µ—З–љ–Њ–є –ї–Є–љ–Є–Є –њ—А–Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є–Є FAST –≤ –њ—А–∞–≤–Њ–Љ –≤–µ—А—Е–љ–µ–Љ –Ї–≤–∞–і—А–∞–љ—В–µ, –Љ–љ–Њ–≥–Є–µ —Б —Г—Б–њ–µ—Е–Њ–Љ –њ—А–Є–Љ–µ–љ—П—О—В –њ—А–Њ–і–Њ–ї—М–љ—Л–є –Є–ї–Є –Ї–Њ—Б–Њ–є —Б–Ї–∞–љ –њ—А–∞–≤–Њ–≥–Њ –≤–µ—А—Е–љ–µ–≥–Њ –Ї–≤–∞–і—А–∞–љ—В–∞ –њ–Њ –њ–µ—А–µ–і–љ–µ-–њ–Њ–і–Љ—Л—И–µ—З–љ–Њ–є –ї–Є–љ–Є–Є –і–ї—П –њ–Њ–Є—Б–Ї–∞ –Ї—А–Њ–≤–Є –≤ –Ї–∞—А–Љ–∞–љ–µ –Ь–Њ—А–Є—Б–Њ–љ–∞.
–Х—Б–ї–Є —В–µ–љ—М –Њ—В —А–µ–±–µ—А –Љ–µ—И–∞–µ—В –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є, —В–Њ –і–∞—В—З–Є–Ї –љ—Г–ґ–љ–Њ —Б–ї–µ–≥–Ї–∞ –њ–Њ–≤–µ—А–љ—Г—В—М –њ—А–Њ—В–Є–≤ —З–∞—Б–Њ–≤–Њ–є —Б—В—А–µ–ї–Ї–Є, –і–ї—П —В–Њ–≥–Њ —З—В–Њ–±—Л –і–∞—В—З–Є–Ї –±—Л–ї –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –≤ –Љ–µ–ґ—А–µ–±–µ—А–љ–Њ–Љ –њ—А–Њ–Љ–µ–ґ—Г—В–Ї–µ.

–У–µ–њ–∞—В–Њ—А–µ–љ–∞–ї—М–љ—Л–є –Ї–∞—А–Љ–∞–љ (–Ї–∞—А–Љ–∞–љ –Ь–Њ—А–Є—Б–Њ–љ–∞) - —Н—В–Њ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–Њ –Љ–µ–ґ–і—Г –њ—А–∞–≤–∞—П –њ–Њ—З–Ї–∞ –њ—А–∞–≤–Њ–є –і–Њ–ї–µ–є –њ–µ—З–µ–љ–Є –Є –њ—А–∞–≤–Њ–є –њ–Њ—З–Ї–Њ–є. –Т –љ–Њ—А–Љ–µ –Њ–Ї—А—Г–ґ–∞—О—Й–Є–µ —В–Ї–∞–љ–Є —Н—В–Є—Е –Њ—А–≥–∞–љ–Њ–≤ —В–µ—Б–љ–Њ –њ—А–Є–ї–µ–≥–∞—О—В –і—А—Г–≥ –Ї –і—А—Г–≥—Г.
–Я—А–Є –њ–Њ—П–≤–ї–µ–љ–Є–Є –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –Ї–∞—А–Љ–∞–љ –Ь–Њ—А–Є—Б–Њ–љ–∞ —П–≤–ї—П–µ—В—Б—П –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ—Л–Љ –Љ–µ—Б—В–Њ–Љ –µ–µ —Б–Ї–Њ–њ–ї–µ–љ–Є—П. –Я—А–Є –Ј–∞–њ–Њ–ї–љ–µ–љ–Є–Є —Н—В–Њ–≥–Њ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–∞ –ґ–Є–і–Ї–Њ—Б—В—М—О –њ–µ—З–µ–љ—М –Є –њ–Њ—З–Ї–∞ –±—Г–і—Г—В —А–∞–Ј–і–µ–ї–µ–љ—Л –і—А—Г–≥ –Њ—В –і—А—Г–≥–∞. –І–µ–Љ –±–Њ–ї—М—И–µ –ґ–Є–і–Ї–Њ—Б—В–Є, —В–µ–Љ –±–Њ–ї—М—И–µ –±—Г–і–µ—В —Б–µ–њ–∞—А–∞—Ж–Є—П —Н—В–Є—Е –Њ—А–≥–∞–љ–Њ–≤.
–Ф–Њ–ї–ґ–љ–Њ –±—Л—В—М –њ–Њ–ї—Г—З–µ–љ–Њ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–µ –њ—А–∞–≤–Њ–є –і–Њ–ї–Є –њ–µ—З–µ–љ–Є –Є –њ—А–Є–ї–µ–≥–∞—О—Й–µ–є –Ї –љ–µ–є –њ—А–∞–≤–Њ–є –њ–Њ—З–Ї–Є. –Т–љ–Є–Љ–∞–љ–Є–µ –і–Њ–ї–ґ–љ–Њ –±—Л—В—М —Б–Ї–Њ–љ—Ж–µ–љ—В—А–Є—А–Њ–≤–∞–љ–Њ –љ–∞ –њ–Њ–Є—Б–Ї –ґ–Є–і–Ї–Њ—Б—В–Є –Љ–µ–ґ–і—Г —Н—В–Є–Љ–Є –і–≤—Г–Љ—П –Њ—А–≥–∞–љ–∞–Љ–Є –≤ –≤–Є–і–µ –∞–љ—Н—Е–Њ–≥–µ–љ–љ–Њ–≥–Њ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–∞.

–Ґ–Њ–ї—М–Ї–Њ –Ї–Њ–≥–і–∞ –њ–µ—З–µ–љ—М, –њ—А–∞–≤–∞—П –њ–Њ—З–Ї–∞ –Є –і–Є–∞—Д—А–∞–≥–Љ–∞ –±—Г–і—Г—В –≤–Љ–µ—Б—В–µ –Њ—В–Њ–±—А–∞–ґ–µ–љ—Л –љ–∞ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–Є –Є —З–µ—В–Ї–Њ –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А–Њ–≤–∞—В—М—Б—П, —В–Њ–ї—М–Ї–Њ —В–Њ–≥–і–∞ —Б–Ї–∞–љ –±—Г–і–µ—В —Б—З–Є—В–∞—В—М—Б—П –њ—А–Є–µ–Љ–ї–µ–Љ—Л–Љ.
–Т –љ–Њ—А–Љ–µ –љ–∞ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–Љ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–Є –њ—А–∞–≤–∞—П –њ–Њ—З–Ї–∞ –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –њ—А–Є–ї–µ–≥–∞–µ—В –Ї –њ–µ—З–µ–љ–Є, –±–µ–Ј –∞–љ—Н—Е–Њ–≥–µ–љ–љ–Њ–≥–Њ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–∞, —А–∞–Ј–і–µ–ї—П—О—Й–µ–≥–Њ —Н—В–Є –Њ—А–≥–∞–љ—Л.
–Я—А–Є –љ–∞–ї–Є—З–Є–Є —Б–≤–Њ–±–Њ–і–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –њ–µ—А–Є—В–Њ–љ–µ–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –Є –µ–µ —Б–Ї–Њ–њ–ї–µ–љ–Є–Є –≤ –Ї–∞—А–Љ–∞–љ–µ –Ь–Њ—А–Є—Б–Њ–љ–∞ –њ–µ—З–µ–љ—М –Є –њ—А–∞–≤–∞—П –њ–Њ—З–Ї–∞ –±—Г–і—Г—В —А–∞–Ј–і–µ–ї–µ–љ—Л –∞–љ—Н—Е–Њ–≥–µ–љ–љ—Л–Љ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–Њ–Љ (–Њ—В –љ–µ–±–Њ–ї—М—И–Њ–є –∞–љ—Н—Е–Њ–≥–µ–љ–љ–Њ–є –њ–Њ–ї–Њ—Б–Ї–Є –њ—А–Є –љ–µ–±–Њ–ї—М—И–Њ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ –ґ–Є–і–Ї–Њ—Б—В–Є, –і–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є —Б–µ–њ–∞—А–∞—Ж–Є–Є —Н—В–Є—Е –Њ—А–≥–∞–љ–Њ–≤ –±–Њ–ї—М—И–Є–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ –ґ–Є–і–Ї–Њ—Б—В–Є, –Ј–∞–њ–Њ–ї–љ—П—О—Й–µ–є –Ї–∞—А–Љ–∞–љ –Ь–Њ—А–Є—Б–Њ–љ–∞).

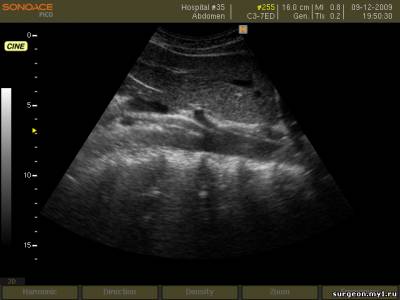
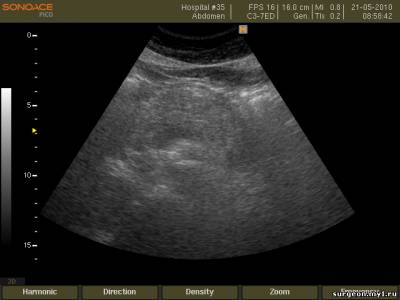
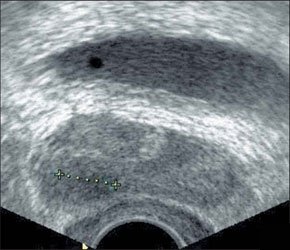
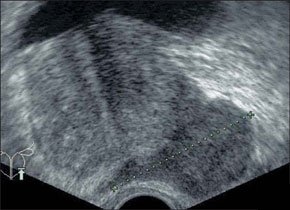
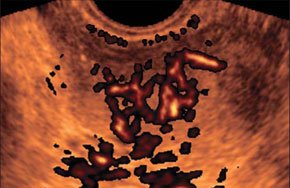
–Э–µ–±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –Ї–∞—А–Љ–∞–љ–µ –Ь–Њ—А–Є—Б–Њ–љ–∞.

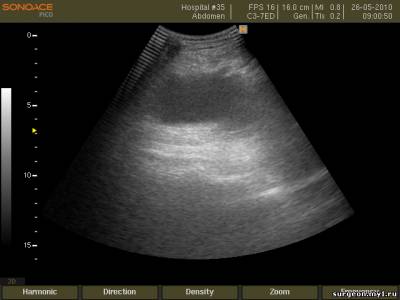
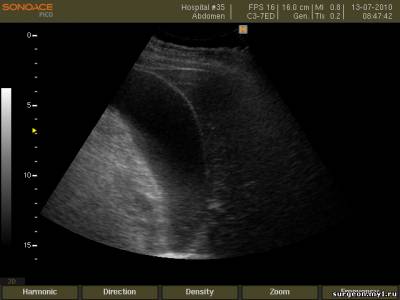
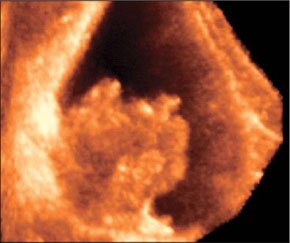
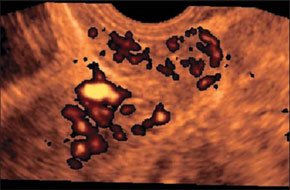
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≥–µ–њ–∞—В–Њ—А–µ–љ–∞–ї—М–љ–Њ–≥–Њ –Ї–∞—А–Љ–∞–љ–∞. –Ъ—А–Њ–≤—М –≤ –Ї–∞—А–Љ–∞–љ–µ –Ь–Њ—А–Є—Б–Њ–љ–∞.

–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≥–µ–њ–∞—В–Њ—А–µ–љ–∞–ї—М–љ–Њ–≥–Њ –Ї–∞—А–Љ–∞–љ–∞.
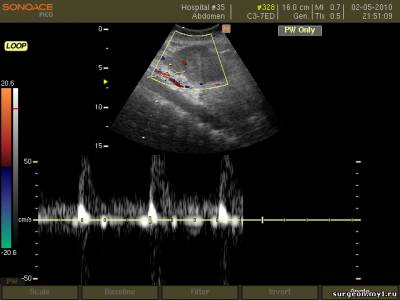
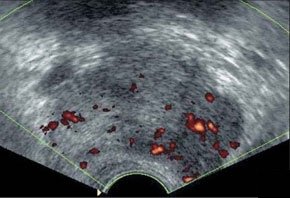
–Ъ—А–Њ–≤—М –≤ –Ї–∞—А–Љ–∞–љ–µ –Ь–Њ—А–Є—Б–Њ–љ–∞ (–њ–µ—З–µ–љ—М –Є –њ—А–∞–≤–∞—П –њ–Њ—З–Ї–∞ —А–∞–Ј–і–µ–ї–µ–љ—Л –∞–љ—Н—Е–Њ–≥–µ–љ–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В—М—О).

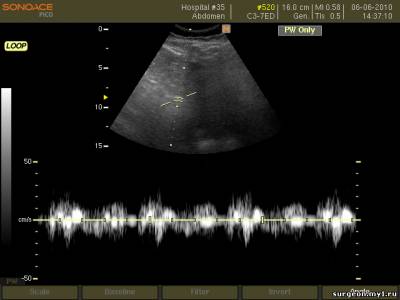
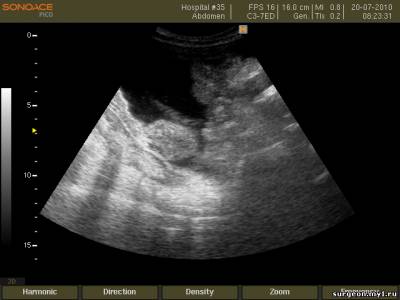
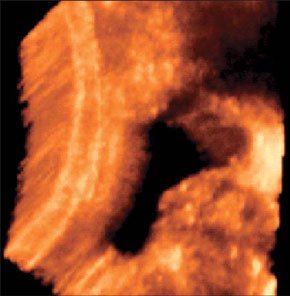
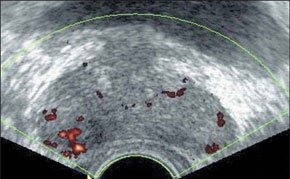
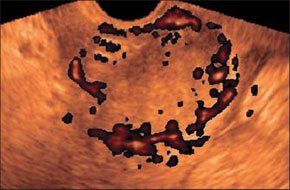
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≥–µ–њ–∞—В–Њ—А–µ–љ–∞–ї—М–љ–Њ–≥–Њ –Ї–∞—А–Љ–∞–љ–∞.
–С–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Ї—А–Њ–≤–Є –≤ –Ї–∞—А–Љ–∞–љ–µ –Ь–Њ—А–Є—Б–Њ–љ–∞ (–њ–µ—З–µ–љ—М –Є –њ—А–∞–≤–∞—П –њ–Њ—З–Ї–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —А–∞–Ј–і–µ–ї–µ–љ—Л –і—А—Г–≥ –Њ—В –і—А—Г–≥–∞ –∞–љ—Н—Е–Њ–≥–µ–љ–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В—М—О)
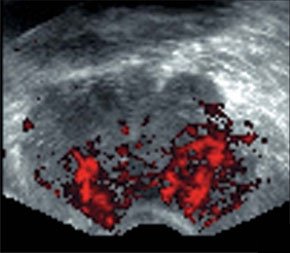
–Т –Ї—А–Є—В–Є—З–µ—Б–Ї–Є—Е —Б–Є—В—Г–∞—Ж–Є—П—Е, —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –љ–µ—Б—В–∞–±–Є–ї—М–љ–Њ—Б—В—М—О –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є–Ї–Є, –ґ–Є–і–Ї–Њ—Б—В—М, –Њ–±–љ–∞—А—Г–ґ–µ–љ–љ–∞—П –≤ –Ї–∞—А–Љ–∞–љ–µ –Ь–Њ—А–Є—Б–Њ–љ–∞ (–Ї–∞–Ї –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ –≥–µ–Љ–Њ–њ–µ—А–Є—В–Њ–љ–µ—Г–Љ–∞) —П–≤–ї—П–µ—В—Б—П –Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –і–ї—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П –љ–µ–Љ–µ–і–ї–µ–љ–љ–Њ–є –ї–∞–њ–∞—А–Њ—В–Њ–Љ–Є–Є.

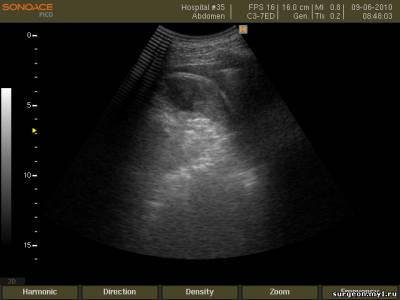
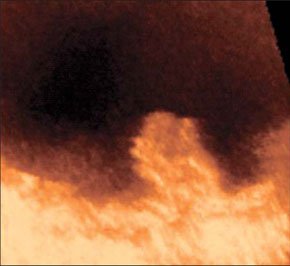
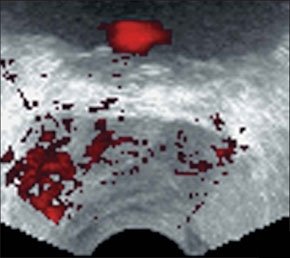
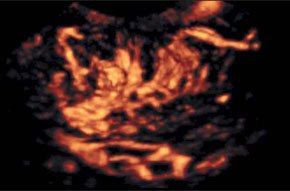
–Ь–∞—Б—Б–Є–≤–љ—Л–є –≥–µ–Љ–Њ–њ–µ—А–Є—В–Њ–љ–µ—Г–Љ.
–Ч–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –ґ–Є–і–Ї–Њ—Б—В–Є, –Њ–Ї—А—Г–ґ–∞—О—Й–µ–є –њ–µ—З–µ–љ—М –њ—А–Є —А–∞–Ј—А—Л–≤–µ —Б–µ–ї–µ–Ј–µ–љ–Ї–Є.
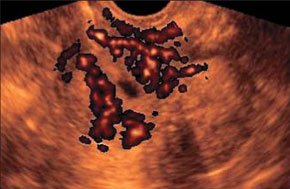
–Р–љ—Н—Е–Њ–≥–µ–љ–љ–∞—П —Б–≤–Њ–±–Њ–і–љ–∞—П –ґ–Є–і–Ї–Њ—Б—В—М —З–µ—В–Ї–Њ –Њ—З–µ—А—З–Є–≤–∞–µ—В –Ї–∞—А–Љ–∞–љ—Л –Є–љ—В—А–∞–њ–µ—А–Є—В–∞–љ–µ–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –Є –Ї–Њ–љ—В—Г—А—Л –Њ—А–≥–∞–љ–Њ–≤.
–С–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –Ї–∞—А–Љ–∞–љ–µ –Ь–Њ—А–Є—Б–Њ–љ–∞ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –ї–µ–≥–Ї–Њ –Є –±—Л—Б—В—А–Њ, –љ–µ –≤—Л–Ј—Л–≤–∞—П –Ј–∞—В—А—Г–і–љ–µ–љ–Є–є –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –≥–µ–Љ–Њ–њ–µ—А–Є—В–Њ–љ–µ—Г–Љ–∞. –°–ї–Њ–ґ–љ–Њ—Б—В–Є –Љ–Њ–≥—Г—В –≤–Њ–Ј–љ–Є–Ї–љ—Г—В—М –њ—А–Є –љ–µ–±–Њ–ї—М—И–Є—Е –Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л—Е –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞—Е –ґ–Є–і–Ї–Њ—Б—В–Є.

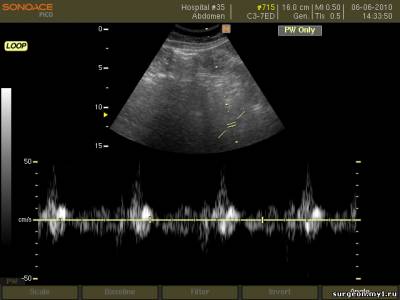
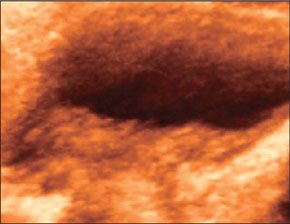
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≥–µ–њ–∞—В–Њ—А–µ–љ–∞–ї—М–љ–Њ–≥–Њ –Ї–∞—А–Љ–∞–љ–∞ –њ—А–Є –њ—А–Њ–і–Њ–ї—М–љ–Њ–Љ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–Є.
–Ь–Є–љ–Є–Љ–∞–ї—М–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Ї—А–Њ–≤–Є –≤ –Ї–∞—А–Љ–∞–љ–µ –Ь–Њ—А–Є—Б–Њ–љ–∞.
–І—В–Њ–±—Л –Є–Ј–±–µ–ґ–∞—В—М –Њ—И–Є–±–Њ–Ї –Ї–∞—А–Љ–∞–љ –Ь–Њ—А–Є—Б–Њ–љ–∞ –і–Њ–ї–ґ–µ–љ –±—Л—В—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ —В–∞–Ї–ґ–µ –Є –њ—А–Є –њ–Њ–њ–µ—А–µ—З–љ–Њ–Љ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–Є, —А–∞–Ј–≤–Њ—А–∞—З–Є–≤–∞—П –і–∞—В—З–Є–Ї –љ–∞ 90 –≥—А–∞–і—Г—Б–Њ–≤. –≠—В–Њ—В –њ—А–Є–µ–Љ –њ–Њ–≤—Л—И–∞–µ—В —В–Њ—З–љ–Њ—Б—В—М –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –њ—А–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–Є –љ–∞–ї–Є—З–Є—П –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –≥–µ–њ–∞—В–Њ—А–µ–љ–∞–ї—М–љ–Њ–Љ –Ї–∞—А–Љ–∞–љ–µ (–Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л—Е –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞—Е –ґ–Є–і–Ї–Њ—Б—В–Є).

–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≥–µ–њ–∞—В–Њ—А–µ–љ–∞–ї—М–љ–Њ–≥–Њ –Ї–∞—А–Љ–∞–љ–∞ –њ—А–Є –њ–Њ–њ–µ—А–µ—З–љ–Њ–Љ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–Є.
–Ь–Є–љ–Є–Љ–∞–ї—М–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Ї—А–Њ–≤–Є –≤ –Ї–∞—А–Љ–∞–љ–µ –Ь–Њ—А–Є—Б–Њ–љ–∞.

–Я–∞—Ж–Є–µ–љ—В —Б —А–∞–Ј—А—Л–≤–Њ–Љ —Б–µ–ї–µ–Ј–µ–љ–Ї–Є.
–Я—А–Є —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–Є –њ—А–∞–≤–Њ–≥–Њ –≤–µ—А—Е–љ–µ–≥–Њ –Ї–≤–∞–і—А–∞–љ—В–∞ –њ–Њ–ї—Г—З–µ–љ–Њ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–µ –≥–µ–њ–∞—В–Њ—А–µ–љ–∞–ї—М–љ–Њ–≥–Њ –Ї–∞—А–Љ–∞–љ–∞ —Б –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ —Б–≤–Њ–±–Њ–і–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є.
–Я—А–Є —В—Й–∞—В–µ–ї—М–љ–Њ–Љ –љ–∞–±–ї—О–і–µ–љ–Є–Є –Ј–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–Љ —Б–њ–ї–µ–љ—Н–Ї—В–Њ–Љ–Є—П –љ–µ –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–∞—Б—М.

–У–µ–Љ–Њ–њ–µ—А–Є—В–Њ–љ–µ—Г–Љ. –Я–Њ–њ–µ—А–µ—З–љ–Њ–µ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ.
–°–≤–Њ–±–Њ–і–љ–∞—П –ґ–Є–і–Ї–Њ—Б—В—М –≤ –њ–Њ–і–њ–µ—З–µ–љ–Њ—З–љ–Њ–Љ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ –Є –Ї–∞—А–Љ–∞–љ–µ –Ь–Њ—А–Є—Б–Њ–љ–∞.
–°—В–µ–љ–Ї–∞ –Ї–Є—И–µ—З–љ–Є–Ї–∞ –Є–ї–Є 12-–є –Ї–Є—И–Ї–Є, –њ—А–Є–ї–µ–≥–∞—О—Й–Є–µ –Ї –њ–µ—З–µ–љ–Є –≤ –≤–Є–і–µ —В–Њ–љ–Ї–Њ–є –∞–љ—Н—Е–Њ–≥–µ–љ–љ–Њ–Є –њ–Њ–ї–Њ—Б–Ї–Є (—В–∞–Ї–ґ–µ –љ–Є–ґ–љ—П—П –њ–Њ–ї–∞—П –≤–µ–љ–∞, –ґ–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М) –Љ–Њ–≥—Г—В –±—Л—В—М –Њ—И–Є–±–Њ—З–љ–Њ –њ—А–Є–љ—П—В—Л –Ј–∞ —Б–≤–Њ–±–Њ–і–љ—Г—О –ґ–Є–і–Ї–Њ—Б—В—М.
–І—В–Њ–±—Л –Є–Ј–±–µ–ґ–∞—В—М –Њ—И–Є–±–Њ–Ї, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є–Љ–µ–љ—П—В—М —А–∞–Ј–ї–Є—З–љ—Л–µ —Б–Ї–∞–љ—Л, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є–µ –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М —Н—В–Є —Б—В—А—Г–Ї—В—Г—А—Л. –Ю–±—Л—З–љ–Њ –њ–Њ–ї–µ–Ј–љ—Л –≤ —В–∞–Ї–Є—Е —Б–Є—В—Г–∞—Ж–Є—П—Е –≤–Ј–∞–Є–Љ–љ–Њ –њ–µ—А–њ–µ–љ–і–Є–Ї—Г–ї—П—А–љ—Л–µ —Б–Ї–∞–љ—Л —Н—В–Є—Е —Б—В—А—Г–Ї—В—Г—А.

–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≥–µ–њ–∞—В–Њ—А–µ–љ–∞–ї—М–љ–Њ–≥–Њ –Ї–∞—А–Љ–∞–љ–∞ –њ—А–Є –њ—А–Њ–і–Њ–ї—М–љ–Њ–Љ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–Є.
FF (free fluid) - —Б–≤–Њ–±–Њ–і–љ–∞—П –ґ–Є–і–Ї–Њ—Б—В—М –≤ –Ї–∞—А–Љ–∞–љ–µ –Ь–Њ—А–Є—Б–Њ–љ–∞.
–Х—Б–ї–Є –≤–Њ–Ј–љ–Є–Ї–∞—О—В —Б–Њ–Љ–љ–µ–љ–Є—П, —В–Њ –љ—Г–ґ–љ–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В—М —Н—В—Г –Ј–Њ–љ—Г –њ—А–Є –њ–Њ–њ–µ—А–µ—З–љ–Њ–Љ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–Є.

–Ь–Є–љ–Є–Љ–∞–ї—М–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Ї—А–Њ–≤–Є –≤ –Ї–∞—А–Љ–∞–љ–µ –Ь–Њ—А–Є—Б–Њ–љ–∞ –±—Л–ї–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Њ –њ—А–Є –њ–Њ–њ–µ—А–µ—З–љ–Њ–Љ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–Є.

–†–∞–Ј—А—Л–≤ –њ–µ—З–µ–љ–Є.
–≠—Е–Њ–≥–µ–љ–љ–∞—П –Є –≥–µ—В–µ—А–Њ–≥–µ–љ–љ–∞—П –≥–µ–Љ–∞—В–Њ–Љ–∞.
–Ь–Є–љ–Є–Љ–∞–ї—М–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Ї—А–Њ–≤–Є –≤ –Ї–∞—А–Љ–∞–љ–µ –Ь–Њ—А—А–Є—Б–Њ–љ–∞.
–Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤–µ—А—Е–љ–µ–≥–Њ –њ—А–∞–≤–Њ–≥–Њ –Ї–≤–∞–і—А–∞–љ—В–∞ –љ–∞ –љ–∞–ї–Є—З–Є–µ —Б–≤–Њ–±–Њ–і–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є, –Ї—А–Њ–Љ–µ –Ї–∞—А–Љ–∞–љ–∞ –Ь–Њ—А–Є—Б–Њ–љ–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В—М –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–Њ, –Њ–Ї—А—Г–ґ–∞—О—Й–µ–µ –њ–µ—З–µ–љ—М. –Ю—Б–Њ–±–µ–љ–љ–Њ –≤ —В–µ—Е —Б–ї—Г—З–∞—П—Е, –Ї–Њ–≥–і–∞ –≤ –Ї–∞—А–Љ–∞–љ–µ –Ь–Њ—А–Є—Б–Њ–љ–∞ –ґ–Є–і–Ї–Њ—Б—В—М –љ–µ –Њ–±–љ–∞—А—Г–ґ–µ–љ–∞.
–Ф–ї—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–∞, –Њ–Ї—А—Г–ґ–∞—О—Й–µ–≥–Њ –љ–Є–ґ–љ–Є–є –Ї—А–∞–є –њ–µ—З–µ–љ–Є (–њ–Њ–Є—Б–Ї –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –њ–Њ–і–њ–µ—З–µ–љ–Њ—З–љ–Њ–Љ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ) –љ—Г–ґ–љ–Њ —Б–Љ–µ—Б—В–Є—В—М –і–∞—В—З–Є–Ї –≤–љ–Є–Ј –Њ—В –њ–Њ–Ј–Є—Ж–Є–Є –Ї–∞—А–Љ–∞–љ–∞ –Ь–Њ—А–Є—Б–Њ–љ–∞, –њ—А–Є–Љ–µ–љ—П—П —Б–Ї–Њ–ї—М–Ј—П—Й–µ–µ –і–≤–Є–ґ–µ–љ–Є–µ. –Я—А–Є —Н—В–Њ–Љ –±—Г–і–µ—В –њ–Њ–ї—Г—З–µ–љ–Њ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–µ –љ–Є–ґ–љ–µ–≥–Њ –Ї—А–∞—П –њ–µ—З–µ–љ–Є.
–Ч–∞—В–µ–Љ –і–∞—В—З–Є–Ї –љ—Г–ґ–љ–Њ –љ–∞–Ї–ї–Њ–љ–Є—В—М –Є–ї–Є —Б–Љ–µ—Б—В–Є—В—М –Љ–µ–і–Є–∞–ї—М–љ–Њ (–њ–Њ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є—О –Ї –ї–µ–≤–Њ–є –і–Њ–ї–µ –њ–µ—З–µ–љ–Є). –Т—Б–µ —Н—В–Њ –≤—А–µ–Љ—П –≤–љ–Є–Љ–∞–љ–Є–µ –і–Њ–ї–ґ–љ–Њ –±—Л—В—М —Б–Ї–Њ–љ—Ж–µ–љ—В—А–Є—А–Њ–≤–∞–љ–Њ –љ–∞ –њ–Њ–Є—Б–Ї –ґ–Є–і–Ї–Њ—Б—В–Є, –Њ–Ї—А—Г–ґ–∞—О—Й–µ–є –Ї—А–∞—П –њ–µ—З–µ–љ–Є.

–°–Ї–Њ–њ–ї–µ–љ–Є–µ —Б–≤–Њ–±–Њ–і–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є —Г –љ–Є–ґ–љ–µ–≥–Њ –Ї—А–∞—П –њ—А–∞–≤–Њ–є –і–Њ–ї–Є –њ–µ—З–µ–љ–Є.
RLL - –њ—А–∞–≤–∞—П –і–Њ–ї—П –њ–µ—З–µ–љ–Є RK - –њ—А–∞–≤–∞—П –њ–Њ—З–Ї–∞

–У–µ–Љ–Њ–њ–µ—А–Є—В–Њ–љ–µ—Г–Љ. –Ъ—А–Њ–≤—М —Г –љ–Є–ґ–љ–µ–≥–Њ –Ї—А–∞—П –њ–µ—З–µ–љ–Є.
–Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Ї–∞—А–Љ–∞–љ–∞ –Ь–Њ—А–Є—Б–Њ–љ–∞ —Б–≤–Њ–±–Њ–і–љ–∞—П –ґ–Є–і–Ї–Њ—Б—В—М –љ–µ –±—Л–ї–∞ –Њ–±–љ–∞—А—Г–ґ–µ–љ–∞, –љ–Њ –њ—А–Є —Б–Љ–µ—Й–µ–љ–Є–Є –і–∞—В—З–Є–Ї–∞ –љ–µ–Љ–љ–Њ–≥–Њ –Ї–∞—Г–і–∞–ї—М–љ–Њ –Є –Љ–µ–і–Є–∞–ї—М–љ–Њ –±—Л–ї–∞ –Њ–±–љ–∞—А—Г–ґ–µ–љ–∞ –ґ–Є–і–Ї–Њ—Б—В—М, –Њ–Ї—А—Г–ґ–∞—О—Й–∞—П –љ–Є–ґ–љ–Є–є –Ї—А–∞–є –њ–µ—З–µ–љ–Є.

–У–µ–Љ–Њ–њ–µ—А–Є—В–Њ–љ–µ—Г–Љ. –Ц–Є–і–Ї–Њ—Б—В—М —Г –љ–Є–ґ–љ–µ–≥–Њ –Ї—А–∞—П –њ–µ—З–µ–љ–Є.
–Ґ–∞–Ї–Є–Љ –ґ–µ –Њ–±—А–∞–Ј–Њ–Љ –Њ—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П –Є –≤–µ—А—Е–љ–Є–є –Ї—А–∞–є –њ–µ—З–µ–љ–Є, —Б —Ж–µ–ї—М—О –њ–Њ–Є—Б–Ї–∞ –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –њ—А–∞–≤–Њ–Љ —Б—Г–±–і–Є–∞—Д—А–∞–≥–Љ–∞–ї—М–љ–Њ–Љ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ (–Љ–µ–ґ–і—Г –њ–µ—З–µ–љ—М—О –Є –і–Є–∞—Д—А–∞–≥–Љ–Њ–є). –Я—А–Є —Н—В–Њ–Љ –і–∞—В—З–Є–Ї —Б–Љ–µ—Й–∞–µ—В—Б—П –љ–µ–Љ–љ–Њ–≥–Њ –≤–≤–µ—А—Е –Њ—В –њ–Њ–Ј–Є—Ж–Є–Є –Ї–∞—А–Љ–∞–љ–∞ –Ь–Њ—А–Є—Б–Њ–љ–∞, –∞ –Ј–∞—В–µ–Љ –љ–∞–Ї–ї–Њ–љ—П–µ—В—Б—П –Є–ї–Є —Б–Љ–µ—Й–∞–µ—В—Б—П –Љ–µ–і–Є–∞–ї—М–љ–Њ (–њ–Њ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є—О –Ї –ї–µ–≤–Њ–є –і–Њ–ї–µ –њ–µ—З–µ–љ–Є).

–У–µ–Љ–Њ–њ–µ—А–Є—В–Њ–љ–µ—Г–Љ.
–С–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Ї—А–Њ–≤–Є –љ–∞–і –њ–µ—З–µ–љ—М—О, –≤ –њ–Њ–і–і–Є–∞—Д—А–∞–≥–Љ–∞–ї—М–љ–Њ–Љ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ.
–Р–љ—Н—Е–Њ–≥–µ–љ–љ–Њ–µ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–Њ –Љ–µ–ґ–і—Г –≤–µ—А—Е–љ–Є–Љ –Ї—А–∞–µ–Љ –њ–µ—З–µ–љ–Є –Є –≥–Є–њ–µ—А—Н—Е–Њ–≥–µ–љ–љ–Њ–є –і–Є–∞—Д—А–∞–≥–Љ–Њ–є.

–Ь–∞—Б—Б–Є–≤–љ—Л–є –≥–µ–Љ–Њ–њ–µ—А–Є—В–Њ–љ–µ—Г–Љ.
–Ч–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –ґ–Є–і–Ї–Њ—Б—В–Є, –Њ–Ї—А—Г–ґ–∞—О—Й–µ–є –њ–µ—З–µ–љ—М –Є –ґ–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М.
–Ц–Є–і–Ї–Њ—Б—В—М –≤ –Ї–Њ–љ—В–µ–Ї—Б—В–µ —В—А–∞–≤–Љ—Л –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –Ї—А–Њ–≤—М—О, –љ–Њ —В–∞–Ї–ґ–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –Љ–Њ—З–Њ–є, –ґ–µ–ї—З—М—О –Є–ї–Є –Ї–Є—И–µ—З–љ—Л–Љ —Б–Њ–і–µ—А–ґ–Є–Љ—Л–Љ –њ—А–Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П—Е –њ–Њ–ї—Л—Е –Њ—А–≥–∞–љ–Њ–≤. –Я—А–Є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –∞—Б—Ж–Є—В–∞—Е (—Ж–Є—А—А–Њ–Ј –њ–µ—З–µ–љ–Є, —Б–µ—А–і–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М) —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —В—А–∞–≤–Љ–Њ–є FAST –њ—А–Њ—В–Њ–Ї–Њ–ї –љ–µ –Љ–Њ–ґ–µ—В –Є—Б–Ї–ї—О—З–Є—В—М –≥–µ–Љ–Њ–њ–µ—А–Є—В–Њ–љ–µ—Г–Љ –Є —Г –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є –љ–µ—Б—В–∞–±–Є–ї—М–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—З–Є—В–∞–µ—В—Б—П –њ–Њ–Ј–Є—В–Є–≤–љ—Л–Љ, —Б—В–∞–±–Є–ї—М–љ—Л–µ –њ–∞—Ж–Є–µ–љ—В—Л —Б –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–Љ –∞—Б—Ж–Є—В–Њ–Љ –њ–Њ–і–≤–µ—А–≥–∞—О—В—Б—П –і—А—Г–≥–Є–Љ –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–Љ —В–µ—Б—В–∞–Љ.
–Я–Њ–Є—Б–Ї –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –њ—А–∞–≤–Њ–є –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є
–Я–Њ—Б–ї–µ —В–Њ–≥–Њ, –Ї–∞–Ї –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ –≥–µ–њ–∞—В–Њ—А–µ–љ–∞–ї—М–љ—Л–є –Ї–∞—А–Љ–∞–љ –љ–∞ –љ–∞–ї–Є—З–Є–µ –њ–µ—А–Є—В–Њ–љ–µ–∞–ї—М–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є, –њ—А–Є—Б—В—Г–њ–∞—О—В –Ї –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—О –њ—А–∞–≤–Њ–є –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є, —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ–є –љ–∞–і –і–Є–∞—Д—А–∞–≥–Љ–Њ–є. –Я—А–Є —Н—В–Њ–Љ –і–∞—В—З–Є–Ї –Є–Ј –њ–Њ–Ј–Є—Ж–Є–Є –Ї–∞—А–Љ–∞–љ–∞ –Ь–Њ—А–Є—Б–Њ–љ–∞ —Б–Ї–Њ–ї—М–Ј—П—Й–Є–Љ –і–≤–Є–ґ–µ–љ–Є–µ–Љ —Б–Љ–µ—Й–∞–µ—В—Б—П –љ–µ–Љ–љ–Њ–≥–Њ –≤–≤–µ—А—Е.
–Ф–ї—П –њ–Њ–Є—Б–Ї–∞ –њ—А–∞–≤–Њ—Б—В–Њ—А–Њ–љ–љ–µ–≥–Њ –≥–µ–Љ–Њ—В–Њ—А–∞–Ї—Б–∞ –і–∞—В—З–Є–Ї —Б–Љ–µ—Й–∞–µ—В—Б—П (—Б–Ї–Њ–ї—М–Ј—П—Й–Є–Љ –і–≤–Є–ґ–µ–љ–Є–µ–Љ) –љ–µ–Љ–љ–Њ–≥–Њ –≤–≤–µ—А—Е –Њ—В –њ–Њ–Ј–Є—Ж–Є–Є –Ї–∞—А–Љ–∞–љ–∞ –Ь–Њ—А–Є—Б–Њ–љ–∞.
–Э–∞ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–Љ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–Є –і–Є–∞—Д—А–∞–≥–Љ–∞ –Є–Љ–µ–µ—В –≤–Є–і –≥–Є–њ–µ—А—Н—Е–Њ–≥–µ–љ–љ–Њ–є –і—Г–≥–Є. –Э–∞–і –і–Є–∞—Д—А–∞–≥–Љ–Њ–є —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–∞ –њ–ї–µ–≤—А–∞–ї—М–љ–∞—П –њ–Њ–ї–Њ—Б—В—М –Є –ї–µ–≥–Ї–Њ–µ, –љ–Њ –≤ –љ–Њ—А–Љ–µ –њ—А–Є —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–Љ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–Є –љ–∞–і –і–Є–∞—Д—А–∞–≥–Љ–Њ–є –Њ—В–Њ–±—А–∞–ґ–µ–љ–Њ –Ј–µ—А–Ї–∞–ї—М–љ–Њ–µ –Њ—В—А–∞–ґ–µ–љ–Є–µ –њ–µ—З–µ–љ–Є (–Є–Ј-–Ј–∞ –Ј–µ—А–Ї–∞–ї—М–љ–Њ–≥–Њ –∞—А—В–µ—Д–∞–Ї—В–∞).
–Я—А–Є –љ–∞–ї–Є—З–Є–Є –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –∞—А—В–µ—Д–∞–Ї—В –Ј–µ—А–Ї–∞–ї—М–љ–Њ–≥–Њ –Њ—В—А–∞–ґ–µ–љ–Є—П –Є—Б—З–µ–Ј–∞–µ—В –Є –љ–∞–і –і–Є–∞—Д—А–∞–≥–Љ–Њ–є –±—Г–і–µ—В –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А–Њ–≤–∞—В—М—Б—П –∞–љ—Н—Е–Њ–≥–µ–љ–љ–Њ–µ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–Њ. –Ґ–∞–Ї–ґ–µ –≤ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є –Љ–Њ–ґ–µ—В –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А–Њ–≤–∞—В—М—Б—П –∞—В–µ–ї–µ–Ї—В–∞—В–Є—З–µ—Б–Ї–Њ–µ –ї–µ–≥–Ї–Њ–µ.

–Ф–Є–∞—Д—А–∞–≥–Љ–∞ –Є–Љ–µ–µ—В –≤–Є–і –≥–Є–њ–µ—А—Н—Е–Њ–≥–µ–љ–љ–Њ–є –і—Г–≥–Є –Є —П–≤–ї—П–µ—В—Б—П –Њ—А–Є–µ–љ—В–Є—А–Њ–Љ, —А–∞–Ј–і–µ–ї—П—О—Й–Є–Љ –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Г—О –њ–Њ–ї–Њ—Б—В—М –Њ—В –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є. –Я–Њ–і –і–Є–∞—Д—А–∞–≥–Љ–Њ–є (–Ї–∞—Г–і–∞–ї—М–љ–Њ) —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–∞ –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–∞—П –њ–Њ–ї–Њ—Б—В—М.
–Э–∞–і –і–Є–∞—Д—А–∞–≥–Љ–Њ–є (–Ї—А–∞–љ–Є–∞–ї—М–љ–Њ) —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–∞ –њ–ї–µ–≤—А–∞–ї—М–љ–∞—П –њ–Њ–ї–Њ—Б—В—М, –Ї–Њ—В–Њ—А–∞—П –љ–∞ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–Љ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–Є –≤ –љ–Њ—А–Љ–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –Ј–µ—А–Ї–∞–ї—М–љ—Л–Љ –Њ—В—А–∞–ґ–µ–љ–Є–µ–Љ –њ–µ—З–µ–љ–Є (–Є–Ј-–Ј–∞ –Ј–µ—А–Ї–∞–ї—М–љ–Њ–≥–Њ –∞—А—В–µ—Д–∞–Ї—В–∞).

–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–∞–≤–Њ–є –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є.
–У–µ–Љ–Њ—В–Њ—А–∞–Ї—Б–∞ –љ–µ—В (–Њ—В—Б—Г—В—Б—В–≤—Г–µ—В –∞–љ—Н—Е–Њ–≥–µ–љ–љ–Њ–µ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–Њ –љ–∞–і –і–Є–∞—Д—А–∞–≥–Љ–Њ–є).
–Я—А–Є—Б—Г—В—Б—В–≤—Г–µ—В –Ј–µ—А–Ї–∞–ї—М–љ—Л–є –∞—А—В–µ—Д–∞–Ї—В –љ–∞–і –і–Є–∞—Д—А–∞–≥–Љ–Њ–є
–Ъ—А–Њ–≤—М –≤ –Ї–∞—А–Љ–∞–љ–µ –Ь–Њ—А–Є—Б–Њ–љ–∞ (—Б–Є–љ—П—П —Б—В—А–µ–ї–Ї–∞)

–Ю—В—Б—Г—В—Б—В–≤–Є–µ –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –њ—А–∞–≤–Њ–є –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є (–Ј–µ—А–Ї–∞–ї—М–љ–Њ–µ –Њ—В—А–∞–ґ–µ–љ–Є–µ –њ–µ—З–µ–љ–Є –љ–∞–і –і–Є–∞—Д—А–∞–≥–Љ–Њ–є).
–У–Є–њ–µ—А—Н—Е–Њ–≥–µ–љ–љ–∞—П –і–Є–∞—Д—А–∞–≥–Љ–∞ –Њ–±–Њ–Ј–љ–∞—З–µ–љ–∞ —Б—В—А–µ–ї–Ї–Њ–є.

–Я—А–∞–≤–Њ—Б—В–Њ—А–Њ–љ–љ–Є–є –≥–µ–Љ–Њ—В–Њ—А–∞–Ї—Б - –∞–љ—Н—Е–Њ–≥–µ–љ–љ–∞—П –ґ–Є–і–Ї–Њ—Б—В—М –љ–∞–і –і–Є–∞—Д—А–∞–≥–Љ–Њ–є.
L - liver (–њ–µ—З–µ–љ—М)
–†–Х - pleural effusion (–ґ–Є–і–Ї–Њ—Б—В—М –≤ –њ—А–∞–≤–Њ–є
–њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є)
–°—В—А–µ–ї–Ї–Њ–є –Њ–±–Њ–Ј–љ–∞—З–µ–љ—Л –љ–Є—В–Є —Д–Є–±—А–Є–љ–∞.

–Э–∞–ї–Є—З–Є–µ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є –Љ–Њ–ґ–µ—В –±—Л—В—М –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Њ –њ—А–Є –њ–Њ–њ–µ—А–µ—З–љ–Њ–Љ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–Є.
–Я–Њ–њ–µ—А–µ—З–љ–Њ–µ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ —З–µ—А–µ–Ј –њ–µ—З–µ–љ—М (L).
–Я–ї–µ–≤—А–∞–ї—М–љ–∞—П –ґ–Є–і–Ї–Њ—Б—В—М (—Б–µ—А–∞—П —Б—В—А–µ–ї–Ї–∞), —В–∞–Ї–ґ–µ –њ—А–Є—Б—Г—В—Б—В–≤—Г–µ—В —Б–≤–Њ–±–Њ–і–љ–∞—П –ґ–Є–і–Ї–Њ—Б—В—М –≤ –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є (—Б–Є–љ—П—П —Б—В—А–µ–ї–Ї–∞), –і–Є–∞—Д—А–∞–≥–Љ–∞ –≤ –≤–Є–і–µ —В–Њ–љ–Ї–Њ–є –≥–Є–њ–µ—А—Н—Е–Њ–≥–µ–љ–љ–Њ–є –і—Г–≥–Є (—З–µ—А–љ–∞—П —Б—В—А–µ–ї–Ї–∞), —Б—В–µ–љ–Ї–∞ –≥—А—Г–і–љ–Њ–є –Ї–ї–µ—В–Ї–Є –≤ –≤–Є–і–µ —В–Њ–ї—Б—В–Њ–є –≥–Є–њ–µ—А—Н—Е–Њ–≥–µ–љ–љ–Њ–є –і—Г–≥–Є (–ґ–µ–ї—В–∞—П —Б—В—А–µ–ї–Ї–∞).

–Я—А–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –≥–µ–Љ–Њ–њ–µ—А–Є—В–Њ–љ–µ—Г–Љ–∞ —Б —Б—Г–±–і–Є–∞—Д—А–∞–≥–Љ–∞–ї—М–љ—Л–Љ —Б–Ї–Њ–њ–ї–µ–љ–Є–µ–Љ –ґ–Є–і–Ї–Њ—Б—В–Є –Є –≥–µ–Љ–Њ—В–Њ—А–∞–Ї—Б–∞ –ґ–Є–і–Ї–Њ—Б—В—М, –Њ–Ї—А—Г–ґ–∞—О—Й–∞—П –њ–µ—З–µ–љ—М –±—Г–і–µ—В –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А–Њ–≤–∞—В—М—Б—П –≤ –≤–Є–і–µ –∞–љ—Н—Е–Њ–≥–µ–љ–љ–Њ–≥–Њ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–∞ –њ–Њ–і –і–Є–∞—Д—А–∞–≥–Љ–Њ–є, –∞ –≥–µ–Љ–Њ—В–Њ—А–∞–Ї—Б –≤ –≤–Є–і–µ –∞–љ—Н—Е–Њ–≥–µ–љ–љ–Њ–≥–Њ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–∞ –љ–∞–і –і–Є–∞—Д—А–∞–≥–Љ–Њ–є. –Ф–Є–∞—Д—А–∞–≥–Љ–∞ –±—Г–і–µ—В –Є–Љ–µ—В—М –≤–Є–і –≥–Є–њ–µ—А—Н—Е–Њ–≥–µ–љ–љ–Њ–є –і—Г–≥–Є, —А–∞–Ј–і–µ–ї—П—О—Й–µ–є —Н—В–Є –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–∞. –Ґ–∞–Ї–Њ–є –ґ–µ –≤–Є–і –±—Г–і–µ—В –Є–Љ–µ—В—М –ї–µ–≤–Њ—Б—В–Њ—А–Њ–љ–љ–Є–є –≥–µ–Љ–Њ—В–Њ—А–∞–Ї—Б —Б –≥–µ–Љ–Њ–њ–µ—А–Є—В–Њ–љ–µ—Г–Љ–Њ–Љ –≤ –ї–µ–≤–Њ–Љ —Б—Г–±–і–Є–∞—Д—А–∞–≥–Љ–∞–ї—М–љ–Њ–Љ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ.

–Я—А–∞–≤–Њ—Б—В–Њ—А–Њ–љ–љ–Є–є –≥–µ–Љ–Њ—В–Њ—А–∞–Ї—Б -–∞–љ—Н—Е–Њ–≥–µ–љ–љ–Њ–µ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–Њ –љ–∞–і –і–Є–∞—Д—А–∞–≥–Љ–Њ–є (–ґ–µ–ї—В–∞—П —Б—В—А–µ–ї–Ї–∞).
–Т –∞–љ—Н—Е–Њ–≥–µ–љ–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А—Г–µ—В—Б—П —З–∞—Б—В–Є—З–љ–Њ –Ї–Њ–ї–ї–∞–±–Є—А–Њ–≤–∞–љ–љ–Њ–µ –ї–µ–≥–Ї–Њ–µ —Б –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л–Љ–Є –≤–µ—А—В–Є–Ї–∞–ї—М–љ—Л–Љ–Є –∞—А—В–µ—Д–∞–Ї—В–∞–Љ–Є (—Б–Є–љ—П—П —Б—В—А–µ–ї–Ї–∞).

–Ь–∞—Б—Б–Є–≤–љ—Л–є –њ—А–∞–≤–Њ—Б—В–Њ—А–Њ–љ–љ–Є–є –≥–µ–Љ–Њ—В–Њ—А–∞–Ї—Б - –±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –∞–љ—Н—Е–Њ–≥–µ–љ–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є –љ–∞–і –і–Є–∞—Д—А–∞–≥–Љ–Њ–є.
–Ъ–Њ–Љ–њ—А–µ—Б—Б–Є—П –ї–µ–≥–Ї–Њ–≥–Њ (—Б—В—А–µ–ї–Ї–∞).
–Р—В–µ–ї–µ–Ї—В–∞—В–Є—З–µ—Б–Ї–Њ–µ –ї–µ–≥–Ї–Њ–µ –і–≤–Є–ґ–µ—В—Б—П –њ—А–Є –і—Л—Е–∞–љ–Є–Є –≤–љ—Г—В—А–Є –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–Љ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ.

–Я—А–∞–≤–Њ—Б—В–Њ—А–Њ–љ–љ–Є–є –≥–µ–Љ–Њ—В–Њ—А–∞–Ї—Б - —Б–Ї–Њ–њ–ї–µ–љ–Є–µ –ґ–Є–і–Ї–Њ—Б—В–Є –Љ–µ–ґ–і—Г –њ–µ—А–µ–і–љ–µ–є –≥—А—Г–і–љ–Њ–є —Б—В–µ–љ–Ї–Њ–є –Є –і–Є–∞—Д—А–∞–≥–Љ–Њ–є (–Х).
(–Э) - –њ–Њ–і–Ї–Њ–ґ–љ–∞—П –≥–µ–Љ–∞—В–Њ–Љ–∞ (–њ–Њ–і–Ї–Њ–ґ–љ–Њ–µ —Б–Ї–Њ–њ–ї–µ–љ–Є–µ –∞–љ—Н—Е–Њ–≥–µ–љ–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є).
–Ь–Є–љ–Є–Љ–∞–ї—М–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є, –Ї–Њ—В–Њ—А–Њ–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –≤—Л—П–≤–ї–µ–љ–Њ –њ—А–Є —А–∞–і–Є–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–∞ –≤ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є —Б—В–Њ—П вАФ 150 –Љ–ї. –£–ї—М—В—А–∞—Б–Њ–љ–Њ–≥—А–∞—Д–Є—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є—В —А–∞–і–Є–Њ–≥—А–∞—Д–Є—О –њ—А–Є –≤—Л—П–≤–ї–µ–љ–Є–Є –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є, –Є–Љ–µ—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М 100% –Є —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В—М 99.7%, –Є –Љ–Њ–ґ–µ—В –≤—Л—П–≤–ї—П—В—М –љ–∞–Є–Љ–µ–љ—М—И–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є, –љ–∞—З–Є–љ–∞—П —Б 5 –Љ–ї.
–†–∞–і–Є–Њ–≥—А–∞—Д–Є—П –Є–Љ–µ–µ—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М 71% –Є —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В—М 98.5%, –љ–Њ –≤ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є –ї–µ–ґ–∞ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –µ—Й–µ –±–Њ–ї–µ–µ —Б–љ–Є–ґ–∞–µ—В—Б—П (43%) –Є –і–∞–ґ–µ –±–Њ–ї—М—И–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –ґ–Є–і–Ї–Њ—Б—В–Є –Љ–Њ–≥—Г—В –±—Л—В—М –љ–µ –Њ–±–љ–∞—А—Г–ґ–µ–љ—Л.
–Ъ—А–Њ–Љ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –≥–µ–Љ–Њ—В–Њ—А–∞–Ї—Б–∞ —Б–Њ–љ–Њ–≥—А–∞—Д–Є—П —В–∞–Ї–ґ–µ —Б–њ–Њ—Б–Њ–±–љ–∞ –Њ—Ж–µ–љ–Є—В—М –µ–≥–Њ —А–∞–Ј–Љ–µ—А. –С—Л—Б—В—А—Л–Љ –Є –њ—А–Њ—Б—В—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –≤—Л—З–Є—Б–ї–µ–љ–Є—П –Њ–±—К–µ–Љ–∞ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є —П–≤–ї—П–µ—В—Б—П —Б–ї–µ–і—Г—О—Й–Є–є:
—Б—Г–Љ–Љ–∞ —А–∞—Б—Б—В–Њ—П–љ–Є–є (—А–∞—Б—Б—В–Њ—П–љ–Є–µ –Њ—В –ї–µ–≥–Ї–Њ–≥–Њ –і–Њ –і–Є–∞—Д—А–∞–≥–Љ—Л –ї–∞—В–µ—А–∞–ї—М–љ–∞—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –≤—Л—Б–Њ—В–∞), —Г–Љ–љ–Њ–ґ–µ–љ–љ–∞—П –љ–∞ 70.

–Ю–±—К–µ–Љ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є —А–∞–≤–µ–љ 700 –Љ–ї –њ—А–Є –≤—Л—З–Є—Б–ї–µ–љ–Є–Є —Б—Г–Љ–Љ—Л —А–∞—Б—Б—В–Њ—П–љ–Є–є (—А–∞—Б—Б—В–Њ—П–љ–Є–µ –Њ—В –ї–µ–≥–Ї–Њ–≥–Њ –і–Њ –і–Є–∞—Д—А–∞–≥–Љ—Л + –ї–∞—В–µ—А–∞–ї—М–љ–∞—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –≤—Л—Б–Њ—В–∞), —Г–Љ–љ–Њ–ґ–µ–љ–љ–Њ–є –љ–∞ 70. (—Д–∞–Ї—В–Є—З–µ—Б–Ї–Є–є –Њ–±—К–µ–Љ —А–∞–≤–µ–љ 800 –Љ–ї)
–Я—А–Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є–Є FAST –њ—А–Њ—В–Њ–Ї–Њ–ї–∞ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є —З–∞—Б—В–Њ –Њ—Ж–µ–љ–Є–≤–∞–µ—В—Б—П –≤–Є–Ј—Г–∞–ї—М–љ–Њ (–Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л–є, —Г–Љ–µ—А–µ–љ–љ—Л–є, –Љ–∞—Б—Б–Є–≤–љ—Л–є –≥–µ–Љ–Њ—В–Њ—А–∞–Ї—Б).
Dr.Yuliya, Ukraine, Sonologist, Regional General Hospital, Libya 2009 http://sonomir.wordpress.com
–£–Ј–Є –њ–µ—З–µ–љ–Є, –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Є –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л.
- Details
- Category: –£–ї—М—В—А–∞–Ј–≤—Г–Ї –≤ —Е–Є—А—Г—А–≥–Є–Є
  
–Ь–µ—В–Њ–і–Є–Ї–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–°–Њ–≤—А–µ–Љ–µ–љ–љ–∞—П —В–µ—Е–љ–Є–Ї–∞ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (–£–Ч–Ш) –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б –≤—Л—Б–Њ–Ї–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–є —В–Њ—З–љ–Њ—Б—В—М—О –Њ—Ж–µ–љ–Є—В—М —Д–Њ—А–Љ—Г, —А–∞–Ј–Љ–µ—А—Л –Є —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ –Њ—А–≥–∞–љ–Њ–≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є (–њ–µ—З–µ–љ–Є, –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П, –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л, —Б–µ–ї–µ–Ј–µ–љ–Ї–Є –Є –і—А.), –≤—Л—П–≤–Є—В—М –Њ—З–∞–≥–Њ–≤—Л–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –≤ –љ–Є—Е (—А–∞–Ї –њ–µ—З–µ–љ–Є, –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л, –Љ–µ—В–∞—Б—В–∞–Ј—Л –Њ–њ—Г—Е–Њ–ї–µ–є, –∞–±—Б—Ж–µ—Б—Б—Л, –Ї–Є—Б—В—Л, –≥–µ–Љ–∞—В–Њ–Љ—Л, –∞–і–µ–љ–Њ–Љ—Л –Є —В. –і.), –Њ—Ж–µ–љ–Є—В—М –њ–ї–Њ—В–љ–Њ—Б—В—М –Є —Б—В—А—Г–Ї—В—Г—А—Г –њ–∞—А–µ–љ—Е–Є–Љ—Л –њ–µ—З–µ–љ–Є –Є –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –њ—А–Є –Є—Е –і–Є—Д—Д—Г–Ј–љ–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є, –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞—В—М –і–∞–ґ–µ –Љ–∞–ї—Л–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ (100вАУ200 –Љ–ї) —Б–≤–Њ–±–Њ–і–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є, –≤—Л—П–≤–Є—В—М –Ї–Њ–љ–Ї—А–µ–Љ–µ–љ—В—Л –≤ –ґ–µ–ї—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В—П—Е, –Њ—Ж–µ–љ–Є—В—М –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Ї—А—Г–њ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤, –ґ–µ–ї—З–љ—Л—Е –њ—А–Њ—В–Њ–Ї–Њ–≤ –Є —В. –њ.
–Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —И–Є—А–Њ–Ї–Њ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –≤ –Ї–ї–Є–љ–Є–Ї–µ –Ї–∞–Ї –Љ–µ—В–Њ–і, –њ–Њ–Љ–Њ–≥–∞—О—Й–Є–є –≤—Л–±—А–∞—В—М –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л–є –і–Њ—Б—В—Г–њ –і–ї—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П –њ—Г–љ–Ї—Ж–Є–Њ–љ–љ–Њ–є –±–Є–Њ–њ—Б–Є–Є –њ–µ—З–µ–љ–Є, –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є—П –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П –і—А—Г–≥–Є—Е –Љ–∞–љ–Є–њ—Г–ї—П—Ж–Є–є.
–Я–Њ–і–≥–Њ—В–Њ–≤–Ї–∞ –њ–∞—Ж–Є–µ–љ—В–∞. –Ч–∞ 3 –і–љ—П –і–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–∞—Ж–Є–µ–љ—В—Г —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –Є—Б–Ї–ї—О—З–Є—В—М –Є–Ј –њ–Є—В–∞–љ–Є—П –Љ–Њ–ї–Њ–Ї–Њ, —З–µ—А–љ—Л–є —Е–ї–µ–±, —Д—А—Г–Ї—В—Л –Є –Њ–≤–Њ—Й–Є, —Б–ї–∞–і–Ї–Є–µ —Б–Њ–Ї–Є –Є –і—А—Г–≥–Є–µ –њ—А–Њ–і—Г–Ї—В—Л, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є–µ –≥–∞–Ј–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О –≤ –Ї–Є—И–µ—З–љ–Є–Ї–µ. –Я—А–Є —Б–Ї–ї–Њ–љ–љ–Њ—Б—В–Є –Ї –Љ–µ—В–µ–Њ—А–Є–Ј–Љ—Г —Б–ї–µ–і—Г–µ—В –љ–∞–Ј–љ–∞—З–Є—В—М —Д–µ—А–Љ–µ–љ—В–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (—Д–µ—Б—В–∞–ї, –њ–∞–љ–Ј–Є–љ–Њ—А–Љ –Є –і—А.) –Є –∞–і—Б–Њ—А–±–µ–љ—В—Л (–∞–Ї—В–Є–≤–Є—А–Њ–≤–∞–љ–љ—Л–є —Г–≥–Њ–ї—М, –љ–∞—Б—В–Њ–є —А–Њ–Љ–∞—И–Ї–Є –Є –і—А.).
–Т–µ—З–µ—А–Њ–Љ –љ–∞–Ї–∞–љ—Г–љ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є —Г—В—А–Њ–Љ –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –њ–µ—А–µ–і –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ —Б—В–∞–≤—П—В –і–≤–µ –Њ—З–Є—Б—В–Є—В–µ–ї—М–љ—Л–µ –Ї–ї–Є–Ј–Љ—Л. –Т–њ—А–Њ—З–µ–Љ, —Н—В–∞ –њ—А–Њ—Ж–µ–і—Г—А–∞ –љ–µ —П–≤–ї—П–µ—В—Б—П –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ–є –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–∞ –Љ–µ—В–µ–Њ—А–Є–Ј–Љ–∞.
–Я—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є —Н–Ї—Б—В—А–µ–љ–љ–Њ–≥–Њ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–њ–µ—Ж–Є–∞–ї—М–љ–∞—П –њ–Њ–і–≥–Њ—В–Њ–≤–Ї–∞ –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –љ–µ –њ—А–Њ–≤–Њ–і–Є—В—Б—П.
–°–ї–µ–і—Г–µ—В –њ–Њ–Љ–љ–Є—В—М, —З—В–Њ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Њ—А–≥–∞–љ–Њ–≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –њ—А–Њ–≤–Њ–і–Є—В—М –љ–µ —А–∞–љ–µ–µ, —З–µ–Љ —З–µ—А–µ–Ј 2 —Б—Г—В–Њ–Ї –њ–Њ—Б–ї–µ —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –ґ–µ–ї—Г–і–Ї–∞ —Б –Ї–Њ–љ—В—А–∞—Б—В–Є—А–Њ–≤–∞–љ–Є–µ–Љ –Є–ї–Є —Н–Ј–Њ—Д–∞–≥–Њ–≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–Њ—Б–Ї–Њ–њ–Є–Є –Є —З–µ—А–µ–Ј 3вАУ5 –і–љ–µ–є –њ–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –ї–∞–њ–∞—А–Њ—Б–Ї–Њ–њ–Є–Є –Є–ї–Є –њ–љ–µ–≤–Љ–Њ–њ–µ—А–Є—В–Њ–љ–µ—Г–Љ–∞.
–Ґ–µ—Е–љ–Є–Ї–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –≠—Е–Њ–≥—А–∞—Д–Є—О –њ–µ—З–µ–љ–Є –Њ—Б—Г—Й–µ—Б—В–≤–ї—П—О—В –Њ–±—Л—З–љ–Њ –Є–Ј —Б—Г–±–Ї–Њ—Б—В–∞–ї—М–љ–Њ–≥–Њ –Є/–Є–ї–Є –Є–љ—В–µ—А–Ї–Њ—Б—В–∞–ї—М–љ–Њ–≥–Њ –і–Њ—Б—В—Г–њ–∞ –≤ —А–µ–∞–ї—М–љ–Њ–Љ –Љ–∞—Б—И—В–∞–±–µ –≤—А–µ–Љ–µ–љ–Є. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–µ—З–µ–љ–Є –њ—А–Њ–≤–Њ–і—П—В –≤–Њ –≤—А–µ–Љ—П –Ј–∞–і–µ—А–ґ–Ї–Є –і—Л—Е–∞–љ–Є—П –љ–∞ –≤–і–Њ—Е–µ, –Ї–Њ–≥–і–∞ –њ–µ—З–µ–љ—М –љ–µ–Љ–љ–Њ–≥–Њ –Њ–њ—Г—Б–Ї–∞–µ—В—Б—П –≤–љ–Є–Ј –Є —Б—В–∞–љ–Њ–≤–Є—В—Б—П –±–Њ–ї–µ–µ –і–Њ—Б—В—Г–њ–љ–Њ–є –і–ї—П –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є. –Я—А–Є –њ—А–Њ–і–Њ–ї—М–љ–Њ–Љ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–Є –≤ —Н–њ–Є–≥–∞—Б—В—А–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є –і–∞—В—З–Є–Ї —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—О—В –љ–∞ 2 —Б–Љ –≤–ї–µ–≤–Њ –Њ—В –њ–µ—А–µ–і–љ–µ–є —Б—А–µ–і–Є–љ–љ–Њ–є –ї–Є–љ–Є–Є, –њ—А–Є –њ–Њ–њ–µ—А–µ—З–љ–Њ–Љ вАФ –і–∞—В—З–Є–Ї –њ–µ—А–µ–Љ–µ—Й–∞—О—В –Ї –њ—Г–њ–Ї—Г (—А–Є—Б.¬†1). –Ш—Б–њ–Њ–ї—М–Ј—Г—О—В —В–∞–Ї–ґ–µ —В–µ—Е–љ–Є–Ї—Г —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ–Њ–≥–Њ ¬Ђ–Ї–Њ—Б–Њ–≥–Њ¬ї —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є—П –њ–µ—З–µ–љ–Є, –Ї–Њ–≥–і–∞ –£–Ч-–і–∞—В—З–Є–Ї —А–∞—Б–њ–Њ–ї–∞–≥–∞–µ—В—Б—П –њ–∞—А–∞–ї–ї–µ–ї—М–љ–Њ –њ—А–∞–≤–Њ–є —А–µ–±–µ—А–љ–Њ–є –і—Г–≥–µ –њ–Њ–і —Г–≥–ї–Њ–Љ 45¬∞ –≤ –Ї—А–∞–љ–Є–∞–ї—М–љ–Њ–Љ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–Є, –Є –і—А—Г–≥–Є–µ –њ–Њ–Ј–Є—Ж–Є–Є –і–∞—В—З–Є–Ї–∞.

–†–Є—Б. 1. –£–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–µ—З–µ–љ–Є
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ —Г–і–∞–µ—В—Б—П –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А–Њ–≤–∞—В—М –њ—А–∞–≤—Г—О –Є –ї–µ–≤—Г—О –і–Њ–ї–Є –њ–µ—З–µ–љ–Є, –ґ–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М, –Њ–±—Й–Є–є –њ–µ—З–µ–љ–Њ—З–љ—Л–є, –Њ–±—Й–Є–є –ґ–µ–ї—З–љ—Л–є –њ—А–Њ—В–Њ–Ї–Є, –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Є–µ —Б—В—А—Г–Ї—В—Г—А—Л, –≤—Е–Њ–і—П—Й–Є–µ –≤ —Б–Њ—Б—В–∞–≤ –≤–Њ—А–Њ—В –њ–µ—З–µ–љ–Є, –≥–Њ–ї–Њ–≤–Ї—Г –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Ј–∞–Ї–∞–љ—З–Є–≤–∞–µ—В—Б—П —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –і–ї—П –≤—Л—П–≤–ї–µ–љ–Є—П —Б–≤–Њ–±–Њ–і–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є.
–Р–љ–∞–ї–Є–Ј –Є –Є–љ—В–µ—А–њ—А–µ—В–∞—Ж–Є—П —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є
–Э–Њ—А–Љ–∞–ї—М–љ–∞—П —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–∞—П –Ї–∞—А—В–Є–љ–∞ –њ–µ—З–µ–љ–Є
–Э–∞ —А–Є—Б. 2. –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –љ–Њ—А–Љ–∞–ї—М–љ–∞—П —Н—Е–Њ–≥—А–∞–Љ–Љ–∞ –њ–µ—З–µ–љ–Є. –£ –Ј–і–Њ—А–Њ–≤–Њ–≥–Њ —З–µ–ї–Њ–≤–µ–Ї–∞ —Б–∞–≥–Є—В—В–∞–ї—М–љ—Л–µ —А–∞–Ј–Љ–µ—А—Л –њ–µ—З–µ–љ–Є –њ–Њ —Б—А–µ–і–Є–љ–љ–Њ-–Ї–ї—О—З–Є—З–љ–Њ–є –ї–Є–љ–Є–Є —Б–Њ—Б—В–∞–≤–ї—П—О—В, –≤ —Б—А–µ–і–љ–µ–Љ, 10,5¬±1,5 —Б–Љ —Б –Ї–Њ–ї–µ–±–∞–љ–Є—П–Љ–Є –Њ—В 9 –і–Њ 12 —Б–Љ, –∞ –њ–Њ –њ–µ—А–µ–і–љ–µ–є —Б—А–µ–і–Є–љ–љ–Њ–є –ї–Є–љ–Є–Є вАФ 8,3¬±1,7 —Б–Љ. –Я–Њ–њ–µ—А–µ—З–љ–Є–Ї –њ–µ—З–µ–љ–Є вАФ 20вАУ22,5 —Б–Љ.
–Э–Є–ґ–љ–Є–є —Г–≥–Њ–ї –њ–µ—З–µ–љ–Є, –Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л–є –і–Њ—А–Ј–∞–ї—М–љ–Њ–є –Є –≤–µ–љ—В—А–∞–ї—М–љ–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—П–Љ–Є –Њ—А–≥–∞–љ–∞ вАФ –Њ—Б—В—А—Л–є: –≤ –Њ–±–ї–∞—Б—В–Є –ї–µ–≤–Њ–є –і–Њ–ї–Є –Њ–љ –љ–µ –њ—А–µ–≤—Л—И–∞–µ—В 45¬∞, –∞ –≤ –Њ–±–ї–∞—Б—В–Є –њ—А–∞–≤–Њ–є –і–Њ–ї–Є вАФ 75¬∞.

–†–Є—Б. 2. –Э–Њ—А–Љ–∞–ї—М–љ–∞—П —Н—Е–Њ–≥—А–∞–Љ–Љ–∞ –њ–µ—З–µ–љ–Є.
–•–Њ—А–Њ—И–Њ –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А—Г–µ—В—Б—П –≤–Њ—А–Њ—В–љ–∞—П –≤–µ–љ–∞ (–≤ —Ж–µ–љ—В—А–µ), –њ–Њ–і –љ–µ–є - –њ—А–∞–≤–∞—П –њ–µ—З–µ–љ–Њ—З–љ–∞—П –≤–µ–љ–∞ (–њ—А–Њ–і–Њ–ї—М–љ—Л–є —Б—А–µ–Ј)
 
–Т –љ–Њ—А–Љ–µ –Ї–Њ–љ—В—Г—А—Л –њ–µ—З–µ–љ–Є –њ–Њ—З—В–Є –љ–∞ –≤—Б–µ–Љ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є —З–µ—В–Ї–Є–µ –Є —А–Њ–≤–љ—Л–µ. –Я–µ—З–µ–љ—М –Є–Љ–µ–µ—В –≥–Њ–Љ–Њ–≥–µ–љ–љ–Њ–µ —Б—В—А–Њ–µ–љ–Є–µ —Б —А–∞–≤–љ–Њ–Љ–µ—А–љ—Л–Љ –Њ–і–Є–љ–∞–Ї–Њ–≤—Л–Љ –њ–Њ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ–Љ —Б–Є–≥–љ–∞–ї–Њ–≤, –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–µ–Љ —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А (—Б–Њ—Б—Г–і—Л, —Б–≤—П–Ј–Ї–Є, –њ—А–Њ—В–Њ–Ї–Є). –Я–Њ—Б—В–Њ—П–љ–љ–Њ –ї–Њ—Ж–Є—А—Г–µ—В—Б—П –љ–Є–ґ–љ—П—П –њ–Њ–ї–∞—П –≤–µ–љ–∞ –≤ –≤–Є–і–µ –ї–µ–љ—В–Њ–Њ–±—А–∞–Ј–љ–Њ–≥–Њ —Н—Е–Њ–љ–µ–≥–∞—В–Є–≤–љ–Њ–≥–Њ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –і–Є–∞–Љ–µ—В—А–Њ–Љ –і–Њ 15 –Љ–Љ.
–Я–Њ—А—В–∞–ї—М–љ–∞—П –≤–µ–љ–∞ –њ–Њ—Б–ї–µ –µ–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –Є–Ј –≤–µ—А—Е–љ–µ–±—А—Л–ґ–µ—З–љ–Њ–є –Є —Б–µ–ї–µ–Ј–µ–љ–Њ—З–љ–Њ–є –≤–µ–љ –≤–њ–∞–і–∞–µ—В –≤ –≤–Њ—А–Њ—В–∞ –њ–µ—З–µ–љ–Є, –Ї–Њ—В–Њ—А—Л–µ –ї–Њ—Ж–Є—А—Г—О—В—Б—П –њ—А–Є –њ–Њ–њ–µ—А–µ—З–љ–Њ–Љ –Є —Б–∞–≥–Є—В—В–∞–ї—М–љ–Њ–Љ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є –Ј–Њ–љ–і–∞. –Т–љ—Г—В—А–Є–њ–µ—З–µ–љ–Њ—З–љ—Л–µ –њ—А–Њ—В–Њ–Ї–Є –≤ –љ–Њ—А–Љ–µ –њ—А–Њ—Б–ї–µ–ґ–Є–≤–∞—О—В—Б—П —Б —В—А—Г–і–Њ–Љ, –Є—Е –њ—А–Њ—Б–≤–µ—В —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –Њ—В –њ–µ—А–Є—Д–µ—А–Є–Є –Ї –≤–Њ—А–Њ—В–∞–Љ –њ–µ—З–µ–љ–Є. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В –≤–µ–љ –≤–љ—Г—В—А–Є–њ–µ—З–µ–љ–Њ—З–љ—Л–µ –њ—А–Њ—В–Њ–Ї–Є –ї–Є—И–µ–љ—Л —Б—В–µ–љ–Њ–Ї.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –љ–Њ—А–Љ–∞–ї—М–љ–∞—П —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–∞—П –Ї–∞—А—В–Є–љ–∞ –њ–µ—З–µ–љ–Є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –љ–∞–ї–Є—З–Є–µ–Љ –Љ–µ–ї–Ї–Є—Е, –љ–µ–Є–љ—В–µ–љ—Б–Є–≤–љ—Л—Е, –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –і–∞–ї–µ–Ї–Њ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л—Е –і—А—Г–≥ –Њ—В –і—А—Г–≥–∞ —Н—Е–Њ—Б–Є–≥–љ–∞–ї–Њ–≤, –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —З–µ–≥–Њ –Љ–µ–ґ–і—Г –љ–Є–Љ–Є –Њ—Б—В–∞—О—В—Б—П —Н—Е–Њ–љ–µ–≥–∞—В–Є–≤–љ—Л–µ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–∞. –≠—Е–Њ—Б–Є–≥–љ–∞–ї—Л –≥–Њ–Љ–Њ–≥–µ–љ–љ—Л –њ–Њ —А–∞–Ј–Љ–µ—А—Г –Є —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ—Л –њ–Њ –≤—Б–µ–є –њ–µ—З–µ–љ–Є. –Я–Њ—А—В–∞–ї—М–љ—Л–µ —Б–Њ—Б—Г–і—Л –њ—А–Њ—Б–ї–µ–ґ–Є–≤–∞—О—В—Б—П –њ–Њ –њ–µ—А–Є—Д–µ—А–Є–Є –њ–µ—З–µ–љ–Є; —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А–∞ –Є—Е —Б—В–µ–љ–Њ–Ї –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–∞, —З–µ–Љ —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А–∞ –Њ–Ї—А—Г–ґ–∞—О—Й–µ–є –Є—Е –њ–∞—А–µ–љ—Е–Є–Љ—Л –њ–µ—З–µ–љ–Є, –Ј–≤—Г–Ї–Њ–њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В—М –њ–µ—З–µ–љ–Є –њ–Њ–ї–љ–Њ—Б—В—М—О —Б–Њ—Е—А–∞–љ–µ–љ–∞; —Б–∞–≥–Є—В—В–∞–ї—М–љ—Л–є —А–∞–Ј–Љ–µ—А —Б–Њ—Б—В–∞–≤–ї—П–µ—В 9вАУ12 —Б–Љ; –њ–µ—З–µ–љ—М —Н–ї–∞—Б—В–Є—З–љ–∞—П –Є –Є–Љ–µ–µ—В —А–Њ–≤–љ—Л–є, —З–µ—В–Ї–Є–є –Ї–Њ–љ—В—Г—А.
–Ф–Є—Д—Д—Г–Ј–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–µ—З–µ–љ–Є
–Ъ —З–Є—Б–ї—Г –љ–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л—Е –і–Є—Д—Д—Г–Ј–љ—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є –њ–µ—З–µ–љ–Є –Њ—В–љ–Њ—Б—П—В—Б—П –≥–µ–њ–∞—В–Є—В—Л (–Њ—Б—В—А—Л–µ –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–µ), –ґ–Є—А–Њ–≤–∞—П –і–Є—Б—В—А–Њ—Д–Є—П –Є —Ж–Є—А—А–Њ–Ј—Л –њ–µ—З–µ–љ–Є. –Я—А–∞–≤–Є–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј –њ—А–Є —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Ј–∞–≤–Є—Б–Є—В –Њ—В —Ж–µ–ї–Њ–≥–Њ —А—П–і–∞ –Њ–±—К–µ–Ї—В–Є–≤–љ—Л—Е –Є —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л—Е –њ—А–Є—З–Є–љ (—В–∞–±–ї.¬†1). –Ъ –њ–µ—А–≤—Л–Љ –Є–Ј –љ–Є—Е –Њ—В–љ–Њ—Б—П—В —В–Є–њ –њ—А–Є–±–Њ—А–∞, –µ–≥–Њ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М, —А–∞–Ј—А–µ—И–∞—О—Й—Г—О —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М, –љ–∞–ї–Є—З–Є–µ —Д–∞–Ї—В–Њ—А–Њ–≤, —Г—Е—Г–і—И–∞—О—Й–Є—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–µ (–Њ–ґ–Є—А–µ–љ–Є–µ, –≥–∞–Ј–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –≤ –Ї–Є—И–µ—З–љ–Є–Ї–µ –Є –і—А.). –С–Њ–ї—М—И–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ—О—В –Њ–њ—Л—В —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–∞ –Є —В—Й–∞—В–µ–ї—М–љ–Њ—Б—В—М –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Э–∞–Є–±–Њ–ї—М—И–Є–µ —В—А—Г–і–љ–Њ—Б—В–Є –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –і–Є–∞–≥–љ–Њ–Ј —А–∞–љ–љ–Є—Е —Б—В–∞–і–Є–є –ґ–Є—А–Њ–≤–Њ–є –і–Є—Б—В—А–Њ—Д–Є–Є –Є —Ж–Є—А—А–Њ–Ј–∞ –њ–µ—З–µ–љ–Є.
–Ґ–∞–±–ї–Є—Ж–∞ 1. ¬†–І–∞—Б—В–Њ—В–∞ –њ—А–∞–≤–Є–ї—М–љ–Њ–≥–Њ —Н—Е–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Њ–≥–Њ –і–Є–∞–≥–љ–Њ–Ј–∞ –њ—А–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є—Е—Б—П –і–Є—Д—Д—Г–Ј–љ—Л–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –њ–µ—З–µ–љ–Є (–≤ –њ—А–Њ—Ж–µ–љ—В–∞—Е)
| –•—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –≥–µ–њ–∞—В–Є—В | –Ц–Є—А–Њ–≤–∞—П –і–Є—Б—В—А–Њ—Д–Є—П |
–¶–Є—А—А–Њ–Ј –њ–µ—З–µ–љ–Є |
| 52вАУ63 | 80вАУ92 | 58вАУ83 |

–†–Є—Б. 3. –≠—Е–Њ–≥—А–∞–Љ–Љ–∞ –њ–µ—З–µ–љ–Є —Г –±–Њ–ї—М–љ–Њ–≥–Њ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –≥–µ–њ–∞—В–Є—В–Њ–Љ
–Я—А–Є –Њ—Б—В—А—Л—Е –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –≥–µ–њ–∞—В–Є—В–∞—Е —Н—Е–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–∞—П –Ї–∞—А—В–Є–љ–∞ –≤–µ—Б—М–Љ–∞ –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–љ–∞. –Ю–±—Л—З–љ–Њ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –њ–µ—З–µ–љ–Є –Ј–∞ —Б—З–µ—В –Њ–і–љ–Њ–є –Є–ї–Є –Њ–±–µ–Є—Е –і–Њ–ї–µ–є, –Ј–∞–Ї—А—Г–≥–ї–µ–љ–Є–µ –µ–µ –Ї—А–∞–µ–≤. –≠—Е–Њ—Б—В—А—Г–Ї—В—Г—А–∞ —З–∞—Б—В–Њ –љ–Њ—А–Љ–∞–ї—М–љ–∞, —Б–ї–∞–±–Њ—Н—Е–Њ–≥–µ–љ–љ–∞ (—А–Є—Б.¬†3). –Ы–Є—И—М –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ —В–µ—З–µ–љ–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А–∞ –њ–µ—З–µ–љ–Є —Б—В–∞–љ–Њ–≤–Є—В—Б—П ¬Ђ–њ–µ—Б—В—А–Њ–є¬ї –Є –љ–∞–±–ї—О–і–∞–µ—В—Б—П —З–µ—А–µ–і–Њ–≤–∞–љ–Є–µ —Г—З–∞—Б—В–Ї–Њ–≤ —Б–ї–∞–±–Њ–є –Є –≤—Л—Б–Њ–Ї–Њ–є —Н—Е–Њ–≥–µ–љ–љ–Њ—Б—В–Є. –Т –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Б–ї—Г—З–∞—П—Е, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –њ—А–Є —А–∞–Ј–≤–Є—В–Є–Є –њ–Њ—А—В–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є, –Љ–Њ–ґ–љ–Њ –Њ–±–љ–∞—А—Г–ґ–Є—В—М —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–µ–ї–µ–Ј–µ–љ–Ї–Є –Є —А–∞—Б—И–Є—А–µ–љ–Є–µ —Б–µ–ї–µ–Ј–µ–љ–Њ—З–љ–Њ–є –Є –њ–Њ—А—В–∞–ї—М–љ–Њ–є –≤–µ–љ—Л.
–Ц–Є—А–Њ–≤–∞—П –і–Є—Б—В—А–Њ—Д–Є—П –њ–µ—З–µ–љ–Є (–ґ–Є—А–Њ–≤–Њ–є –≥–µ–њ–∞—В–Њ–Ј). –Ю—Б–љ–Њ–≤–љ—Л–Љ —Н—Е–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–Љ –њ—А–Є–Ј–љ–∞–Ї–Њ–Љ –ґ–Є—А–Њ–≤–Њ–є –і–Є—Б—В—А–Њ—Д–Є–Є –њ–µ—З–µ–љ–Є —П–≤–ї—П–µ—В—Б—П —Г—Б–Є–ї–µ–љ–Є–µ —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А—Л –њ–µ—З–µ–љ–Є –≤ –≤–Є–і–µ —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ–≥–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Є —А–∞–Ј–Љ–µ—А–Њ–≤ —Н—Е–Њ—Б–Є–≥–љ–∞–ї–Њ–≤. –≠—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –Њ—В–ї–Њ–ґ–µ–љ–Є–µ–Љ –ґ–Є—А–∞ –≤ –њ–µ—З–µ–љ–Њ—З–љ—Л—Е –і–Њ–ї—М–Ї–∞—Е, —А–∞—Б—Б—В–Њ—П–љ–Є–µ –Љ–µ–ґ–і—Г –Ї–Њ—В–Њ—А—Л–Љ–Є –Є –Є—Е —А–∞–Ј–Љ–µ—А—Л —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В—Б—П –љ–∞—Б—В–Њ–ї—М–Ї–Њ, —З—В–Њ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л–µ –≤–Њ–ї–љ—Л –Њ—В—А–∞–ґ–∞—О—В—Б—П –Њ—В –љ–Є—Е.
–Ъ —З–Є—Б–ї—Г –≤–∞–ґ–љ—Л—Е, –љ–Њ –Љ–µ–љ–µ–µ —Б–њ–µ—Ж–Є—Д–Є—З–љ—Л—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –Њ—В–љ–Њ—Б—П—В—Б—П —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —А–∞–Ј–Љ–µ—А–Њ–≤ –њ–µ—З–µ–љ–Є, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –љ–Є–ґ–љ–µ–≥–Њ —Г–≥–ї–∞ –ї–µ–≤–Њ–є –і–Њ–ї–Є –±–Њ–ї–µ–µ 45¬∞, –љ–µ—З–µ—В–Ї–Њ—Б—В—М –Ї–Њ–љ—В—Г—А–Њ–≤ –њ–µ—З–µ–љ–Є –Є –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –≤—Л—П–≤–ї–µ–љ–Є—П –≤–Њ—А–Њ—В–љ–Њ–є –≤–µ–љ—Л.
–≠—Е–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–∞—П –Ї–∞—А—В–Є–љ–∞ –њ—А–Є –ґ–Є—А–Њ–≤–Њ–є –і–Є—Б—В—А–Њ—Д–Є–Є –њ–µ—З–µ–љ–Є –Ј–∞–≤–Є—Б–Є—В –Њ—В —Б—В–µ–њ–µ–љ–Є –≤–Њ–≤–ї–µ—З–µ–љ–Є—П –≤ –њ—А–Њ—Ж–µ—Б—Б –њ–µ—З–µ–љ–Њ—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї. –Я—А–Є –њ–µ—А–≤–Њ–є —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–µ—З–µ–љ—М –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Г–≤–µ–ї–Є—З–µ–љ–∞, –Ї—А–∞–є –Ј–∞–Ї—А—Г–≥–ї–µ–љ. –≠—Е–Њ—Б—В—А—Г–Ї—В—Г—А–∞ –Є–Љ–µ–µ—В –њ–µ—Б—В—А—Г—О –Ї–∞—А—В–Є–љ—Г, –њ–∞—А–µ–љ—Е–Є–Љ–∞ –љ–µ—А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ –Љ–µ–ї–Ї–Њ–Њ—З–∞–≥–Њ–≤–Њ —Г–њ–ї–Њ—В–љ–µ–љ–∞. –≠—В–Њ —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–є ¬Ђ–Њ—Б—В—А–Њ–≤–Ї–Њ–≤—Л–є¬ї –≤–Є–і –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–µ—З–µ–љ–Є, –Ї–Њ—В–Њ—А—Л–є –≤—Б—В—А–µ—З–∞–µ—В—Б—П –Є –њ—А–Є –≥–µ–њ–∞—В–Є—В–∞—Е. –Я—А–Є –≤—В–Њ—А–Њ–є —Б—В–∞–і–Є–Є –њ–µ—З–µ–љ—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –±–Њ–ї—М—И–µ–≥–Њ —А–∞–Ј–Љ–µ—А–∞, –љ–Є–ґ–љ–Є–є –Ї—А–∞–є –Ј–∞–Ї—А—Г–≥–ї–µ–љ, —Б—В—А—Г–Ї—В—Г—А–∞ –њ–∞—А–µ–љ—Е–Є–Љ—Л –Љ–µ–ї–Ї–Њ–Њ—З–∞–≥–Њ–≤–∞—П, –њ–µ—З–µ–љ—М –і–Є—Д—Д—Г–Ј–љ–Њ –Є —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ —Г–њ–ї–Њ—В–љ–µ–љ–∞. –Я—А–Є —В—А–µ—В—М–µ–є —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–µ—З–µ–љ—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л—Е —А–∞–Ј–Љ–µ—А–Њ–≤ –Ј–∞ —Б—З–µ—В —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Њ–±–µ–Є—Е –і–Њ–ї–µ–є. –Ю–љ–∞ –Є–Љ–µ–µ—В –Њ–Ї—А—Г–≥–ї—Г—О —Д–Њ—А–Љ—Г. –°—В—А—Г–Ї—В—Г—А–∞ –њ–∞—А–µ–љ—Е–Є–Љ—Л –≤—Л—Б–Њ–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є (—Н—Е–Њ–≥–µ–љ–љ–Њ—Б—В–Є), –њ–Њ—А—В–∞–ї—М–љ—Л–µ —Б–Њ—Б—Г–і—Л –љ–µ –ї–Њ—Ж–Є—А—Г—О—В—Б—П.
–¶–Є—А—А–Њ–Ј –њ–µ—З–µ–љ–Є. –Т—Л–і–µ–ї—П—О—В –њ—А—П–Љ—Л–µ –Є –Ї–Њ—Б–≤–µ–љ–љ—Л–µ —Н—Е–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Є —Ж–Є—А—А–Њ–Ј–∞ –њ–µ—З–µ–љ–Є (—В–∞–±–ї. 2). –Ф–Є–∞–≥–љ–Њ–Ј —Ж–Є—А—А–Њ–Ј–∞ –њ–µ—З–µ–љ–Є —Б—З–Є—В–∞–µ—В—Б—П –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ, –µ—Б–ї–Є –њ—А–Є —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤—Л—П–≤–ї—П—О—В—Б—П 3 –њ—А—П–Љ—Л—Е –Є–ї–Є 2 –њ—А—П–Љ—Л—Е –Є 2 –Ї–Њ—Б–≤–µ–љ–љ—Л—Е –њ—А–Є–Ј–љ–∞–Ї–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П.
–Ґ–∞–±–ї–Є—Ж–∞ 2. –Я—А—П–Љ—Л–µ –Є –Ї–Њ—Б–≤–µ–љ–љ—Л–µ —Н—Е–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Є —Ж–Є—А—А–Њ–Ј–∞ –њ–µ—З–µ–љ–Є
| –Я—А—П–Љ—Л–µ –њ—А–Є–Ј–љ–∞–Ї–Є | –Ъ–Њ—Б–≤–µ–љ–љ—Л–µ –њ—А–Є–Ј–љ–∞–Ї–Є |
| –Ш–Ј–Љ–µ–љ–µ–љ–Є–µ —А–∞–Ј–Љ–µ—А–Њ–≤ –њ–µ—З–µ–љ–Є | –£–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–µ–ї–µ–Ј–µ–љ–Ї–Є |
| –Ш–Ј–Љ–µ–љ–µ–љ–Є–µ —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А—Л | –Р—Б—Ж–Є—В |
| –Э–µ—А–Њ–≤–љ–Њ—Б—В—М –Ї–Њ–љ—В—Г—А–Њ–≤ –њ–µ—З–µ–љ–Є | –†–∞—Б—И–Є—А–µ–љ–Є–µ –≤–Њ—А–Њ—В–љ–Њ–є –Є —Б–µ–ї–µ–Ј–µ–љ–Њ—З–љ–Њ–є –≤–µ–љ |
| –Ч–∞–Ї—А—Г–≥–ї–µ–љ–Є–µ –љ–Є–ґ–љ–µ–≥–Њ –Ї—А–∞—П | ¬† |
| –°–љ–Є–ґ–µ–љ–Є–µ —Н–ї–∞—Б—В–Є—З–љ–Њ—Б—В–Є –Є –Ј–≤—Г–Ї–Њ–њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В–Є | ¬† |
–Т –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ —А–∞–Ј–Љ–µ—А—Л –њ–µ—З–µ–љ–Є —Г–≤–µ–ї–Є—З–µ–љ—Л, –љ–µ—А–µ–і–Ї–Њ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Ј–∞ —Б—З–µ—В –ї–µ–≤–Њ–є –і–Њ–ї–Є –њ–µ—З–µ–љ–Є. –Т –Ї–Њ–љ–µ—З–љ–Њ–є —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ—А–Є –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–Є –∞—В—А–Њ—Д–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ —А–∞–Ј–Љ–µ—А—Л –Њ—А–≥–∞–љ–∞ —Г–Љ–µ–љ—М—И–∞—О—В—Б—П.
–•–∞—А–∞–Ї—В–µ—А–љ–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –Ј–∞–Ї—А—Г–≥–ї–µ–љ–Є–µ –љ–Є–ґ–љ–µ–≥–Њ –Ї—А–∞—П –њ–µ—З–µ–љ–Є –Є –љ–µ—А–Њ–≤–љ–Њ—Б—В—М –µ–µ –Ї–Њ–љ—В—Г—А–Њ–≤.
–≠—Е–Њ—Б—В—А—Г–Ї—В—Г—А–∞ –њ–µ—З–µ–љ–Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П –Ј–∞ —Б—З–µ—В –њ–Њ—П–≤–ї–µ–љ–Є—П –±–Њ–ї–µ–µ —З–∞—Б—В—Л—Е –Є –Ї—А—Г–њ–љ—Л—Е —Н—Е–Њ—Б–Є–≥–љ–∞–ї–Њ–≤, —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є –њ–µ—А–µ—Б—В—А–Њ–є–Ї–Њ–є –∞—А—Е–Є—В–µ–Ї—В–Њ–љ–Є–Ї–Є –њ–µ—З–µ–љ–Є, —Е–∞—А–∞–Ї—В–µ—А–љ–Њ–є –і–ї—П —Ж–Є—А—А–Њ–Ј–∞. –Я—А–Є –∞—В—А–Њ—Д–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Є —А–∞–Ј–Љ–µ—А —Н—Е–Њ—Б–Є–≥–љ–∞–ї–Њ–≤ —Б–љ–Є–ґ–∞—О—В—Б—П.
–Э–∞–Ї–Њ–љ–µ—Ж, –≤–∞–ґ–љ—Л–Љ–Є –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є —Ж–Є—А—А–Њ–Ј–∞ —П–≤–ї—П–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ —Н–ї–∞—Б—В–Є—З–љ–Њ—Б—В–Є –Є –Ј–≤—Г–Ї–Њ–њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В–Є –њ–µ—З–µ–љ–Є.
–Ъ–Њ—Б–≤–µ–љ–љ—Л–µ —Н—Е–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Є —Ж–Є—А—А–Њ–Ј–∞ —Б–≤—П–Ј–∞–љ—Л –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ —Б–Є–љ–і—А–Њ–Љ–∞ –њ–Њ—А—В–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є. –†–∞—Б—И–Є—А–µ–љ–Є–µ —Б–µ–ї–µ–Ј–µ–љ–Њ—З–љ–Њ–є –≤–µ–љ—Л –±–Њ–ї—М—И–µ 10 –Љ–Љ –Є –њ–Њ—А—В–∞–ї—М–љ–Њ–є –≤–µ–љ—Л –±–Њ–ї—М—И–µ 15 –Љ–Љ —Б—З–Є—В–∞—О—В –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ–Є –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є –њ–Њ–≤—Л—И–µ–љ–Є—П –і–∞–≤–ї–µ–љ–Є—П –≤ —Б–Є—Б—В–µ–Љ–µ v. porta.
–£–≤–µ–ї–Є—З–µ–љ–Є–µ —А–∞–Ј–Љ–µ—А–Њ–≤ —Б–µ–ї–µ–Ј–µ–љ–Ї–Є –Є —Г—Б–Є–ї–µ–љ–Є–µ –µ–µ —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А—Л –љ–∞–±–ї—О–і–∞—О—В—Б—П –≤ 60вАУ70% —Б–ї—Г—З–∞–µ–≤ —Ж–Є—А—А–Њ–Ј–∞ –њ–µ—З–µ–љ–Є, —Е–Њ—В—П —Н—В–Њ—В –њ—А–Є–Ј–љ–∞–Ї –љ–µ —П–≤–ї—П–µ—В—Б—П —Б–њ–µ—Ж–Є—Д–Є—З–љ—Л–Љ —В–Њ–ї—М–Ї–Њ –і–ї—П –њ–Њ—А—В–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є.
–Р—Б—Ж–Є—В–Є—З–µ—Б–Ї–∞—П –ґ–Є–і–Ї–Њ—Б—В—М –≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –њ—А–Є —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤—Л–≥–ї—П–і–Є—В –Ї–∞–Ї —Н—Е–Њ–љ–µ–≥–∞—В–Є–≤–љ–∞—П —Б—В—А—Г–Ї—В—Г—А–∞, –Ї–Њ—В–Њ—А–∞—П —Б–Ї–∞–њ–ї–Є–≤–∞–µ—В—Б—П –≤ –±–Њ–Ї–Њ–≤—Л—Е —З–∞—Б—В—П—Е –ґ–Є–≤–Њ—В–∞, –≤ –Љ–∞–ї–Њ–Љ —В–∞–Ј—Г –Є–ї–Є (–њ—А–Є –Љ–∞–ї—Л—Е –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞—Е –ґ–Є–і–Ї–Њ—Б—В–Є) —А–∞—Б–њ–Њ–ї–∞–≥–∞–µ—В—Б—П –≤–Њ–Ї—А—Г–≥ –њ–µ—З–µ–љ–Є. –Т —Н—В–Є—Е —Б–ї—Г—З–∞—П—Е —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Є –њ–µ—А–µ–Љ–µ–љ–µ –њ–Њ–ї–Њ–ґ–µ–љ–Є—П —В–µ–ї–∞ –њ–∞—Ж–Є–µ–љ—В–∞ (–ї–µ–ґ–∞ –Є —Б—В–Њ—П).
¬Ђ–Ч–∞—Б—В–Њ–є–љ–∞—П¬ї –њ–µ—З–µ–љ—М. –Т–Њ –≤—Б–µ—Е —Б–ї—Г—З–∞—П—Е –Ј–∞—Б—В–Њ–є–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –Њ—В–Љ–µ—З–∞—О—В —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —А–∞–Ј–Љ–µ—А–Њ–≤ –њ–µ—З–µ–љ–Є –Є –Ј–∞–Ї—А—Г–≥–ї–µ–љ–Є–µ –µ–µ –Ї—А–∞–µ–≤ (—А–Є—Б.¬†4). –Я–∞—В–Њ–≥–љ–Њ–Љ–Њ–љ–Є—З–љ—Л–Љ –њ—А–Є–Ј–љ–∞–Ї–Њ–Љ ¬Ђ–Ј–∞—Б—В–Њ–є–љ–Њ–є¬ї –њ–µ—З–µ–љ–Є —П–≤–ї—П–µ—В—Б—П —А–∞—Б—И–Є—А–µ–љ–Є–µ –љ–Є–ґ–љ–µ–є –њ–Њ–ї–Њ–є –≤–µ–љ—Л –Є –њ–µ—З–µ–љ–Њ—З–љ—Л—Е –≤–µ–љ, –≤–µ—В–≤–ї–µ–љ–Є–µ –њ–µ—З–µ–љ–Њ—З–љ—Л—Е –≤–µ–љ –њ–Њ–і —Г–≥–ї–Њ–Љ –±–ї–Є–Ј–Ї–Є–Љ –Ї 90¬∞. –•–∞—А–∞–Ї—В–µ—А–љ–Њ, —З—В–Њ –љ–Є–ґ–љ—П—П –њ–Њ–ї–∞—П –≤–µ–љ–∞ —В–µ—А—П–µ—В —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Є–Ј–Љ–µ–љ—П—В—М –і–Є–∞–Љ–µ—В—А –њ—А–Є –і—Л—Е–∞–љ–Є–Є: –Њ–љ–∞ –≤–Њ–Њ–±—Й–µ –љ–µ —Б—Г–ґ–∞–µ—В—Б—П –њ—А–Є –≤–і–Њ—Е–µ –Є–ї–Є —Б—Г–ґ–∞–µ—В—Б—П –Њ—З–µ–љ—М –Љ–∞–ї–Њ.

–†–Є—Б. 4. –≠—Е–Њ–≥—А–∞–Љ–Љ–∞ –њ–µ—З–µ–љ–Є —Г –±–Њ–ї—М–љ–Њ–≥–Њ —Б –Ј–∞—Б—В–Њ–є–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П
–Ю—З–∞–≥–Њ–≤—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ –њ–µ—З–µ–љ–Є
–£–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–µ—З–µ–љ–Є –њ—А–Є –Њ—З–∞–≥–Њ–≤—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є—П—Е –њ–µ—З–µ–љ–Є –±–Њ–ї–µ–µ –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ–Њ, —З–µ–Љ –њ—А–Є –і–Є—Д—Д—Г–Ј–љ—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є—П—Е. –Я—А–Є —Н—В–Њ–Љ –Њ—В–Љ–µ—З–∞—О—В—Б—П –ї–Њ–Ї–∞–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Є–ї–Є —Г—Б–Є–ї–µ–љ–Є–µ —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А—Л, –і–Є—Д—Д—Г–Ј–љ–Њ–µ –Є–ї–Є –Њ—З–∞–≥–Њ–≤–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —А–∞–Ј–Љ–µ—А–Њ–≤ –њ–µ—З–µ–љ–Є –Є –љ–µ—А–Њ–≤–љ–Њ—Б—В—М –µ–µ –Ї–Њ–љ—В—Г—А–∞ —Б –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ –≤—Л–њ—Г–Ї–ї–Њ—Б—В–Є. –Ю–±—К–µ–Љ–љ—Л–µ –Њ—З–∞–≥–Њ–≤—Л–µ –њ—А–Њ—Ж–µ—Б—Б—Л –≤ –њ–µ—З–µ–љ–Є –Љ–Њ–≥—Г—В –≤—Л–Ј—Л–≤–∞—В—М —Б–і–∞–≤–ї–µ–љ–Є–µ –ґ–µ–ї—З–љ—Л—Е –њ—А–Њ—В–Њ–Ї–Њ–≤ —Б –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ–Љ –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Њ–є –ґ–µ–ї—В—Г—Е–Є.
–Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ –њ—А–Є–Ј–љ–∞–Ї–Њ–Љ –Њ—З–∞–≥–Њ–≤—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –њ–µ—З–µ–љ–Є —П–≤–ї—П–µ—В—Б—П –љ–∞—А—Г—И–µ–љ–Є–µ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А—Л –њ–µ—З–µ–љ–Є. –†–∞–Ј–ї–Є—З–∞—О—В –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —В–Є–њ–Њ–≤ –Њ—З–∞–≥–Њ–≤—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А—Л.
-
–Ю—З–∞–≥–Є, –ї–Є—И–µ–љ–љ—Л–µ —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А—Л (–Ї–Є—Б—В—Л –њ–µ—З–µ–љ–Є, –≥–µ–Љ–∞—В–Њ–Љ–∞, –∞–±—Б—Ж–µ—Б—Б –њ–µ—З–µ–љ–Є, –љ–µ–Ї—А–Њ—В–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ –Њ–њ—Г—Е–Њ–ї–Є).
-
–Ю—З–∞–≥–Є —Б–Њ —Б–љ–Є–ґ–µ–љ–љ–Њ–є —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А–Њ–є (–Љ–µ—В–∞—Б—В–∞–Ј—Л –љ–Є–Ј–Ї–Њ–і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —А–∞–Ї–∞, —Б–∞—А–Ї–Њ–Љ–∞, –Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ–∞—П –ї–Є–Љ—Д–Њ–Љ–∞, –≥–µ–њ–∞—В–Њ—Ж–µ–ї–ї—О–ї—П—А–љ—Л–є —А–∞–Ї, –∞–і–µ–љ–Њ–Љ–∞, –≥–µ–Љ–∞–љ–≥–Є–Њ–Љ–∞, –∞–±—Б—Ж–µ—Б—Б, –≥–µ–Љ–∞—В–Њ–Љ–∞ –Є –і—А.).
-
–Ю—З–∞–≥–Є —Б —Г—Б–Є–ї–µ–љ–љ–Њ–є —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А–Њ–є (–Љ–µ—В–∞—Б—В–∞–Ј—Л –≤—Л—Б–Њ–Ї–Њ–і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —А–∞–Ї–∞, –≥–µ–њ–∞—В–Њ–Љ–∞, –∞–і–µ–љ–Њ–Љ–∞, –≥–µ–Љ–∞–љ–≥–Є–Њ–Љ–∞, —А—Г–±—Ж—Л, –Њ—З–∞–≥–Є –Њ–±—Л–Ј–≤–µ—Б—В–≤–ї–µ–љ–Є—П) (—А–Є—Б.¬†5вАУ8).
-
–°–Є–Љ–њ—В–Њ–Љ ¬Ђ–Љ–Є—И–µ–љ–Є¬ї вАФ —Б–љ–Є–ґ–µ–љ–Є–µ —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А—Л –њ–Њ –њ–µ—А–Є—Д–µ—А–Є–Є –Њ—З–∞–≥–∞ –Є —Г—Б–Є–ї–µ–љ–Є–µ –µ–µ –≤ —Ж–µ–љ—В—А–µ (–Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ–∞—П –Њ–њ—Г—Е–Њ–ї—М –њ–µ—З–µ–љ–Є).

–†–Є—Б. 5. –≠—Е–Њ–≥—А–∞–Љ–Љ–∞ –њ–µ—З–µ–љ–Є —Г –±–Њ–ї—М–љ–Њ–≥–Њ —Б —А–∞–Ї–Њ–Љ –њ–µ—З–µ–љ–Є

–†–Є—Б. 6. –У–µ–Љ–∞–љ–≥–Є–Њ–Љ–∞ –њ–µ—З–µ–љ–Є

–†–Є—Б. 7. –≠—Е–Њ–≥—А–∞–Љ–Љ–∞ –њ–µ—З–µ–љ–Є —Г –±–Њ–ї—М–љ–Њ–≥–Њ —Б –≥–µ–њ–∞—В–Њ–Љ–Њ–є

–†–Є—Б. 8. –≠—Е–Њ–≥—А–∞–Љ–Љ–∞ –±–Њ–ї—М–љ–Њ–≥–Њ —Б –Љ–µ—В–∞—Б—В–∞—В–Є—З–µ—Б–Ї–Є–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –њ–µ—З–µ–љ–Є
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ–Њ—Б—В—М —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–µ—З–µ–љ–Є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –≤—Л—Б–Њ–Ї–∞, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –Њ—З–∞–≥–Њ–≤—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є—П—Е –Њ—А–≥–∞–љ–∞. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ —Б–ї–µ–і—Г–µ—В —Г—З–Є—В—Л–≤–∞—В—М –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–µ –ї–Њ–ґ–љ–Њ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ –Є –ї–Њ–ґ–љ–Њ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ –Ј–∞–Ї–ї—О—З–µ–љ–Є—П. –Я–Њ—Н—В–Њ–Љ—Г –њ—А–Є –∞–љ–∞–ї–Є–Ј–µ –Є –Є–љ—В–µ—А–њ—А–µ—В–∞—Ж–Є–Є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—З–Є—В—Л–≤–∞—В—М –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –Ї–∞—А—В–Є–љ—Г –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≤ —Ж–µ–ї–Њ–Љ, –∞ —В–∞–Ї–ґ–µ –і–∞–љ–љ—Л–µ –і—А—Г–≥–Є—Е –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –Є –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П.
–Т–∞–ґ–љ–Њ –Ј–љ–∞—В—М:
- –Э–Њ—А–Љ–∞–ї—М–љ–∞—П —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–∞—П –Ї–∞—А—В–Є–љ–∞, –≤ —В–Њ–Љ —З–Є—Б–ї–µ —Б–∞–≥–Є—В—В–∞–ї—М–љ—Л–µ —А–∞–Ј–Љ–µ—А—Л –њ–µ—З–µ–љ–Є –њ–Њ —Б—А–µ–і–Є–љ–љ–Њ-–Ї–ї—О—З–Є—З–љ–Њ–є –ї–Є–љ–Є–Є, –љ–µ –њ—А–µ–≤—Л—И–∞—О—Й–Є–µ 12вАУ15 —Б–Љ, –љ–µ –Є—Б–Ї–ї—О—З–∞–µ—В –љ–∞–ї–Є—З–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Н—В–Њ–≥–Њ –Њ—А–≥–∞–љ–∞.
- –Ф–Є—Д—Д—Г–Ј–љ—Л–µ –Є–ї–Є –Њ—З–∞–≥–Њ–≤—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А—Л –њ–µ—З–µ–љ–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –≤ –њ–Њ–ї—М–Ј—Г –µ–µ –њ–∞—В–Њ–ї–Њ–≥–Є–Є.
- –Я–Њ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є –Ї–∞—А—В–Є–љ–µ –љ–µ–ї—М–Ј—П –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞—В—М —А–∞–Ј–ї–Є—З–љ—Л–µ —Д–Њ—А–Љ—Л –≥–µ–њ–∞—В–Є—В–∞, –љ–∞—З–∞–ї—М–љ—Л–µ —Б—В–∞–і–Є–Є –ґ–Є—А–Њ–≤–Њ–є –і–Є—Б—В—А–Њ—Д–Є–Є –Є —Ж–Є—А—А–Њ–Ј–∞ –њ–µ—З–µ–љ–Є.
- –Я—А–Є –і–Є—Д—Д—Г–Ј–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є—П—Е –њ–µ—З–µ–љ–Є –Њ–Ї–Њ–љ—З–∞—В–µ–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј —Б–ї–µ–і—Г–µ—В –≤–µ—А–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є (—Б–Љ. –љ–Є–ґ–µ).
- –Ф–ї—П —Г—В–Њ—З–љ–µ–љ–Є—П –і–Є–∞–≥–љ–Њ–Ј–∞ –њ—А–Є –Њ—З–∞–≥–Њ–≤—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є—П—Е –≤ –њ–µ—З–µ–љ–Є –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –њ—А–Є—Ж–µ–ї—М–љ–Њ–є –±–Є–Њ–њ—Б–Є–Є –њ–Њ–і —Н—Е–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–Љ –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –і–ї—П –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–≥–Њ —Ж–Є—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞.
–Ц–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М –Є –ґ–µ–ї—З–љ—Л–µ –њ—А–Њ—В–Њ–Ї–Є
–£–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Є –ґ–µ–ї—З–љ—Л—Е –њ—А–Њ—В–Њ–Ї–Њ–≤ –Є–Љ–µ–µ—В –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –њ–µ—А–µ–і —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ (—Е–Њ–ї–µ—Ж–Є—Б—В–Њ–≥—А–∞—Д–Є–µ–є, –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–є —Е–Њ–ї–µ–≥—А–∞—Д–Є–µ–є –Є –і—А.), —В–∞–Ї –Ї–∞–Ї –њ–Њ–ї–љ–Њ—Б—В—М—О –Є—Б–Ї–ї—О—З–∞–µ—В –ї—Г—З–µ–≤—Г—О –љ–∞–≥—А—Г–Ј–Ї—Г –љ–∞ –њ–∞—Ж–Є–µ–љ—В–∞, –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ—А–Њ–≤–Њ–і–Є—В—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Г –і–µ—В–µ–є –Є –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ, –∞ —В–∞–Ї–ґ–µ –њ—А–Є —Б–љ–Є–ґ–µ–љ–Є–Є —Д—Г–љ–Ї—Ж–Є–Є –њ–µ—З–µ–љ–Є –Є –њ–Њ—З–µ–Ї.
–Э–∞–Є–±–Њ–ї–µ–µ –Њ–±—Й–Є–Љ–Є –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ–Є –Ї –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—О –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Є –ґ–µ–ї—З–љ—Л—Е –њ—А–Њ—В–Њ–Ї–Њ–≤ —П–≤–ї—П—О—В—Б—П:
-
–Њ—Б—В—А—Л–є –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є —Е–Њ–ї–µ—Ж–Є—Б—В–Є—В;
-
–ґ–µ–ї—З–љ–Њ–Ї–∞–Љ–µ–љ–љ–∞—П –±–Њ–ї–µ–Ј–љ—М;
-
–ґ–µ–ї—В—Г—Е–∞;
-
–Њ–њ—Г—Е–Њ–ї—М;
-
–≤–Њ–і—П–љ–Ї–∞ –Є —Н–Љ–њ–Є–µ–Љ–∞ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П;
-
—Б–Њ—Б—В–Њ—П–љ–Є–µ –њ–Њ—Б–ї–µ —Е–Њ–ї–µ—Ж–Є—Б—В—Н–Ї—В–Њ–Љ–Є–Є –Є–ї–Є –і—А—Г–≥–Є—Е –Њ–њ–µ—А–∞—Ж–Є–є –љ–∞ –ґ–µ–ї—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В—П—Е.
–Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Њ—Ж–µ–љ–Є–≤–∞—О—В –µ–≥–Њ –њ–Њ–ї–Њ–ґ–µ–љ–Є–µ, —Д–Њ—А–Љ—Г, –≤–µ–ї–Є—З–Є–љ—Г, –і—Л—Е–∞—В–µ–ї—М–љ—Г—О –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В—М, —Б–Њ—Б—В–Њ—П–љ–Є–µ –љ–∞—А—Г–ґ–љ—Л—Е –Є –≤–љ—Г—В—А–µ–љ–љ–Є—Е –Ї–Њ–љ—В—Г—А–Њ–≤, —В–Њ–ї—Й–Є–љ—Г —Б—В–µ–љ–Њ–Ї, —Б—В—А—Г–Ї—В—Г—А—Г —Б—В–µ–љ–Ї–Є, –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –њ–Њ–ї–Њ—Б—В–Є –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П, —Н–≤–∞–Ї—Г–∞—В–Њ—А–љ—Г—О —Д—Г–љ–Ї—Ж–Є—О –Њ—А–≥–∞–љ–∞.
–Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤–љ–µ–њ–µ—З–µ–љ–Њ—З–љ—Л—Е –ґ–µ–ї—З–љ—Л—Е –њ—А–Њ—В–Њ–Ї–Њ–≤ –Њ–њ—А–µ–і–µ–ї—П—О—В –Є—Е –њ–Њ–ї–Њ–ґ–µ–љ–Є–µ, –і–Є–∞–Љ–µ—В—А, —Б–Њ—Б—В–Њ—П–љ–Є–µ —Б—В–µ–љ–Њ–Ї, –љ–∞–ї–Є—З–Є–µ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –≤–Ї–ї—О—З–µ–љ–Є–є –≤ –њ—А–Њ—Б–≤–µ—В–µ.
–Т –љ–Њ—А–Љ–µ –ґ–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М –≤—Л—П–≤–ї—П–µ—В—Б—П –Ї–∞–Ї —Н—Е–Њ–љ–µ–≥–∞—В–Є–≤–љ–∞—П —Б—В—А—Г–Ї—В—Г—А–∞ –љ–∞ –і–Њ—А–Ј–∞–ї—М–љ–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –њ—А–∞–≤–Њ–є –і–Њ–ї–Є –њ–µ—З–µ–љ–Є. –Ф–љ–Њ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П —З–∞—Б—В–Њ –≤—Л—Б—В—Г–њ–∞–µ—В –Є–Ј-–њ–Њ–і –љ–Є–ґ–љ–µ–≥–Њ –Ї—А–∞—П –њ–µ—З–µ–љ–Є –љ–∞ 1,0вАУ1,5 —Б–Љ. –Х–≥–Њ –і–ї–Є–љ–∞ –љ–µ –њ—А–µ–≤—Л—И–∞–µ—В 7вАУ10 —Б–Љ, –∞ —И–Є—А–Є–љ–∞ 3вАУ4 —Б–Љ. –Ц–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М –Є–Љ–µ–µ—В —Г–і–ї–Є–љ–µ–љ–љ—Г—О –≥—А—Г—И–µ–≤–Є–і–љ—Г—О, –Њ–≤–∞–ї—М–љ—Г—О –Є–ї–Є –Њ–Ї—А—Г–≥–ї—Г—О —Д–Њ—А–Љ—Г, —З–µ—В–Ї–Є–є –Є —А–Њ–≤–љ—Л–є –Ї–Њ–љ—В—Г—А.
–Т–љ—Г—В—А–Є–њ–µ—З–µ–љ–Њ—З–љ—Л–µ –ґ–µ–ї—З–љ—Л–µ –њ—А–Њ—В–Њ–Ї–Є —Г –Ј–і–Њ—А–Њ–≤–Њ–≥–Њ —З–µ–ї–Њ–≤–µ–Ї–∞ –љ–µ –≤—Л—П–≤–ї—П—О—В—Б—П. –Ф–Є–∞–Љ–µ—В—А –Њ–±—Й–µ–≥–Њ –њ–µ—З–µ–љ–Њ—З–љ–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–∞ –љ–µ –њ—А–µ–≤—Л—И–∞–µ—В 3вАУ5 –Љ–Љ, –∞ –Њ–±—Й–µ–≥–Њ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–∞ вАФ 4вАУ6 –Љ–Љ (—А–Є—Б.¬†9).

–†–Є—Б. 9. –Э–Њ—А–Љ–∞–ї—М–љ–∞—П —Н—Е–Њ–≥—А–∞–Љ–Љ–∞ –њ–µ—З–µ–љ–Є.
–Т —Ж–µ–љ—В—А–µ –Ј–∞–Љ–µ—В–љ—Л –Њ–±—Й–Є–є –ґ–µ–ї—З–љ—Л–є –њ—А–Њ—В–Њ–Ї –Є –њ–Њ–і –љ–Є–Љ –≤–Њ—А–Њ—В–љ–∞—П –≤–µ–љ–∞ (–њ—А–Њ–і–Њ–ї—М–љ—Л–є —Б—А–µ–Ј)
–Ю—Б—В—А—Л–є —Е–Њ–ї–µ—Ж–Є—Б—В–Є—В. –•–∞—А–∞–Ї—В–µ—А–љ—Л–Љ–Є —Н—Е–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є –Њ—Б—В—А–Њ–≥–Њ —Е–Њ–ї–µ—Ж–Є—Б—В–Є—В–∞ —П–≤–ї—П–µ—В—Б—П —Г—В–Њ–ї—Й–µ–љ–Є–µ —Б—В–µ–љ–Ї–Є –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –±–Њ–ї–µ–µ 4 –Љ–Љ. –Х–≥–Њ —А–∞–Ј–Љ–µ—А—Л –Љ–Њ–≥—Г—В –Њ—Б—В–∞–≤–∞—В—М—Б—П –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ–Є –Є–ї–Є –і–∞–ґ–µ —Г–Љ–µ–љ—М—И–µ–љ—Л, —Е–Њ—В—П —З–∞—Й–µ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –љ–µ–±–Њ–ї—М—И–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П.
–≠—Е–Њ—Б—В—А—Г–Ї—В—Г—А–∞ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –µ–≥–Њ –≤–љ—Г—В—А–µ–љ–љ–µ–≥–Њ –Ї–Њ–љ—В—Г—А–∞, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, —Б–љ–Є–ґ–µ–љ–∞. –Я—А–Є —Д–ї–µ–≥–Љ–Њ–љ–Њ–Ј–љ–Њ–Љ —Е–Њ–ї–µ—Ж–Є—Б—В–Є—В–µ –≤–љ—Г—В—А–µ–љ–љ–Є–µ –Є –љ–∞—А—Г–ґ–љ—Л–µ –Ї–Њ–љ—В—Г—А—Л –њ—Г–Ј—Л—А—П –љ–µ—З–µ—В–Ї–Є–µ. –Я—А–Є –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–Є –њ–µ—А–Є—Е–Њ–ї–µ—Ж–Є—Б—В–Є—В–∞ —Б—В–µ–љ–Ї–∞ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Є–Љ–µ–µ—В –і–≤–Њ–є–љ–Њ–є –Ї–Њ–љ—В—Г—А —Б —Г—Б–Є–ї–µ–љ–Є–µ–Љ —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А—Л –љ–∞—А—Г–ґ–љ–Њ–≥–Њ –Є —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А—Л –≤–љ—Г—В—А–µ–љ–љ–µ–≥–Њ –Ї–Њ–љ—В—Г—А–∞. –Я–Њ—П–≤–ї–µ–љ–Є–µ –њ–Њ–ї–Њ—Б–Ї–Є –ґ–Є–і–Ї–Њ—Б—В–Є –≤–Њ–Ї—А—Г–≥ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П —Г–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞ –љ–∞–ї–Є—З–Є–µ –ї–Њ–Ї–∞–ї—М–љ–Њ–≥–Њ –њ–µ—А–Є—В–Њ–љ–Є—В–∞.
–•—А–Њ–љ–Є—З–µ—Б–Ї–Є–є (–±–µ—Б–Ї–∞–Љ–µ–љ–љ—Л–є) —Е–Њ–ї–µ—Ж–Є—Б—В–Є—В. –Т –њ–µ—А–Є–Њ–і —А–µ–Љ–Є—Б—Б–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Е–Њ–ї–µ—Ж–Є—Б—В–Є—В–∞ —А–∞–Ј–Љ–µ—А—Л –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П —Г–Љ–µ–љ—М—И–µ–љ—Л –Є–ї–Є –љ–Њ—А–Љ–∞–ї—М–љ—Л–µ. –Э–∞–Є–±–Њ–ї–µ–µ –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ–Є –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є —П–≤–ї—П—О—В—Б—П —Г—В–Њ–ї—Й–µ–љ–Є–µ —Б—В–µ–љ–Ї–Є –њ—Г–Ј—Л—А—П –њ—А–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ –µ–µ —Г–њ–ї–Њ—В–љ–µ–љ–Є–Є (—Г—Б–Є–ї–µ–љ–Є–µ —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А—Л) –Є –љ–∞–ї–Є—З–Є–µ —З–µ—В–Ї–Є—Е –Ї–Њ–љ—В—Г—А–Њ–≤. –≠—В–Њ –Њ—В–ї–Є—З–∞–µ—В —Н—Е–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї—Г—О –Ї–∞—А—В–Є–љ—Г –Њ—В —В–∞–Ї–Њ–≤–Њ–є –њ—А–Є –Њ—Б—В—А–Њ–Љ —Е–Њ–ї–µ—Ж–Є—Б—В–Є—В–µ.
–Э–µ—А–µ–і–Ї–Њ –Є–Ј–Љ–µ–љ—П–µ—В—Б—П —Д–Њ—А–Љ–∞ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П: –њ–Њ—П–≤–ї—П—О—В—Б—П –Є–Ј–≥–Є–±—Л, –≤—В—П–ґ–µ–љ–Є—П —Б—В–µ–љ–Њ–Ї –Є –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–∞—П –і–µ—Д–Њ—А–Љ–∞—Ж–Є—П –µ–≥–Њ —Б—В–µ–љ–Њ–Ї (—А–Є—Б.¬†10).

–†–Є—Б. 10. –Ф–µ—Д–Њ—А–Љ–∞—Ж–Є—П –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П
–Т —В–Њ –ґ–µ –≤—А–µ–Љ—П —Б–ї–µ–і—Г–µ—В –њ–Њ–Љ–љ–Є—В—М, —З—В–Њ –і–Є–∞–≥–љ–Њ–Ј —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Е–Њ–ї–µ—Ж–Є—Б—В–Є—В–∞ –љ–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –њ–Њ—Б—В–∞–≤–ї–µ–љ —В–Њ–ї—М–Ї–Њ –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ.
–Ц–µ–ї—З–љ–Њ–Ї–∞–Љ–µ–љ–љ–∞—П –±–Њ–ї–µ–Ј–љ—М. –Я—А–Њ–±–ї–µ–Љ–∞ –ґ–µ–ї—З–љ–Њ–Ї–∞–Љ–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є (—Е–Њ–ї–µ–ї–Є—В–Є–∞–Ј–∞) –Ј–∞–љ–Є–Љ–∞–µ—В –≤–µ–і—Г—Й–µ–µ –Љ–µ—Б—В–Њ –≤ –њ–∞—В–Њ–ї–Њ–≥–Є–Є –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П. –£–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л–µ –њ—А–Є–Ј–љ–∞–Ї–Є –Ї–∞–ї—М–Ї—Г–ї–µ–Ј–∞ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –і–µ–ї—П—В—Б—П –љ–∞ –њ—А—П–Љ—Л–µ –Є –Ї–Њ—Б–≤–µ–љ–љ—Л–µ. –Ъ –њ—А—П–Љ—Л–Љ –њ—А–Є–Ј–љ–∞–Ї–∞–Љ –Њ—В–љ–Њ—Б—П—В –љ–∞–ї–Є—З–Є–µ –≤ –њ—А–Њ—Б–≤–µ—В–µ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –љ–∞ —Д–Њ–љ–µ —Н—Е–Њ–љ–µ–≥–∞—В–Є–≤–љ–Њ–є —Б—В—А—Г–Ї—В—Г—А—Л –ґ–µ–ї—З–Є —Г—Б–Є–ї–µ–љ–љ–Њ–≥–Њ —Н—Е–Њ—Б–Є–≥–љ–∞–ї–∞, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–≥–Њ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–Є—О –Ї–∞–Љ–љ—П (—А–Є—Б.¬†11). –†–∞–Ј–Љ–µ—А —Б–Є–≥–љ–∞–ї–∞ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Љ–µ–љ—М—И–µ –Є—Б—В–Є–љ–љ–Њ–≥–Њ —А–∞–Ј–Љ–µ—А–∞ –Ї–∞–Љ–љ—П. –Я—А–Є –Њ—Б–Љ–Њ—В—А–µ –±–Њ–ї—М–љ–Њ–≥–Њ –≤ –≥–Њ—А–Є–Ј–Њ–љ—В–∞–ї—М–љ–Њ–Љ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є –Ї–∞–Љ–љ–Є —А–∞—Б–њ–Њ–ї–∞–≥–∞—О—В—Б—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–∞ –і–Њ—А–Ј–∞–ї—М–љ–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Є –≤ —И–µ–є–Ї–µ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П.

–†–Є—Б. 11. –Ь–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л–µ –Ї–∞–Љ–љ–Є –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П.
–•–Њ—А–Њ—И–Њ –Ј–∞–Љ–µ—В–љ–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л—Е —А–∞–Ј–Љ–µ—А–Њ–≤ —Б–њ–ї–Њ—И–љ–∞—П –∞–Ї—Г—Б—В–Є—З–µ—Б–Ї–∞—П —В–µ–љ—М
–Т–∞–ґ–љ—Л–Љ –њ—А–Є–Ј–љ–∞–Ї–Њ–Љ –Ї–∞–ї—М–Ї—Г–ї–µ–Ј–∞ —П–≤–ї—П–µ—В—Б—П —Б–Љ–µ—Й–µ–љ–Є–µ –Ї–∞–Љ–љ–µ–є –њ—А–Є –њ–µ—А–µ–Љ–µ–љ–µ –њ–Њ–ї–Њ–ґ–µ–љ–Є—П —В–µ–ї–∞. –Т –≤–µ—А—В–Є–Ї–∞–ї—М–љ–Њ–Љ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є –Ї–∞–Љ–љ–Є ¬Ђ—Б–Ї–∞—В—Л–≤–∞—О—В—Б—П¬ї –љ–∞ –і–љ–Њ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П. –≠—Е–Њ—Б—В—А—Г–Ї—В—Г—А–∞, –Є–і—Г—Й–∞—П –Њ—В –Ї–Њ–љ–Ї—А–µ–Љ–µ–љ—В–∞, —А–∞–Ј–Љ–µ—А –Ї–Њ—В–Њ—А–Њ–≥–Њ –њ—А–µ–≤—Л—И–∞–µ—В 4 –Љ–Љ, –≤—Б–µ–≥–і–∞ –Њ–±—А–∞–Ј—Г–µ—В –њ–Њ—Б–ї–µ —Б–µ–±—П —В–µ–љ–µ–≤—Г—О –і–Њ—А–Њ–ґ–Ї—Г вАФ –∞–Ї—Г—Б—В–Є—З–µ—Б–Ї—Г—О —В–µ–љ—М, –≤–Њ–Ј–љ–Є–Ї–∞—О—Й—Г—О –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ–Њ–≥–ї–Њ—Й–µ–љ–Є—П –Ї–∞–Љ–љ–µ–Љ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л—Е –≤–Њ–ї–љ.
–Ю–і–љ–Є–Љ –Є–Ј –Ї–Њ—Б–≤–µ–љ–љ—Л—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –Ї–∞–ї—М–Ї—Г–ї–µ–Ј–∞ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П —П–≤–ї—П–µ—В—Б—П —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –µ–≥–Њ —А–∞–Ј–Љ–µ—А–Њ–≤ –±–Њ–ї–µ–µ 5 —Б–Љ –≤ –њ–Њ–њ–µ—А–µ—З–љ–Є–Ї–µ –Є –і–Њ 10 —Б–Љ –Є –±–Њ–ї–µ–µ –≤ –і–ї–Є–љ—Г, –∞ —В–∞–Ї–ґ–µ —Г—В–Њ–ї—Й–µ–љ–Є–µ –µ–≥–Њ —Б—В–µ–љ–Ї–Є –Є –љ–µ—А–Њ–≤–љ–Њ—Б—В—М –Ї–Њ–љ—В—Г—А–∞.
–≠—Е–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–∞—П –Ї–∞—А—В–Є–љ–∞ –њ—А–Є –љ–∞–ї–Є—З–Є–Є –Ї–∞–Љ–љ–µ–є –≤–Њ –≤–љ–µ–њ–µ—З–µ–љ–Њ—З–љ—Л—Е –ґ–µ–ї—З–љ—Л—Е –њ—А–Њ—В–Њ–Ї–∞—Е –љ–∞–њ–Њ–Љ–Є–љ–∞–µ—В —В–∞–Ї–Њ–≤—Г—О –њ—А–Є –Ї–∞–ї—М–Ї—Г–ї–µ–Ј–µ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П. –Ъ–∞–Љ–љ–Є —А–∞–Ј–Љ–µ—А–Њ–Љ –±–Њ–ї–µ–µ 3вАУ4 –Љ–Љ –≤ –і–Є–∞–Љ–µ—В—А–µ –і–∞—О—В —Г—Б–Є–ї–µ–љ–љ—Л–є —Н—Е–Њ—Б–Є–≥–љ–∞–ї. –Х—Б–ї–Є –і–Є–∞–Љ–µ—В—А –Ї–∞–Љ–љ—П –њ—А–µ–≤—Л—И–∞–µ—В 5 –Љ–Љ, –Ј–∞ –µ–≥–Њ –і–Њ—А–Ј–∞–ї—М–љ–Њ–є —Б—В–µ–љ–Ї–Њ–є –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –∞–Ї—Г—Б—В–Є—З–µ—Б–Ї–∞—П —В–µ–љ—М.
–Ъ–∞–Љ–љ–Є –љ–µ–±–Њ–ї—М—И–Є—Е —А–∞–Ј–Љ–µ—А–Њ–≤ –њ—А–Є —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Њ–±—Л—З–љ–Њ –љ–µ –≤—Л—П–≤–ї—П—О—В—Б—П. –Т —Н—В–Є—Е —Б–ї—Г—З–∞—П—Е –Ї–Њ—Б–≤–µ–љ–љ—Л–Љ –њ—А–Є–Ј–љ–∞–Ї–Њ–Љ –Ї–∞–ї—М–Ї—Г–ї–µ–Ј–∞ —П–≤–ї—П–µ—В—Б—П —А–∞—Б—И–Є—А–µ–љ–Є–µ –њ—А–Њ—В–Њ–Ї–∞ –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ–µ–µ –Љ–µ—Б—В–∞ –µ–≥–Њ –Њ–±—В—Г—А–∞—Ж–Є–Є.
–Ф–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Њ–є –Є –њ–∞—А–µ–љ—Е–Є–Љ–∞—В–Њ–Ј–љ–Њ–є –ґ–µ–ї—В—Г—Е. –≠—Е–Њ–ї–Њ–Ї–∞—Ж–Є—П –Њ–Ї–∞–Ј–∞–ї–∞—Б—М –Њ–і–љ–Њ–є –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ—Л—Е –Є —Ж–µ–љ–љ—Л—Е –Љ–µ—В–Њ–і–Є–Ї –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Њ–±—В—Г—А–∞—Ж–Є–Њ–љ–љ–Њ–є –Є –њ–∞—А–µ–љ—Е–Є–Љ–∞—В–Њ–Ј–љ–Њ–є –ґ–µ–ї—В—Г—Е. –Я—А–Є —Н—В–Њ–Љ —Б–ї–µ–і—Г–µ—В –Є–Љ–µ—В—М –≤ –≤–Є–і—Г, —З—В–Њ –Њ–і–љ–Є–Љ –Є–Ј –Њ—Б–љ–Њ–≤–љ—Л—Е —Н—Е–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Њ–є –ґ–µ–ї—В—Г—Е–Є —П–≤–ї—П–µ—В—Б—П —А–∞—Б—И–Є—А–µ–љ–Є–µ –ґ–µ–ї—З–љ—Л—Е –њ—Г—В–µ–є.
–Ф–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј —Б—В—А–Њ–Є—В—Б—П –љ–∞ —Б–ї–µ–і—Г—О—Й–Є—Е –њ—А–Є–љ—Ж–Є–њ–∞—Е.
-
–Х—Б–ї–Є –≤–љ—Г—В—А–Є–њ–µ—З–µ–љ–Њ—З–љ—Л–µ –Є –≤–љ–µ–њ–µ—З–µ–љ–Њ—З–љ—Л–µ –њ—А–Њ—В–Њ–Ї–Є –љ–µ —А–∞—Б—И–Є—А–µ–љ—Л, –∞ —А–∞–Ј–Љ–µ—А—Л –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –љ–µ —Г–≤–µ–ї–Є—З–µ–љ—Л, –Њ–±—В—Г—А–∞—Ж–Є–Њ–љ–љ–∞—П –њ—А–Є—З–Є–љ–∞ –ґ–µ–ї—В—Г—Е–Є –≤—Л–Ј—Л–≤–∞–µ—В —Б–Њ–Љ–љ–µ–љ–Є—П. –Т —Н—В–Є—Е —Б–ї—Г—З–∞—П—Е –Њ–љ–∞, —Б–Ї–Њ—А–µ–µ –≤—Б–µ–≥–Њ, —П–≤–ї—П–µ—В—Б—П —Б–ї–µ–і—Б—В–≤–Є–µ–Љ –і–Є—Д—Д—Г–Ј–љ—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є –њ–µ—З–µ–љ–Є (–≥–µ–њ–∞—В–Є—В, —Ж–Є—А—А–Њ–Ј –њ–µ—З–µ–љ–Є –Є –і—А.).
-
–Х—Б–ї–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —А–∞—Б—И–Є—А–µ–љ—Л –≤–љ—Г—В—А–Є–њ–µ—З–µ–љ–Њ—З–љ—Л–µ –њ—А–Њ—В–Њ–Ї–Є, –∞ –ґ–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М –Є –≤–љ–µ–њ–µ—З–µ–љ–Њ—З–љ—Л–µ –њ—А–Њ—В–Њ–Ї–Є –Є–Љ–µ—О—В –љ–Њ—А–Љ–∞–ї—М–љ—Л–µ —А–∞–Ј–Љ–µ—А—Л, –њ—А–Є—З–Є–љ—Г –ґ–µ–ї—В—Г—Е–Є —Б–ї–µ–і—Г–µ—В —Г—Б–Љ–∞—В—А–Є–≤–∞—В—М –≤ –≤—Л—Б–Њ–Ї–Њ–є –Њ–±—В—Г—А–∞—Ж–Є–Є, –љ–∞–њ—А–Є–Љ–µ—А –љ–∞ —Г—А–Њ–≤–љ–µ –Њ–±—Й–µ–≥–Њ –њ–µ—З–µ–љ–Њ—З–љ–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–∞.
-
–Х—Б–ї–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–≤–µ–ї–Є—З–µ–љ—Л —А–∞–Ј–Љ–µ—А—Л –≤–љ–µ- –Є –≤–љ—Г—В—А–Є–њ–µ—З–µ–љ–Њ—З–љ—Л—Е –ґ–µ–ї—З–љ—Л—Е –њ—А–Њ—В–Њ–Ї–Њ–≤, –∞ —В–∞–Ї–ґ–µ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П, –Є —Н—В–Є —А–∞–Ј–Љ–µ—А—Л –љ–µ –Є–Ј–Љ–µ–љ—П—О—В—Б—П –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –ґ–µ–ї—З–µ–≥–Њ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤, –љ–∞–Є–±–Њ–ї–µ–µ –≤–µ—А–Њ—П—В–љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є –ґ–µ–ї—В—Г—Е–Є —П–≤–ї—П–µ—В—Б—П –Њ–±—В—Г—А–∞—Ж–Є—П –і–Є—Б—В–∞–ї—М–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –Њ–±—Й–µ–≥–Њ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–∞ (¬Ђ–≤–Ї–Њ–ї–Њ—З–µ–љ–љ—Л–є¬ї –Ї–∞–Љ–µ–љ—М, —А–∞–Ї —Б—Д–Є–љ–Ї—В–µ—А–∞ –Ю–і–і–Є, –Ї–∞—А—Ж–Є–љ–Њ–Љ–∞ –≥–Њ–ї–Њ–≤–Ї–Є –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –Є —В.¬†–і.). –Я—А–Є —Н—В–Њ–Љ —Б–ї–µ–і—Г–µ—В –Є–Љ–µ—В—М –≤ –≤–Є–і—Г, —З—В–Њ —Б–і–∞–≤–ї–µ–љ–Є–µ –Њ–±—Й–µ–≥–Њ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–∞ –њ—А–Є –Њ–њ—Г—Е–Њ–ї–Є –≥–Њ–ї–Њ–≤–Ї–Є –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –љ–µ—А–µ–і–Ї–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —Б–Є–Љ–њ—В–Њ–Љ–Њ–Љ –Ъ—Г—А–≤—Г–∞–Ј—М–µ (—Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —А–∞–Ј–Љ–µ—А–Њ–≤ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –љ–∞ —Д–Њ–љ–µ –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Њ–є –ґ–µ–ї—В—Г—Е–Є). –Я—А–Є –љ–∞–ї–Є—З–Є–Є –Ї–∞–Љ–љ—П –≤ –Њ–±—Й–µ–Љ –ґ–µ–ї—З–љ–Њ–Љ –њ—А–Њ—В–Њ–Ї–µ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П —А–∞—Б—И–Є—А–µ–љ–Є–µ –њ—А–Њ—В–Њ–Ї–Њ–≤, –љ–Њ –ґ–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М —З–∞—Й–µ –љ–µ —Г–≤–µ–ї–Є—З–µ–љ.
–£–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л
–≠—Е–Њ–≥—А–∞—Д–Є—П –і–∞–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А–Њ–≤–∞—В—М –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ—Г—О –ґ–µ–ї–µ–Ј—Г –≤ —А–∞–Ј–љ—Л—Е –њ—А–Њ–µ–Ї—Ж–Є—П—Е –Є –Њ—Ж–µ–љ–Є—В—М –µ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ –≤ –і–Є–љ–∞–Љ–Є–Ї–µ —А–∞–Ј–≤–Є—В–Є—П –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞, —Е–Њ—В—П –≤ —Б–≤—П–Ј–Є —Б –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П–Љ–Є –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В—А–Њ–µ–љ–Є—П –Є —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–Є—П –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б–Њ–њ—А—П–ґ–µ–љ–Њ —Б –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–Љ–Є —В—А—Г–і–љ–Њ—Б—В—П–Љ–Є.
–Я–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ–Є –і–ї—П —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л —П–≤–ї—П—О—В—Б—П:
-
–ї—О–±—Л–µ —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–Є–µ –Є–ї–Є –і–ї–Є—В–µ–ї—М–љ–Њ —Б–Њ—Е—А–∞–љ—П—О—Й–Є–µ—Б—П –±–Њ–ї–Є –≤ —Н–њ–Є–≥–∞—Б—В—А–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є;
-
–њ–∞–ї—М–њ–Є—А—Г–µ–Љ–Њ–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –≤ —Н–њ–Є–≥–∞—Б—В—А–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є –Є–ї–Є –±–Њ–ї–µ–Ј–љ–µ–љ–љ–Њ—Б—В—М –њ—А–Є –њ–∞–ї—М–њ–∞—Ж–Є–Є;
-
–≤–µ—А–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–є –Њ—Б—В—А—Л–є –Є–ї–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –њ–∞–љ–Ї—А–µ–∞—В–Є—В —Б —Ж–µ–ї—М—О —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ –≤—Л—П–≤–ї–µ–љ–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є (–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –Ї–Є—Б—В, –∞–±—Б—Ж–µ—Б—Б–∞, –љ–µ–Ї—А–Њ–Ј–∞);
-
–њ–Њ–і–Њ–Ј—А–µ–љ–Є–µ –љ–∞ –Ї–Є—Б—В—Г, –∞–±—Б—Ж–µ—Б—Б, –≥–µ–Љ–∞—В–Њ–Љ—Г, —А–∞–Ї –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л;
-
–і–µ—Д–Њ—А–Љ–∞—Ж–Є—П –Ј–∞–і–љ–µ–є —Б—В–µ–љ–Ї–Є –ґ–µ–ї—Г–і–Ї–∞ –њ—А–Є –≥–∞—Б—В—А–Њ—Б–Ї–Њ–њ–Є–Є;
-
–Є–Ј–Љ–µ–љ–µ–љ–Є–µ —Д–Њ—А–Љ—Л –Є –Ї–Њ–љ—В—Г—А–Њ–≤ –њ–µ—В–ї–Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є –њ—А–Є —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є.
–£–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –љ–∞—З–Є–љ–∞—О—В –≤ –≥–Њ—А–Є–Ј–Њ–љ—В–∞–ї—М–љ–Њ–Љ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–∞ —Б–∞–≥–Є—В—В–∞–ї—М–љ—Л–Љ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ. –Ф–∞—В—З–Є–Ї —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—О—В –њ—А–Њ–і–Њ–ї—М–љ–Њ –≤ —Н–њ–Є–≥–∞—Б—В—А–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є —Б–ї–µ–≤–∞ –Њ—В —Б—А–µ–і–Є–љ–љ–Њ–є –ї–Є–љ–Є–Є.
–Ю—Б–Љ–Њ—В—А—Г –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –њ—А–µ–і—И–µ—Б—В–≤—Г–µ—В –≤—Л—П–≤–ї–µ–љ–Є–µ –Ї—А—Г–њ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є вАФ –∞–Њ—А—В—Л, –љ–Є–ґ–љ–µ–є –њ–Њ–ї–Њ–є –≤–µ–љ—Л, —Б–µ–ї–µ–Ј–µ–љ–Њ—З–љ–Њ–є –Є –≤–Њ—А–Њ—В–љ–Њ–є –≤–µ–љ, –≤–µ—А—Е–љ–µ–є –±—А—Л–ґ–µ–µ—З–љ–Њ–є –∞—А—В–µ—А–Є–є –Є –≤–µ–љ—Л, –Ї–Њ—В–Њ—А—Л–µ —Б–ї—Г–ґ–∞—В –Њ—А–Є–µ–љ—В–Є—А–∞–Љ–Є –і–ї—П –љ–∞—Е–Њ–ґ–і–µ–љ–Є—П –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л, –∞ —В–∞–Ї–ґ–µ —З—А–µ–≤–љ–Њ–≥–Њ —Б—В–≤–Њ–ї–∞. –Я—А–Є —Н—В–Њ–Љ –Њ–њ—А–µ–і–µ–ї—П—О—В –њ–Њ–ї–Њ–ґ–µ–љ–Є–µ —Б–Њ—Б—Г–і–Њ–≤, –Є—Е –і–Є–∞–Љ–µ—В—А, –љ–∞—А—Г–ґ–љ—Л–є –Є –≤–љ—Г—В—А–µ–љ–љ–Є–є –Ї–Њ–љ—В—Г—А—Л, –њ—Г–ї—М—Б–∞—Ж–Є—О, –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –і–Є–∞–Љ–µ—В—А–∞ –љ–∞ –≤–і–Њ—Е–µ –Є –љ–∞ –≤—Л–і–Њ—Е–µ, –љ–∞–ї–Є—З–Є–µ –≤–љ—Г—В—А–Є–њ—А–Њ—Б–≤–µ—В–љ—Л—Е –≤–Ї–ї—О—З–µ–љ–Є–є.
–Ґ–µ–ї–Њ –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –њ—А–Є–Љ—Л–Ї–∞–µ—В –Ї –і–Њ—А–Ј–∞–ї—М–љ–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –ї–µ–≤–Њ–є –і–Њ–ї–Є –њ–µ—З–µ–љ–Є, –∞ –≥–Њ–ї–Њ–≤–Ї–∞ вАФ –Ї –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–µ. –Ю—Б–Љ–Њ—В—А –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –њ—А–Њ–≤–Њ–і—П—В –љ–∞ –≤—Л—Б–Њ—В–µ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –≤–і–Њ—Е–∞, –Ї–Њ–≥–і–∞ –ї–µ–≤–∞—П –і–Њ–ї—П –њ–µ—З–µ–љ–Є –Њ–њ—Г—Б–Ї–∞–µ—В—Б—П –≤ –±—А—О—И–љ—Г—О –њ–Њ–ї–Њ—Б—В—М.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–і–Њ–ї–ґ–∞—О—В –њ—А–Є –њ–Њ–њ–µ—А–µ—З–љ–Њ–Љ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–Є–Є —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –і–∞—В—З–Є–Ї–∞, –Ї–Њ—В–Њ—А—Л–є –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ –њ–µ—А–µ–Љ–µ—Й–∞—О—В –Ї–љ–Є–Ј—Г –і–Њ –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є —Б–µ–ї–µ–Ј–µ–љ–Њ—З–љ–Њ–є –≤–µ–љ—Л. –Я—А–Є –њ–Њ–њ–µ—А–µ—З–љ–Њ–Љ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–Є –љ–µ—А–µ–і–Ї–Њ —Г–і–∞–µ—В—Б—П –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А–Њ–≤–∞—В—М –≤—Б—О –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ—Г—О –ґ–µ–ї–µ–Ј—Г. –Я—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і—П—В –Є –≤ –і—А—Г–≥–Є—Е –њ–Њ–Ј–Є—Ж–Є—П—Е: –њ—А–Є –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–∞ –љ–∞ –њ—А–∞–≤–Њ–Љ –Є –ї–µ–≤–Њ–Љ –±–Њ–Ї—Г, –≤ –≤–µ—А—В–Є–Ї–∞–ї—М–љ–Њ–Љ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є.
–Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –Є–Ј—Г—З–∞—О—В –µ–µ –њ–Њ–ї–Њ–ґ–µ–љ–Є–µ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ ¬Ђ—Б–Њ—Б—Г–і–Њ–≤-–Њ—А–Є–µ–љ—В–Є—А–Њ–≤¬ї –Є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Њ–≥–Њ —Б—В–Њ–ї–±–∞, –Њ–њ—А–µ–і–µ–ї—П—О—В —Д–Њ—А–Љ—Г, –Ї–Њ–љ—В—Г—А—Л –Є —А–∞–Ј–Љ–µ—А—Л –Њ—А–≥–∞–љ–∞, —Б–Њ—Б—В–Њ—П–љ–Є–µ –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–∞, —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А—Г –ґ–µ–ї–µ–Ј—Л, –≤—Л—П–≤–ї—П—О—В –љ–∞–ї–Є—З–Є–µ –≤ –љ–µ–є –Њ—З–∞–≥–Њ–≤—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є.
–Я–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–∞—П –ґ–µ–ї–µ–Ј–∞ —А–∞—Б–њ–Њ–ї–∞–≥–∞–µ—В—Б—П –Ј–∞–±—А—О—И–Є–љ–љ–Њ –њ–Њ–њ–µ—А–µ–Ї –Ј–∞–і–љ–µ–є –±—А—О—И–љ–Њ–є —Б—В–µ–љ–Ї–Є –љ–∞ —Г—А–Њ–≤–љ–µ I –Є II –њ–Њ—П—Б–љ–Є—З–љ—Л—Е –њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤. –•–Њ—В—П —Д–Њ—А–Љ–∞ –µ–µ –Љ–Њ–ґ–µ—В –≤–∞—А—М–Є—А–Њ–≤–∞—В—М, –≥–Њ–ї–Њ–≤–Ї–∞ –≤—Б–µ–≥–і–∞ —П–≤–ї—П–µ—В—Б—П —Б–∞–Љ–Њ–є –±–Њ–ї—М—И–Њ–є —З–∞—Б—В—М—О –ґ–µ–ї–µ–Ј—Л. –Ф–ї—П –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є—Е —Ж–µ–ї–µ–є —Б–ї–µ–і—Г–µ—В —Г—З–Є—В—Л–≤–∞—В—М, —З—В–Њ —А–∞–Ј–Љ–µ—А –≥–Њ–ї–Њ–≤–Ї–Є —Б–≤—Л—И–µ 35 –Љ–Љ, —В–µ–ї–∞ —Б–≤—Л—И–µ 25 –Љ–Љ –Є —Е–≤–Њ—Б—В–∞ –±–Њ–ї—М—И–µ 30 –Љ–Љ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Г–Ї–∞–Ј—Л–≤–∞—О—В –љ–∞ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –Є —Б–≤—П–Ј–∞–љ–љ—Г—О —Б —Н—В–Є–Љ –њ–∞—В–Њ–ї–Њ–≥–Є—О.
–Т –љ–Њ—А–Љ–µ —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А–∞ –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –њ–Њ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –љ–∞–њ–Њ–Љ–Є–љ–∞–µ—В —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А—Г –њ–µ—З–µ–љ–Є. –Я—А–µ–Њ–±–ї–∞–і–∞—О—В –Љ–µ–ї–Ї–Є–µ —Н—Е–Њ—Б–Є–≥–љ–∞–ї—Л, –Ї–Њ—В–Њ—А—Л–µ —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ —А–∞—Б–њ—А–µ–і–µ–ї—П—О—В—Б—П –њ–Њ –≤—Б–µ–є –ґ–µ–ї–µ–Ј–µ. –° –≤–Њ–Ј—А–∞—Б—В–Њ–Љ –≤ —Б–≤—П–Ј–Є —Б —Д–Є–±—А–Њ—В–Є–Ј–∞—Ж–Є–µ–є –Є –Њ—В–ї–Њ–ґ–µ–љ–Є–µ–Љ –ґ–Є—А–∞ —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А–∞ –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П.
–Я—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е –≤ –ґ–µ–ї–µ–Ј–µ –µ–µ —Н—Е–Њ—Б—В—А—Г–Ї—В—Г—А–∞ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Є–Ј–Љ–µ–љ—П–µ—В—Б—П. –Ф–ї—П –Њ—Б—В—А–Њ–≥–Њ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–∞ —Е–∞—А–∞–Ї—В–µ—А–љ–Њ –µ–µ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Є–Ј-–Ј–∞ –Њ—В–µ–Ї–∞ –ґ–µ–ї–µ–Ј—Л, –∞ –њ—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–Љ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–µ –Є —А–∞–Ї–µ вАФ —Г—Б–Є–ї–µ–љ–Є–µ –Є –≥–µ—В–µ—А–Њ–≥–µ–љ–љ–Њ—Б—В—М (–Ј–∞ —Б—З–µ—В —А–∞–Ј–≤–Є—В–Є—П —Д–Є–±—А–Њ–Ј–∞ –Є —А—Г–±—Ж–Њ–≤—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є).
–Т –љ–Њ—А–Љ–µ –і–Є–∞–Љ–µ—В—А –≤–Є—А—Б—Г–љ–≥–Њ–≤–∞ –њ—А–Њ—В–Њ–Ї–∞ –љ–µ –њ—А–µ–≤—Л—И–∞–µ—В 1,5вАУ2 –Љ–Љ. –Я–Њ—Б–ї–µ –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П —Б–µ–Ї—А–µ—В–Є–љ–∞ –µ–≥–Њ –і–Є–∞–Љ–µ—В—А —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –і–Њ 2,5вАУ5 –Љ–Љ. –Я—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–Љ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–µ –љ–µ—А–µ–і–Ї–Њ –≤—Л—П–≤–ї—П—О—В —А–∞—Б—И–Є—А–µ–љ–Є–µ –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—В–Њ–Ї–∞ (–і–Њ 2,5вАУ3,5 –Љ–Љ). –Я–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П —Б–µ–Ї—А–µ—В–Є–љ–∞ –і–Є–∞–Љ–µ—В—А –µ–≥–Њ –њ—А–Њ—Б–≤–µ—В–∞ –њ–Њ—З—В–Є –љ–µ –Є–Ј–Љ–µ–љ—П–µ—В—Б—П, —З—В–Њ —П–≤–ї—П–µ—В—Б—П –≤–∞–ґ–љ—Л–Љ –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–Љ –Ї—А–Є—В–µ—А–Є–µ–Љ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–∞.
–Т —В–∞–±–ї. 3. –њ—А–Є–≤–µ–і–µ–љ—Л –њ—А—П–Љ—Л–µ –Є –Ї–Њ—Б–≤–µ–љ–љ—Л–µ –њ—А–Є–Ј–љ–∞–Ї–Є –љ–µ–Ї–Њ—В–Њ—А—Л—Е –љ–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л.
–Ґ–∞–±–ї–Є—Ж–∞ 3. –Я—А—П–Љ—Л–µ –Є –Ї–Њ—Б–≤–µ–љ–љ—Л–µ —Н—Е–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Є –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л¬† (–њ–Њ –Ь.¬†–Ь.¬†–С–Њ–≥–µ—А—Г –Є –°.¬†–Р.¬†–Ь–Њ—А–і–≤–Њ–≤—Г –≤ –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–Є)
| –£–Ч-–њ–∞—А–∞–Љ–µ—В—А—Л | –Ш–Ј–Љ–µ–љ–µ–љ–Є—П –£–Ч-–њ–∞—А–∞–Љ–µ—В—А–Њ–≤ | –Ч–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є —Б–Є–љ–і—А–Њ–Љ—Л |
| –Я—А—П–Љ—Л–µ –њ—А–Є–Ј–љ–∞–Ї–Є | ||
| –†–∞–Ј–Љ–µ—А –ґ–µ–ї–µ–Ј—Л | –Ф–Є—Д—Д—Г–Ј–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ | –Ю—В–µ–Ї, –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ |
| –°–µ–≥–Љ–µ–љ—В–∞—А–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ | –Ю–њ—Г—Е–Њ–ї—М, –Ї–Є—Б—В–∞, –∞–±—Б—Ж–µ—Б—Б | |
| –Ъ–Њ–љ—В—Г—А –ґ–µ–ї–µ–Ј—Л | –†–Њ–≤–љ—Л–є | –Э–Њ—А–Љ–∞ |
| –°–Љ–∞–Ј–∞–љ–љ—Л–є | –Ю—В–µ–Ї | |
| –Э–µ—А–Њ–≤–љ—Л–є | –Ю–њ—Г—Е–Њ–ї—М, —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –њ–∞–љ–Ї—А–µ–∞—В–Є—В | |
| –У–ї–∞–і–Ї–Є–є, –≤—Л–њ—Г–Ї–ї—Л–є | –Ъ–Є—Б—В–∞ | |
| –≠—Е–Њ—Б—В—А—Г–Ї—В—Г—А–∞ –ґ–µ–ї–µ–Ј—Л | –Э–µ–±–Њ–ї—М—И–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є | –Э–Њ—А–Љ–∞ |
| –£—Б–Є–ї–µ–љ–љ–∞—П | –•—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –њ–∞–љ–Ї—А–µ–∞—В–Є—В | |
| –°–љ–Є–ґ–µ–љ–љ–∞—П | –Ю–њ—Г—Е–Њ–ї—М, –Њ—В–µ–Ї | |
| –≠—Е–Њ–љ–µ–≥–∞—В–Є–≤–љ–∞—П | –Ъ–Є—Б—В–∞ | |
| –Ъ–Њ—Б–≤–µ–љ–љ—Л–µ –њ—А–Є–Ј–љ–∞–Ї–Є | ||
| –Р–Њ—А—В–Њ-–њ–µ—З–µ–љ–Њ—З–љ–Њ–µ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–Њ | –£–≤–µ–ї–Є—З–µ–љ–Є–µ | –Т—Б–µ —Б–ї—Г—З–∞–Є —Г–≤–µ–ї–Є—З–µ–љ–Є—П –ґ–µ–ї–µ–Ј—Л |
| –Ф–Њ—А–Ј–∞–ї—М–љ–∞—П –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М –њ–µ—З–µ–љ–Є | –Т–і–∞–≤–ї–µ–љ–Є—П | –Ю–±—К–µ–Љ–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б |
| –Р–Њ—А—В–∞ –Є –љ–Є–ґ–љ—П—П –њ–Њ–ї–∞—П –≤–µ–љ–∞ | –°–Љ–µ—Й–µ–љ–Є–µ –Є —Б–і–∞–≤–ї–µ–љ–Є–µ | –Ю–±—К–µ–Љ–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б |
| –Ф–Є–∞–Љ–µ—В—А –≤–Є—А—Б—Г–љ–≥–Њ–≤–∞ –њ—А–Њ—В–Њ–Ї–∞ | –£–≤–µ–ї–Є—З–µ–љ | –Ю–±—К–µ–Љ–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б, —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –њ–∞–љ–Ї—А–µ–∞—В–Є—В, —А–µ–∞–Ї—В–Є–≤–љ—Л–є –њ–∞–љ–Ї—А–µ–∞—В–Є—В |
–Э–∞ —А–Є—Б. 12вАУ15 –њ—А–Є–≤–µ–і–µ–љ—Л –і–≤—Г—Е–Љ–µ—А–љ—Л–µ —Н—Е–Њ–≥—А–∞–Љ–Љ—Л –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е —Н—В–Њ–≥–Њ –Њ—А–≥–∞–љ–∞.
 

–†–Є—Б. 12. –≠—Е–Њ–≥—А–∞–Љ–Љ–∞ –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л —Г –±–Њ–ї—М–љ–Њ–≥–Њ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–Њ–Љ
 

–†–Є—Б. 13. –Ш–Ј–Љ–µ–љ–µ–љ–Є—П —Н—Е–Њ–≥—А–∞–Љ–Љ—Л –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л —Г –±–Њ–ї—М–љ–Њ–≥–Њ —Б –њ–∞–љ–Ї—А–µ–Њ–љ–µ–Ї—А–Њ–Ј–Њ–Љ (–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –і–Є–∞–≥–љ–Њ–Ј)
 

–†–Є—Б. 14. –Ф–≤–µ —Н—Е–Њ–≥—А–∞–Љ–Љ—Л –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л (–∞, –±) —Г –±–Њ–ї—М–љ–Њ–≥–Њ —Б –Љ–µ–ї–Ї–Њ–Ї–Є—Б—В–Њ–Ј–љ–Њ–є —В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є–µ–є –≥–Њ–ї–Њ–≤–Ї–Є –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л. –Ь–µ–ї–Ї–Є–µ –Ї–Є—Б—В—Л –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А—Г—О—В—Б—П –≤ –≤–Є–і–µ –љ–µ–±–Њ–ї—М—И–Є—Е –Њ–Ї—А—Г–≥–ї—Л—Е –∞–љ—Н—Е–Њ–≥–µ–љ–љ—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤

–†–Є—Б. 15. –†–∞–Ї –≥–Њ–ї–Њ–≤–Ї–Є –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л
 
–Э–∞–≤–Є–≥–∞—Ж–Є–Њ–љ–љ–∞—П —Е–Є—А—Г—А–≥–Є—П –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –£–Ч–Ш
- Details
- Category: –£–ї—М—В—А–∞–Ј–≤—Г–Ї –≤ —Е–Є—А—Г—А–≥–Є–Є
–Э–∞–≤–Є–≥–∞—Ж–Є–Њ–љ–љ–∞—П —Е–Є—А—Г—А–≥–Є—П –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –£–Ч–Ш
 
–Э–∞–≤–Є–≥–∞—Ж–Є–Њ–љ–љ–∞—П –њ—Г–љ–Ї—Ж–Є–Њ–љ–љ–∞—П —Е–Є—А—Г—А–≥–Є—П –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –£–Ч–Ш вАУ –љ–Њ–≤–Њ–µ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–µ –≤ –Љ–∞–ї–Њ–Є–љ–≤–∞–Ј–Є–≤–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–µ–µ –Є–Ј–ї–µ—З–Є–≤–∞—В—М –љ–µ–Ї–Њ—В–Њ—А—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Њ—А–≥–∞–љ–Њ–≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –±–µ–Ј —А–∞—Б—Б–µ—З–µ–љ–Є—П –њ–Њ–Ї—А–Њ–≤–Њ–≤. –°—Г—В—М –Љ–µ—В–Њ–і–∞ —Б–Њ—Б—В–Њ–Є—В –≤ —В–Њ–Љ, —З—В–Њ —Е–Є—А—Г—А–≥ –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –£–Ч–Ш —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ–є –Є–≥–ї–Њ–є –њ—Г–љ–Ї—В–Є—А—Г–µ—В –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ (–Ї–Є—Б—В–∞, –∞–±—Б—Ж–µ—Б—Б, –њ–Њ–ї–Њ—Б—В—М), –Њ—Б—В–∞–≤–ї—П—П –≤ —В–Ї–∞–љ—П—Е –њ–Њ–ї–Є—Н—В–Є–ї–µ–љ–Њ–≤—Л–є –Ї–∞—В–µ—В–µ—А –і–ї—П –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є —Б–∞–љ–∞—Ж–Є–Є –Є–ї–Є –≤–≤–µ–і–µ–љ–Є—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Я–Њ–Ї–∞–Ј–∞–љ–Є—П –Ї —Н—В–Њ–є –њ—А–Њ—Ж–µ–і—Г—А–µ –і–Њ–≤–Њ–ї—М–љ–Њ –Њ–±—И–Є—А–љ—Л: –ї–Њ–ґ–љ—Л–µ –Ї–Є—Б—В—Л –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л, –њ–∞—А–∞–Ј–Є—В–∞—А–љ—Л–µ –Є –љ–µ–њ–∞—А–∞–Ј–Є—В–∞—А–љ—Л–µ –Ї–Є—Б—В—Л –њ–µ—З–µ–љ–Є, –∞–±—Б—Ж–µ—Б—Б—Л –њ–µ—З–µ–љ–Є, –Ј–∞–±—А—О—И–Є–љ–љ–Њ–≥–Њ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–∞, –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–µ –∞–±—Б—Ж–µ—Б—Б—Л –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є - –њ–Њ–і–і–Є–∞—Д—А–∞–≥–Љ–∞–ї—М–љ—Л–µ, –њ–Њ–і–њ–µ—З–µ–љ–Њ—З–љ—Л–µ, –Љ–µ–ґ–Ї–Є—И–µ—З–љ—Л–µ. –І–∞—Й–µ —В–∞–Ї–Є–µ —Б–Є—В—Г–∞—Ж–Є–Є¬† –≤–Њ–Ј–љ–Є–Ї–∞–ї–Є –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–є –њ–Њ –њ–Њ–≤–Њ–і—Г –Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л—Е —Д–Њ—А–Љ —П–Ј–≤–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –ґ–µ–ї—Г–і–Ї–∞.
 
–Т –†–Њ—Б—Б–Є–Є –њ—Г–љ–Ї—Ж–Є–Њ–љ–љ–∞—П —Е–Є—А—Г—А–≥–Є—П —Б—Г—Й–µ—Б—В–≤—Г–µ—В –≤–Њ –Љ–љ–Њ–≥–Є—Е –≥–Њ—А–Њ–і–∞—Е.¬† –Ю—Б–Њ–±—Л—Е —В—А–µ–±–Њ–≤–∞–љ–Є–є –Ї –∞–њ–њ–∞—А–∞—В–∞–Љ –£–Ч–Ш –љ–µ—В, –љ–Њ —З–µ–Љ –ї—Г—З—И–µ, —В–µ–Љ –ї—Г—З—И–µ. –Т–∞–ґ–љ–µ–µ, –Ї–∞–Ї —З–µ–ї–Њ–≤–µ–Ї —Б–Љ–Њ—В—А–Є—В, –Ї —З–µ–Љ—Г –њ—А–Є–≤—Л–Ї–∞–µ—В.¬†
 
–Ф–ї—П –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Њ–≥–Њ —Е–Є—А—Г—А–≥–∞ –≤—Б–µ–≥–і–∞ –±–µ—Б–њ–Њ–Ї–Њ–є–љ–Њ, –љ–∞—Б–Ї–Њ–ї—М–Ї–Њ —Н—В–Є –њ—Г–љ–Ї—Ж–Є–Є —А–∞–і–Є–Ї–∞–ї—М–љ—Л? –°–µ–є—З–∞—Б –±–Њ–ї—М—И–µ –Ј–∞–љ–Є–Љ–∞—О—В—Б—П –ї–µ—З–µ–љ–Є–µ–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є: –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Є —Б–∞–Љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є. –° —Г–≤–µ—А–µ–љ–љ–Њ—Б—В—М—О –Љ–Њ–ґ–љ–Њ —Б–Ї–∞–Ј–∞—В—М, —З—В–Њ –≤ 70% —Б–ї—Г—З–∞–µ–≤ –њ—Г–љ–Ї—Ж–Є–Њ–љ–љ–∞—П ¬†—Е–Є—А—Г—А–≥–Є—П вАУ —Н—В–Њ –Ј–∞–Ї–Њ–љ—З–µ–љ–љ–∞—П –Њ–њ–µ—А–∞—Ж–Є—П, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–∞—П –і–Њ–±–Є—В—М—Б—П —А–∞–і–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Є–Ј–ї–µ—З–µ–љ–Є—П. –Ш–љ–Њ–≥–і–∞ –њ—А–Є—Е–Њ–і–Є—В—Б—П –≤–Љ–µ—И–Є–≤–∞—В—М—Б—П –њ–Њ–≤—В–Њ—А–љ–Њ. –Я—А–Є –≥–љ–Њ–є–љ—Л—Е –∞–±—Б—Ж–µ—Б—Б–∞—Е –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤–≤–µ–і–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –њ—А–Є –љ–µ–њ–∞—А–∞–Ј–Є—В–∞—А–љ—Л—Е –Ї–Є—Б—В–∞—Е –њ–µ—З–µ–љ–Є вАУ —Б–Ї–ї–µ—А–Њ–Ј–Є—А–Њ–≤–∞–љ–Є–µ 96¬Ї —Б–њ–Є—А—В–Њ–Љ. –Т —Б—А–µ–і–љ–µ–Љ, –Љ–µ—В–Њ–і –≤ 2 —А–∞–Ј–∞ —Б–Њ–Ї—А–∞—Й–∞–µ—В –Є –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–є –њ–µ—А–Є–Њ–і, –Є —Б—А–Њ–Ї–Є —Г—В—А–∞—В—Л —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є. –Ю–±–µ–Ј–±–Њ–ї–Є–≤–∞–љ–Є–µ –њ—А–Є–Љ–µ–љ—П–µ–Љ –Љ–µ—Б—В–љ–Њ–µ, –њ–Њ —Е–Њ–і—Г –≤—Б–µ–≥–Њ –Ї–∞–љ–∞–ї–∞ –≤–≤–Њ–і—П—В –љ–Њ–≤–Њ–Ї–∞–Є–љ –Є–ї–Є –ї–Є–і–Њ–Ї–∞–Є–љ. –С–Њ–ї—М–љ—Л–µ, –і–∞–ґ–µ —Б –Љ–Њ–±–Є–ї—М–љ–Њ–є –њ—Б–Є—Е–Є–Ї–Њ–є, –њ–µ—А–µ–љ–Њ—Б—П—В –Њ–њ–µ—А–∞—Ж–Є—О —Е–Њ—А–Њ—И–Њ. –Ъ–∞—В–µ—В–µ—А –і–µ—А–ґ–∞—В –љ–µ –Љ–µ–љ–µ–µ –Љ–µ—Б—П—Ж–∞, –њ–∞—Ж–Є–µ–љ—В—Л –њ—А–Є—Е–Њ–і—П—В –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ. –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –і–µ–±–Є—В–∞ –Є —А–∞–Ј–Љ–µ—А–Њ–≤ –њ–Њ–ї–Њ—Б—В–Є —А–µ—И–∞—О—В, –Ї–Њ–≥–і–∞ –µ–≥–Њ —Г–і–∞–ї—П—В—М. –Ъ–Є—Б—В—Л –њ–µ—З–µ–љ–Є –ї–µ—З–Є—В—М —В—П–ґ–µ–ї–µ–µ –≤—Б–µ–≥–Њ, –Њ–љ–Є —З–∞—Й–µ —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—В.
–Я—А–Њ–≤–Њ–і–Є—В—М –њ—Г–љ–Ї—Ж–Є–Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –Є –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є —В–Њ–Љ–Њ–≥—А–∞—Д–Є–Є. –Ю–і–љ–∞–Ї–Њ, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П –Љ–∞–љ–Є–њ—Г–ї—П—Ж–Є–є –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –£–Ч–Ш, –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –Ъ–Ґ, –≤ —В–Њ–Љ, —З—В–Њ –њ—А–Њ—Ж–µ–і—Г—А–∞ –њ—А–Њ—Е–Њ–і–Є—В –≤ —А–µ–ґ–Є–Љ–µ —А–µ–∞–ї—М–љ–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є.
 
–Х—Б–ї–Є –≥–Њ–≤–Њ—А–Є—В—М –Њ —Б–Њ–≤–Љ–µ—Й–µ–љ–Є–Є –љ–∞–≤–Є–≥–∞—Ж–Є–Њ–љ–љ–Њ–є –Є —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–є —Е–Є—А—Г—А–≥–Є–Є, —В–Њ —Н—В–Њ –≤–њ–Њ–ї–љ–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ. –Э–∞–њ—А–Є–Љ–µ—А, —Ж–Є—Б—В–Њ–µ—О–љ–Њ–∞–љ–∞—Б—В–Њ–Љ–Њ–Ј –њ—А–Є –Ї–Є—Б—В–µ –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л. –°–µ–є—З–∞—Б –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –£–Ч–Ш¬† –љ–∞–Ї–ї–∞–і—Л–≤–∞–µ—О—В –њ–∞–љ–Ї—А–µ–∞—В–Њ—Ж–Є—Б—В–Њ–≥–∞—Б—В—А–Њ–∞–љ–∞—Б—В–Њ–Љ–Њ–Ј—Л. –Ъ–Њ–≥–і–∞ –µ—Б—В—М —Е–Њ—А–Њ—И–∞—П –Ї–Є—Б—В–∞, –Ї–Њ—В–Њ—А–∞—П –≤—Л–±—Г—Е–∞–µ—В —З–µ—А–µ–Ј –Ј–∞–і–љ—О—О —Б—В–µ–љ–Ї—Г –ґ–µ–ї—Г–і–Ї–∞, –њ—Г–љ–Ї—В–Є—А—Г—О—В –Њ–±–µ —Б—В–µ–љ–Ї–Є –ґ–µ–ї—Г–і–Ї–∞ –Є –Ї–Є—Б—В—Г. –Ш—Б–њ–Њ–ї—М–Ј—Г–µ–Љ –і—А–µ–љ–∞–ґ —Б —Д–Є–Ї—Б–Є—А—Г—О—Й–Є–Љ—Б—П –Ї–Њ–љ—Ж–Њ–Љ, –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ –њ–Њ–і—В—П–≥–Є–≤–∞—П –µ–≥–Њ. –Ю–±—А–∞–Ј—Г–µ—В—Б—П –њ—А–Њ–ї–µ–ґ–µ–љ—М –Љ–µ–ґ–і—Г –њ–µ—А–µ–і–љ–µ–є —Б—В–µ–љ–Ї–Њ–є –Ї–Є—Б—В—Л –Є –Ј–∞–і–љ–µ–є —Б—В–µ–љ–Ї–Њ–є –ґ–µ–ї—Г–і–Ї–∞. –Я—А–Є–Љ–µ—А–љ–Њ —З–µ—А–µ–Ј –љ–µ–і–µ–ї—О —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П –∞–љ–∞—Б—В–Њ–Љ–Њ–Ј 1—Е2,5—Б–Љ. –Ф–µ–Ї–Њ–Љ–њ—А–µ—Б—Б–Є—П –ґ–µ–ї—Г–і–Ї–∞ –љ–∞–Ј–Њ–≥–∞—Б—В—А–∞–ї—М–љ—Л–Љ –Ј–Њ–љ–і–Њ–Љ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Є–Ј–±–µ–ґ–∞—В—М –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –≤ –≤–Є–і–µ, –љ–∞–њ—А–Є–Љ–µ—А, –њ–Њ–і—В–µ–Ї–∞–љ–Є—П –ґ–µ–ї—Г–і–Њ—З–љ–Њ–≥–Њ —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–≥–Њ —З–µ—А–µ–Ј –њ—А–Њ–Ї–Њ–ї –њ–µ—А–µ–і–љ–µ–є —Б—В–µ–љ–Ї–Є.
–Э–∞–≤–Є–≥–∞—Ж–Є–Њ–љ–љ–Њ–є —Е–Є—А—Г—А–≥–Є–µ–є –њ–Њ–ї—М–Ј—Г—О—В—Б—П¬† —Г—А–Њ–ї–Њ–≥–Є. –Ю–љ–Є –і—А–µ–љ–Є—А—Г—О—В –Ї–Є—Б—В—Л, –∞–±—Б—Ж–µ—Б—Б—Л –њ–Њ—З–µ–Ї, –Њ–њ–µ—А–Є—А—Г—О—В –≥–Є–і—А–Њ–љ–µ—Д—А–Њ–Ј, –і—А–µ–љ–Є—А—Г—О—В –ї–Њ—Е–∞–љ–Ї–Є вАУ –њ—Г–љ–Ї—Ж–Є–Њ–љ–љ–∞—П –љ–µ—Д—А–Њ—Б—В–Њ–Љ–Є—П. –Я–Њ—В–Њ–Љ —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—О—В —Б—В–µ–љ—В –≤ –Љ–Њ—З–µ—В–Њ—З–љ–Є–Ї. –Т –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є–Є¬† –њ—Г–љ–Ї—В–Є—А—Г—О—В –Њ—З–µ–љ—М –±–Њ–ї—М—И–Є–µ –Ї–Є—Б—В—Л —П–Є—З–љ–Є–Ї–Њ–≤.
–Ю–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ —Б–ї–Њ–ґ–љ—Л—Е —Б–ї—Г—З–∞–µ–≤ –љ–µ–Њ—В–ї–Њ–ґ–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є
- Details
- Category: –£–ї—М—В—А–∞–Ј–≤—Г–Ї –≤ —Е–Є—А—Г—А–≥–Є–Є
¬†–£–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ (–£–Ч–Ш) –≤ —В–µ—З–µ–љ–Є–µ —Г–ґ–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є —П–≤–ї—П–µ—В—Б—П –≤–µ–і—Г—Й–Є–Љ –Љ–µ—В–Њ–і–Њ–Љ –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –≤ —Н–Ї—Б—В—А–µ–љ–љ–Њ–є –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є. –Т –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М —Н—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –µ–≥–Њ –≤—Л—Б–Њ–Ї–Њ–є –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ–Њ—Б—В—М—О –њ—А–Є —Ж–µ–ї–Њ–Љ —А—П–і–µ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –љ–∞—А—П–і—Г —Б –і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М—О –Є –∞–±—Б–Њ–ї—О—В–љ–Њ–є –љ–µ–Є–љ–≤–∞–Ј–Є–≤–љ–Њ—Б—В—М—О –і–ї—П –њ–∞—Ж–Є–µ–љ—В–∞. –Ю–і–љ–∞–Ї–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є–Ј–љ–∞—В—М, —З—В–Њ –≤–Њ –Љ–љ–Њ–≥–Є—Е —Б–ї—Г—З–∞—П—Е —Б—В–∞–љ–і–∞—А—В–љ–∞—П —Г–ї—М—В—А–∞—Б–Њ–љ–Њ–≥—А–∞—Д–Є—П —Б –њ–Њ–Њ—З–µ—А–µ–і–љ—Л–Љ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ –≤—Б–µ—Е –Њ—А–≥–∞–љ–Њ–≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –љ–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤–µ—А–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М –і–Є–∞–≥–љ–Њ–Ј –Є, —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –Њ–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П –±–µ—Б–њ–Њ–ї–µ–Ј–љ–Њ–є –≤ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є —В–∞–Ї—В–Є–Ї–Є. –Т–∞–ґ–љ—Г—О —А–Њ–ї—М –њ—А–Є–Њ–±—А–µ—В–∞–µ—В —В—Й–∞—В–µ–ї—М–љ—Л–є –∞–љ–∞–ї–Є–Ј –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –Є —Ж–µ–ї–µ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л–є –њ–Њ–Є—Б–Ї¬† –њ—А–Є –£–Ч–Ш —В–µ—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –Њ–±—К–µ–і–Є–љ–Є—В—М –Є–Љ–µ—О—Й–Є–µ—Б—П —Б–Є–Љ–њ—В–Њ–Љ—Л. –Ф–∞–љ–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Љ–Њ–≥—Г—В –љ–µ –Є–Љ–µ—В—М –Њ—А–≥–∞–љ–љ–Њ–є –њ—А–Є–љ–∞–і–ї–µ–ґ–љ–Њ—Б—В–Є (–≤—Л–њ–Њ—В, –њ–∞—А–µ—В–Є—З–љ—Л–µ –њ–µ—В–ї–Є –Ї–Є—И–µ—З–љ–Є–Ї–∞, –љ–∞—А—Г—И–µ–љ–Є–µ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞, —А–µ–≥–Є—Б—В—А–Є—А—Г–µ–Љ–Њ–µ –њ—А–Є –і–Њ–њ–њ–ї–µ—А–Њ–≥—А–∞—Д–Є–Є) –Є –љ–µ —Г–Ї–∞–Ј—Л–≤–∞—В—М –њ—А—П–Љ–Њ –љ–∞ –Є–Љ–µ—О—Й—Г—О—Б—П –њ–∞—В–Њ–ї–Њ–≥–Є—О. –Э–∞–Є–±–Њ–ї—М—И–Є–µ —В—А—Г–і–љ–Њ—Б—В–Є –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –њ–Њ—Б—В–∞–љ–Њ–≤–Ї–∞ –і–Є–∞–≥–љ–Њ–Ј–∞ –њ—А–Є –љ–µ–ї–Њ–Ї–∞–ї–Є–Ј–Њ–≤–∞–љ–љ—Л—Е –±–Њ–ї—П—Е –≤ –ґ–Є–≤–Њ—В–µ, –њ—А–Є —В—П–ґ–µ–ї–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є–Є –±–Њ–ї—М–љ–Њ–≥–Њ –Є –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —Г—В–Њ—З–љ–Є—В—М –∞–љ–∞–Љ–љ–µ–Ј, –њ—А–Є —Б—В–µ—А—В–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–µ —Г –њ–Њ–ґ–Є–ї—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Т—А–∞—З—Г –£–Ч-–і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —З–µ—В–Ї–Њ –њ—А–µ–і—Б—В–∞–≤–ї—П—В—М –Ї—А—Г–≥ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, —Б—А–µ–і–Є –Ї–Њ—В–Њ—А—Л—Е –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Њ–≤–Њ–і–Є—В—М –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ—Л–є –њ–Њ–Є—Б–Ї, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —Е–Є—А—Г—А–≥–∞–Љ, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є–Љ –љ–µ–Њ—В–ї–Њ–ґ–љ—Г—О –њ–Њ–Љ–Њ—Й—М, –Є–Љ–µ—В—М –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є–µ –Њ —Н—Е–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є—Е —Д–µ–љ–Њ–Љ–µ–љ–∞—Е –Є –Є—Е –Ј–љ–∞—З–µ–љ–Є–Є.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л. –С—Л–ї –Њ–±–Њ–±—Й–µ–љ –Њ–њ—Л—В —А–∞–±–Њ—В—Л —Б–ї—Г–ґ–±—Л –£–Ч–Ш –≤ –љ–µ–Њ—В–ї–Њ–ґ–љ–Њ–є –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є –Ј–∞ –њ–µ—А–Є–Њ–і 2001-2010 –≥–≥. –њ—А–Є –µ–ґ–µ–≥–Њ–і–љ–Њ–Љ –≤—Л–њ–Њ–ї–љ–µ–љ–Є–Є –і–Њ 2000 –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є (SonoAce PicoMedison). –Т—Л—П–≤–ї–µ–љ–љ—Л–µ —Г–ї—М—В—А–∞—Б–Њ–љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–µ —Д–µ–љ–Њ–Љ–µ–љ—Л —Б–Њ–Њ—В–љ–Њ—Б–Є–ї–Є —Б –і–∞–љ–љ—Л–Љ–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –Є–љ—Д—А–∞–Ї—А–∞—Б–љ–Њ–є —В–µ—А–Љ–Њ–≥—А–∞—Д–Є–Є (CEM ThermoDiagnostic), –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є –Є –Љ–∞–≥–љ–Є—В–љ–Њ-—А–µ–Ј–Њ–љ–∞–љ—Б–љ–Њ–є —В–Њ–Љ–Њ–≥—А–∞—Д–Є–Є, —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ–є –∞–љ–≥–Є–Њ–≥—А–∞—Д–Є–Є, –Є–љ—В—А–∞–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–є —А–µ–≤–Є–Ј–Є–Є –Њ—А–≥–∞–љ–Њ–≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є, –≤–µ—А–Є—Д–Є—Ж–Є—А–Њ–≤–∞–ї–Є –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є (—В–Њ–љ–Ї–Њ–Є–≥–Њ–ї—М–љ–∞—П –Є –Є–љ—В—А–∞–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–∞—П –±–Є–Њ–њ—Б–Є—П —В–Ї–∞–љ–µ–є), –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –≤–Љ–µ—Б—В–µ —Б —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –Є –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є –Њ–±—Б—Г–ґ–і–µ–љ–Є–µ. –Я—А–µ–і—Б—В–∞–≤–ї—П–љ—Л —Б–∞–Љ—Л–µ —Б–ї–Њ–ґ–љ—Л–µ¬† –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–Љ –њ–ї–∞–љ–µ –Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —З–∞—Б—В–Њ –≤—Б—В—А–µ—З–∞—О—Й–Є–µ—Б—П –≤ —Н–Ї—Б—В—А–µ–љ–љ–Њ–є –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П вАУ –Љ–µ–Ј–µ–љ—В–µ—А–Є–∞–ї—М–љ—Л–є —В—А–Њ–Љ–±–Њ–Ј –Є –і–µ—Б—В—А—Г–Ї—В–Є–≤–љ—Л–є –њ–∞–љ–Ї—А–µ–∞—В–Є—В. –Т –Ї–∞—А—В–Є–љ–µ —Н—В–Є—Е –±–Њ–ї–µ–Ј–љ–µ–є –Љ–љ–Њ–≥–Њ –Њ–±—Й–µ–≥–Њ вАУ –Њ—Б—В—А–Њ–µ –љ–∞—З–∞–ї–Њ, –Є–љ—В–µ–љ—Б–Є–≤–љ—Л–є –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ, —З–∞—Б—В–Њ–µ —А–∞–љ–љ–µ–µ —А–∞–Ј–≤–Є—В–Є–µ —И–Њ–Ї–∞, –Є–Ј–љ–∞—З–∞–ї—М–љ–Њ —В—П–ґ–µ–ї–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є –і—А. –Ю–њ–Є—Б—Л–≤–∞–µ–Љ—Л–µ –Њ–њ–Њ—А–љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Ї—А–Є—В–µ—А–Є–Є —П–≤–ї—П—О—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –≤—Б—В—А–µ—З–∞—О—Й–Є–Љ–Є—Б—П –Є —Б–њ–µ—Ж–Є—Д–Є—З–љ—Л–Љ–Є –Є, –±–µ–Ј—Г—Б–ї–Њ–≤–љ–Њ, –љ–µ –Њ—В—А–∞–ґ–∞—О—В –≤—Б–µ–≥–Њ –Љ–љ–Њ–≥–Њ–Њ–±—А–∞–Ј–Є—П —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є. –Ю–і–љ–∞–Ї–Њ –Њ–љ–Є –Љ–Њ–≥—Г—В –±—Л—В—М –≤—Л—П–≤–ї–µ–љ—Л –≤—А–∞—З–Њ–Љ –£–Ч-–і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –њ—А–Є —Б–ґ–∞—В–Њ–Љ –Њ—Б–Љ–Њ—В—А–µ –Є —А–∞—Б—Б–њ—А–Њ—Б–µ –њ–∞—Ж–Є–µ–љ—В–∞ –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –њ–µ—А–µ–і –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ. –Ґ–∞–Ї–ґ–µ –њ—А–Є–≤–Њ–і–Є–Љ –љ–∞–±–ї—О–і–µ–љ–Є—П –њ–Њ —Н—Е–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –≤ –љ–µ—Б—В–∞–љ–і–∞—А—В–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є—В—Г–∞—Ж–Є—П—Е.
–Ь–µ–Ј–µ–љ—В–µ—А–Є–∞–ї—М–љ—Л–є —В—А–Њ–Љ–±–Њ–Ј. –Ч–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ —Б–≤—П–Ј–∞–љ–Њ —Б –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –≤ —Б–Њ—Б—Г–і–∞—Е –Ї–Є—И–µ—З–љ–Є–Ї–∞. –Ґ—П–ґ–µ–ї—Л–µ —Д–Њ—А–Љ—Л —Б –≤—Л—Б–Њ–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П –њ—А–Є —В—А–Њ–Љ–±–Њ–Ј–µ —Г—Б—В—М—П –≤–µ—А—Е–љ–µ–є –±—А—Л–ґ–µ–µ—З–љ–Њ–є –∞—А—В–µ—А–Є–Є (–Т–С–Р) —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ —В–Њ—В–∞–ї—М–љ—Л–Љ –Є–ї–Є —Б—Г–±—В–Њ—В–∞–ї—М–љ—Л–Љ –љ–µ–Ї—А–Њ–Ј–Њ–Љ —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є. –Ґ–∞–Ї–Њ–µ —В–µ—З–µ–љ–Є–µ –±–Њ–ї–µ–Ј–љ–Є –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Г 85% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ—Б—В—А—Л–Љ –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –Љ–µ–Ј–µ–љ—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ . –Т 5-15% —Б–ї—Г—З–∞—П—Е¬† –Є–Љ–µ—О—В –Љ–µ—Б—В–Њ –≤–µ–љ–Њ–Ј–љ—Л–µ —Д–Њ—А–Љ—Л —В—А–Њ–Љ–±–Њ–Ј–∞, –Њ—Б–ї–Њ–ґ–љ—П—О—Й–Є–µ —В–µ—З–µ–љ–Є–µ —А–∞–Ј–ї–Є—З–љ—Л—Е —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Њ—А–≥–∞–љ–Њ–≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є (–Ї–Є—И–µ—З–љ–Њ–є –љ–µ–њ—А–Њ—Е–Њ–і–Є–Љ–Њ—Б—В–Є, –њ–µ—А–Є—В–Њ–љ–Є—В–∞, –Њ–њ—Г—Е–Њ–ї–µ–є –Є –і—А.) . –Я—А–Є —В—А–Њ–Љ–±–Њ–Ј–µ –≤–µ–љ –Ї–Є—И–µ—З–љ–Є–Ї–∞ —З–∞—Й–µ –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Б–µ–≥–Љ–µ–љ—В–∞—А–љ–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ –Ї–Є—И–Ї–Є.
–Ю–њ–Њ—А–љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Ї—А–Є—В–µ—А–Є–Є.
¬Ј¬†¬†¬†¬†¬†¬†¬† –Т–Њ–Ј—А–∞—Б—В —Б—В–∞—А—И–µ 50 –ї–µ—В
¬Ј¬†¬†¬†¬†¬†¬†¬† –Ю—Б—В—А–Њ–µ –љ–∞—З–∞–ї–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П
¬Ј¬†¬†¬†¬†¬†¬†¬† –Э–∞–ї–Є—З–Є–µ ¬Ђ—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ¬ї –∞–љ–∞–Љ–љ–µ–Ј–∞
¬Ј¬†¬†¬†¬†¬†¬†¬† –Т—Л—А–∞–ґ–µ–љ–љ—Л–µ –±–Њ–ї–Є –≤ –ґ–Є–≤–Њ—В–µ –њ—А–Є –Љ—П–≥–Ї–Њ–є –±—А—О—И–љ–Њ–є —Б—В–µ–љ–Ї–µ
¬Ј¬†¬†¬†¬†¬†¬†¬† –Я–µ—А–Є—В–Њ–љ–µ–∞–ї—М–љ–∞—П —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–∞ –њ–Њ—П–≤–ї—П–µ—В—Б—П –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –њ–Њ–Ј–і–љ–Њ
–≠—Е–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є–µ —Д–µ–љ–Њ–Љ–µ–љ—Л. –Я—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ–Њ –≤–∞–ґ–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є—П –њ—А–Є –£–Ч–Ш –±—А—О—И–љ–Њ–є –∞–Њ—А—В—Л –Є –Њ—В—Е–Њ–і—П—Й–Є—Е –Њ—В –љ–µ–µ –≤–Є—Б—Ж–µ—А–∞–ї—М–љ—Л—Е –≤–µ—В–≤–µ–є вАУ —З—А–µ–≤–љ–Њ–≥–Њ —Б—В–≤–Њ–ї–∞ (–І–°) –Є –Т–С–Р (–†–Є—Б 1).
–Ф–∞–ї–µ–µ –њ—А–Њ–≤–Њ–і–Є—В—Б—П –і–Њ–њ–њ–ї–µ—А–Њ–≥—А–∞—Д–Є—П –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –≤ —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –∞—А—В–µ—А–Є–∞–ї—М–љ—Л—Е —Б—В–≤–Њ–ї–∞—Е. –Т –љ–Њ—А–Љ–µ –і–Њ–њ–њ–ї–µ—А–Њ–≥—А–∞–Љ–Љ–∞ –≤ –І–° –Є –Т–С–Р (–†–Є—Б. 2) –Є–Љ–µ–µ—В –∞—А—В–µ—А–Є–∞–ї—М–љ—Л–є —В–Є–њ —Б –њ–Є–Ї–Њ–≤—Л–Љ–Є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Є–Љ–Є —Б–Ї–Њ—А–Њ—Б—В—П–Љ–Є 155¬±13 —Б–Љ\—Б –Є 141¬±13 —Б–Љ\—Б —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –Ї–Њ–љ–µ—З–љ–Њ-–і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Є–Љ–Є —Б–Ї–Њ—А–Њ—Б—В—П–Љ–Є 53¬±4 —Б–Љ\—Б –Є 20¬±2 —Б–Љ\—Б.
–Я—А–Є –њ–∞—В–Њ–ї–Њ–≥–Є–Є —Г—Б—В—М—П –Т–С–Р –Љ–Њ–ґ–µ—В –Є–Љ–µ—В—М¬† –Љ–µ—Б—В–Њ –Њ—В—Б—Г—В—Б—В–≤–Є–µ —А–µ–≥–Є—Б—В—А–∞—Ж–Є–Є –і–Њ–њ–њ–ї–µ—А–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Њ–є –Ї—А–Є–≤–Њ–є –≤ –њ—А–Њ—Б–≤–µ—В–µ –і–∞–љ–љ–Њ–≥–Њ —Б–Њ—Б—Г–і–∞, –∞ –≤ —Б–ї—Г—З–∞–µ –љ–∞–ї–Є—З–Є—П –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –Њ–љ –љ–Њ—Б–Є—В –Є–Ј–Љ–µ–љ–µ–љ–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А, —З—В–Њ –≤—Л—А–∞–ґ–∞–µ—В—Б—П –≤ –≤–Є–і–µ –њ—А–Є—В—Г–њ–ї–µ–љ–Є—П –њ–Є–Ї–∞ —Б–Ї–Њ—А–Њ—Б—В–Є –Є —Г–і–ї–Є–љ–µ–љ–Є—П –≤—А–µ–Љ–µ–љ–Є –њ–Њ–і—К–µ–Љ–∞ –Є —Б–њ–∞–і–∞ —Б–Ї–Њ—А–Њ—Б—В–Є –њ—Г–ї—М—Б–Њ–≤–Њ–є –≤–Њ–ї–љ—Л (–†–Є—Б. 3).¬†
–Т–∞–ґ–љ—Л–Љ —Б—З–Є—В–∞–µ–Љ –љ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –∞–±—Б–Њ–ї—О—В–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Б–Ї–Њ—А–Њ—Б—В–µ–є –≤ –Т–С–Р, –∞ —Б—А–∞–≤–љ–µ–љ–Є–µ –Ї—А–Є–≤—Л—Е, –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –Є–Ј –Т–С–Р –Є –І–°. –£ –Њ–і–љ–Њ–≥–Њ –±–Њ–ї—М–љ–Њ–≥–Њ –≤ –љ–Њ—А–Љ–µ —Е–∞—А–∞–Ї—В–µ—А –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –≤ –љ–Є—Е –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –Є–і–µ–љ—В–Є—З–µ–љ. –Ш–Ј–Љ–µ–љ–µ–љ–Є–µ –і–Њ–њ–њ–ї–µ—А–Њ–≥—А–∞–Љ–Љ—Л –Т–С–Р –њ–Њ –Њ—В–љ–Њ—И–µ–љ–Є—О –Ї —В–∞–Ї–Њ–≤–Њ–є –≤ –І–° —П–≤–ї—П–µ—В—Б—П –≤–∞–ґ–љ—Л–Љ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ-–і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–Љ –Ї—А–Є—В–µ—А–Є–µ–Љ –љ–∞—А—Г—И–µ–љ–Є—П –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –Љ–µ–Ј–µ–љ—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П (–†–Є—Б.4).¬†
–Ф—А—Г–≥–Є–Љ –∞—Б–њ–µ–Ї—В–Њ–Љ —Н—Е–Њ—Б–µ–Љ–Є–Њ—В–Є–Ї–Є —П–≤–ї—П–µ—В—Б—П –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є—П –љ–µ–њ–µ—А–Є—Б—В–∞–ї—М—В–Є—А—Г—О—Й–Є—Е —В–Њ–љ–Ї–Њ—Б—В–µ–љ–љ—Л—Е –њ–µ—В–µ–ї—М –Ї–Є—И–µ—З–љ–Є–Ї–∞, –Ј–∞–њ–Њ–ї–љ–µ–љ–љ—Л—Е –ґ–Є–і–Ї–Њ—Б—В—М—О, –∞ —В–∞–Ї–ґ–µ –љ–∞—А—Г—И–µ–љ–Є–µ —Б–ї–Њ–Є—Б—В–Њ–≥–Њ —Б—В—А–Њ–µ–љ–Є—П —Б—В–µ–љ–Ї–Є –Ї–Є—И–Ї–Є. –Ш–Љ–µ—О—В—Б—П —А–∞–±–Њ—В—Л, —Г–Ї–∞–Ј—Л–≤–∞—О—Й–Є–µ –љ–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —А–µ–≥–Є—Б—В—А–∞—Ж–Є–Є –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –≤ —Б—В–µ–љ–Ї–µ –Ї–Є—И–Ї–Є –Є–ї–Є –µ–≥–Њ –Њ—В—Б—Г—В—Б—В–≤–Є–µ, –Њ–і–љ–∞–Ї–Њ –Љ—Л –љ–µ —А–∞—Б–њ–Њ–ї–∞–≥–∞–µ–Љ –њ–Њ–і–Њ–±–љ—Л–Љ –Њ–њ—Л—В–Њ–Љ. –Э–∞–ї–Є—З–Є–µ –±–Њ–ї—М—И–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –≤—Л–њ–Њ—В–∞ –≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ —А–∞–љ–љ–Є–µ —Б—А–Њ–Ї–Є –±–Њ–ї–µ–Ј–љ–Є, –љ–µ —Е–∞—А–∞–Ї—В–µ—А–љ–Њ.
–Ф–µ—Б—В—А—Г–Ї—В–Є–≤–љ—Л–є –њ–∞–љ–Ї—А–µ–∞—В–Є—В. –Ю—Б—В—А—Л–є –њ–∞–љ–Ї—А–µ–∞—В–Є—В вАУ —Д–∞–Ј–Њ–≤–Њ –њ—А–Њ—В–µ–Ї–∞—О—Й–µ–µ —В—П–ґ–µ–ї–Њ–µ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ, –Є–Љ–µ—О—Й–µ–µ –≤ —Б–≤–Њ–µ–є –Њ—Б–љ–Њ–≤–µ –љ–µ–Ї—А–Њ–Ј –Ї–ї–µ—В–Њ–Ї –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л, –Ј–∞–њ—Г—Б–Ї–∞—О—Й–Є–є –Ї–∞—Б–Ї–∞–і —Б–Є—Б—В–µ–Љ–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤, –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –Є –Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є.
–Ю–њ–Њ—А–љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Ї—А–Є—В–µ—А–Є–Є .
¬Ј¬†¬†¬†¬†¬†¬†¬† –Ч–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –љ–∞—З–Є–љ–∞–µ—В—Б—П –Њ—Б—В—А–Њ —Б –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є –±–Њ–ї–Є –≤ –љ–∞–і—З—А–µ–≤–љ–Њ–є –Њ–±–ї–∞—Б—В–Є –Њ–њ–Њ—П—Б—Л–≤–∞—О—Й–µ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞ —Б –Є—А—А–∞–і–Є–∞—Ж–Є–µ–є –≤ –њ–Њ–і—А–µ–±–µ—А—М—П, —Б–њ–Є–љ—Г, –ї–µ–≤—Г—О –ї–Њ–њ–∞—В–Ї—Г
¬Ј¬†¬†¬†¬†¬†¬†¬† –•–∞—А–∞–Ї—В–µ—А –±–Њ–ї–Є –њ–Њ—Б—В–Њ—П–љ–љ—Л–є
¬Ј¬†¬†¬†¬†¬†¬†¬† –Я–Њ—П–≤–ї–µ–љ–Є—О –±–Њ–ї–µ–є –њ—А–µ–і—И–µ—Б—В–≤—Г–µ—В –љ–∞—А—Г—И–µ–љ–Є–µ –і–Є–µ—В—Л, –Њ–±–Є–ї—М–љ—Л–є –њ—А–Є–µ–Љ –ґ–Є—А–љ–Њ–є –Є –Њ—Б—В—А–Њ–є –њ–Є—Й–Є, –∞–ї–Ї–Њ–≥–Њ–ї–Є–Ј–∞—Ж–Є—П, –Ј–∞–њ–Њ–є, —Г –ґ–µ–љ—Й–Є–љ —З–∞—Б—В—Л —Г–Ї–∞–Ј–∞–љ–Є—П –љ–∞ –ґ–µ–ї—З–љ—Л–µ –Ї–∞–Љ–љ–Є
¬Ј¬†¬†¬†¬†¬†¬†¬† –С–Њ–ї—М —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —В–Њ—И–љ–Њ—В–Њ–є, –Љ–љ–Њ–≥–Њ–Ї—А–∞—В–љ–Њ–є —А–≤–Њ—В–Њ–є
¬Ј¬†¬†¬†¬†¬†¬†¬† –Я–Њ–≤—Л—И–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –і–Є–∞—Б—В–∞–Ј—Л –≤ –Љ–Њ—З–µ
¬Ј¬†¬†¬†¬†¬†¬†¬† –Я–µ—А–Є—В–Њ–љ–µ–∞–ї—М–љ–∞—П —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–∞ –Љ–Њ–ґ–µ—В –њ–Њ—П–≤–ї—П—В—М—Б—П –≤ –њ–µ—А–≤—Л–µ —З–∞—Б—Л –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ—А–Є —Д–µ—А–Љ–µ–љ—В–∞—В–Є–≤–љ–Њ–Љ –њ–µ—А–Є—В–Њ–љ–Є—В–µ
¬Ј¬†¬†¬†¬†¬†¬†¬† –Я—А–Є –њ–Њ–Ј–і–љ–µ–Љ –Њ–±—А–∞—Й–µ–љ–Є–Є вАУ –њ–∞–ї—М–њ–Є—А—Г–µ–Љ—Л–є –Є–љ—Д–Є–ї—М—В—А–∞—В –≤ –≤–µ—А—Е–љ–Є—Е –Њ—В–і–µ–ї–∞—Е –ґ–Є–≤–Њ—В–∞
–≠—Е–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є–µ —Д–µ–љ–Њ–Љ–µ–љ—Л. –Ґ—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Њ—Б—В—А–Њ–≥–Њ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–∞ —Б–Њ—Б—В–Њ–Є—В –Є–Ј –≤—Л—П–≤–ї–µ–љ–Є—П –њ—А—П–Љ—Л—Е –Є –Ї–Њ—Б–≤–µ–љ–љ—Л—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л. –Т—Б–µ –ґ–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –њ—А–Є –Љ–љ–Њ–≥–Њ–Њ–±—А–∞–Ј–Є–Є —Б–Њ–љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –љ–Є –Њ–і–Є–љ –Є–Ј –љ–Є—Е –љ–µ —П–≤–ї—П–µ—В—Б—П —Г–Ј–Ї–Њ—Б–њ–µ—Ж–Є—Д–Є—З–љ—Л–Љ —В–Њ–ї—М–Ї–Њ –і–ї—П –і–∞–љ–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Ш–љ—В–µ—А–њ—А–µ—В–∞—Ж–Є—П –љ–µ –і–Њ–ї–ґ–љ–∞ –±—Л—В—М –Њ–і–љ–Њ–Ј–љ–∞—З–љ–Њ–є, –∞ –Њ—Ж–µ–љ–Ї—Г —Б–ї–µ–і—Г–µ—В –њ—А–Њ–≤–Њ–і–Є—В—М –≤–Њ –≤—Б–µ–є –Є—Е —Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В–Є —Б —Г—З–µ—В–Њ–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П.
¬Ј¬†¬†¬†¬†¬†¬†¬† –£–≤–µ–ї–Є—З–µ–љ–Є–µ —А–∞–Ј–Љ–µ—А–Њ–≤ –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л —Б –њ—А–µ–≤—Л—И–µ–љ–Є–µ–Љ –њ–µ—А–µ–і–љ–µ–Ј–∞–і–љ–µ–≥–Њ —А–∞–Ј–Љ–µ—А–∞ –≥–Њ–ї–Њ–≤–Ї–Є –Є —В–µ–ї–∞ –±–Њ–ї–µ–µ 3 —Б–Љ, —Е–≤–Њ—Б—В–∞ вАУ –±–Њ–ї–µ–µ 2,5 —Б–Љ¬†
¬Ј¬†¬†¬†¬†¬†¬†¬† –Ъ–Њ–љ—В—Г—А –ґ–µ–ї–µ–Ј—Л –љ–µ—З–µ—В–Ї–Є–є, —В–Ї–∞–љ–µ–≤–∞—П —Б—В—А—Г–Ї—В—Г—А–∞ –≤—Л–≥–ї—П–і–Є—В ¬Ђ—А–∞–Ј–Љ—Л—В–Њ–є¬ї, –њ–ї–Њ—Е–Њ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А—Г—О—В—Б—П —Б–Є–љ—Г—Б –≤–Њ—А–Њ—В–љ–Њ–є –≤–µ–љ—Л –Є —Б–µ–ї–µ–Ј–µ–љ–Њ—З–љ–∞—П –≤–µ–љ–∞ (–†–Є—Б. 5)
¬Ј¬†¬†¬†¬†¬†¬†¬† –Э–µ–Њ–і–љ–Њ—А–Њ–і–љ–Њ—Б—В—М —Б—В—А—Г–Ї—В—Г—А—Л –Њ—А–≥–∞–љ–∞ —Б –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ –≥–Є–њ–Њ—Н—Е–Њ–≥–µ–љ–љ—Л—Е –Њ—З–∞–≥–Њ–≤ —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ —А–∞–Ј–Љ–µ—А–∞ –Є —Д–Њ—А–Љ—Л
¬Ј¬†¬†¬†¬†¬†¬†¬† –£—Б–Є–ї–µ–љ–Є–µ –Њ—А–≥–∞–љ–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞, –≤—Л—П–≤–ї—П–µ–Љ–Њ–µ –њ—А–Є —Ж–≤–µ—В–љ–Њ–є –Є –Њ—Б–Њ–±–µ–љ–љ–Њ —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–є –і–Њ–њ–њ–ї–µ—А–Њ–≥—А–∞—Д–Є–Є
¬Ј¬†¬†¬†¬†¬†¬†¬† –£–≤–µ–ї–Є—З–µ–љ–Є–µ —А–∞–Ј–Љ–µ—А–Њ–≤ –Ї–ї–µ—В—З–∞—В–Њ—З–љ—Л—Е –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤, —Б–љ–Є–ґ–µ–љ–Є–µ —Н—Е–Њ–≥–µ–љ–љ–Њ—Б—В–Є –Ј–∞–±—А—О—И–Є–љ–љ–Њ–є –Ї–ї–µ—В—З–∞—В–Ї–Є, —Б–ї–Њ–Є—Б—В–Њ—Б—В—М –µ–µ —Б—В—А–Њ–µ–љ–Є—П
¬Ј¬†¬†¬†¬†¬†¬†¬† ¬†–≠—Е–Њ–љ–µ–≥–∞—В–Є–≤–љ—Л–µ —Б—В—А—Г–Ї—В—Г—А—Л –≤ –њ—А–Њ–µ–Ї—Ж–Є–Є —Б–∞–ї—М–љ–Є–Ї–Њ–≤–Њ–є —Б—Г–Љ–Ї–Є (–†–Є—Б. 6)
¬Ј¬†¬†¬†¬†¬†¬†¬† –°–≤–Њ–±–Њ–і–љ–∞—П –ґ–Є–і–Ї–Њ—Б—В—М –≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є, –њ–Њ—П–≤–ї—П—О—Й–∞—П—Б—П –≤ —А–∞–љ–љ–Є–µ —Б—А–Њ–Ї–Є –±–Њ–ї–µ–Ј–љ–Є –Є –љ–µ—А–µ–і–Ї–Њ –≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ (–†–Є—Б. 7)
¬Ј¬†¬†¬†¬†¬†¬†¬† –°–≤–Њ–±–Њ–і–љ–∞—П –ґ–Є–і–Ї–Њ—Б—В—М –≤ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є, –≤ –њ–Њ–і–∞–≤–ї—П—О—Й–µ–Љ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ —Б–ї–µ–≤–∞ (–†–Є—Б. 8)
¬Ј¬†¬†¬†¬†¬†¬†¬† –Э–∞–ї–Є—З–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –ґ–µ–ї—З–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є –њ–Њ —В–Є–њ—Г ¬Ђ–і–Є—Б—В–∞–ї—М–љ–Њ–≥–Њ¬ї –±–ї–Њ–Ї–∞ (—Г–≤–µ–ї–Є—З–µ–љ–Є–µ —А–∞–Ј–Љ–µ—А–Њ–≤ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П, –і–Є–ї–∞—В–∞—Ж–Є—П —Е–Њ–ї–µ–і–Њ—Е–∞). –Ъ–Њ–љ–Ї—А–µ–Љ–µ–љ—В—Л –≤ –ґ–µ–ї—З–љ–Њ–Љ –њ—Г–Ј—Л—А–µ –Љ–Њ–≥—Г—В —Б–ї—Г–ґ–Є—В—М –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ –≤ –њ–Њ–ї—М–Ј—Г –і–Є–∞–≥–љ–Њ–Ј–∞ –Њ—Б—В—А–Њ–≥–Њ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–∞ (–†–Є—Б. 9)
¬Ј¬†¬†¬†¬†¬†¬†¬† –†–∞–Ј–і—Г—В—Л–µ, –≤—П–ї–Њ –њ–µ—А–Є—Б—В–∞–ї—М—В–Є—А—Г—О—Й–Є–µ –њ–µ—В–ї–Є –Ї–Є—И–µ—З–љ–Є–Ї–∞, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ–Њ–њ–µ—А–µ—З–љ–Њ-–Њ–±–Њ–і–Њ—З–љ–∞—П –Ї–Є—И–Ї–∞. –Я–∞—А–µ–Ј –Ц–Ъ–Ґ —В–∞–Ї–ґ–µ –≤—Л—П–≤–ї—П–µ—В—Б—П —А–∞–љ–Њ.
–Ш–Ј –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л—Е —Н—Е–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Њ—Б—В—А–Њ–≥–Њ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–∞ –љ–∞–Є–±–Њ–ї–µ–µ –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ—Л, –њ–Њ –љ–∞—И–µ–Љ—Г –Љ–љ–µ–љ–Є—О, —Б–ї–µ–і—Г—О—Й–Є–µ: –≤—Л–њ–Њ—В –≤ —Б–∞–ї—М–љ–Є–Ї–Њ–≤–Њ–є —Б—Г–Љ–Ї–µ, –ї–µ–≤–Њ—Б—В–Њ—А–Њ–љ–љ–Є–є –≤—Л–њ–Њ—В –≤ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –Є –њ—А–Є–Ј–љ–∞–Ї–Є –ґ–µ–ї—З–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є –њ–Њ —В–Є–њ—Г –і–Є—Б—В–∞–ї—М–љ–Њ–≥–Њ –±–ї–Њ–Ї–∞. –Ю—В–Љ–µ—В–Є–Љ —В–∞–Ї–ґ–µ –њ–Њ—П–≤–ї–µ–љ–Є–µ –≤ —А–∞–љ–љ–Є–µ —Б—А–Њ–Ї–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ –≤—Л–њ–Њ—В–∞ –≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –њ–∞—А–µ–Ј–∞ –њ–Њ–њ–µ—А–µ—З–љ–Њ-–Њ–±–Њ–і–Њ—З–љ–Њ–є –Ї–Є—И–Ї–Є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –∞–Ї–Ї—Г—А–∞—В–љ—Л–є –∞–љ–∞–ї–Є–Ј –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –±–Њ–ї–µ–Ј–љ–Є –Є –∞–љ–∞–Љ–љ–µ–Ј–∞ –≤ —Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В–Є —Б —Ж–µ–ї–µ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л–Љ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –њ–Њ–Ј–≤–Њ–ї–Є—В –њ–Њ—Б—В–∞–≤–Є—В—М –њ—А–∞–≤–Є–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј. –Ю–±–∞ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ–Љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Њ—В–љ–Њ—Б—П—В—Б—П –Ї —Г—А–≥–µ–љ—В–љ–Њ–є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є. –Я—А–Є –Љ–µ–Ј–µ–љ—В–µ—А–Є–∞–ї—М–љ–Њ–Љ —В—А–Њ–Љ–±–Њ–Ј–µ, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г—Б—В—М—П –Т–С–Р вАУ –∞ —В–∞–Ї–Є—Е —Б–ї—Г—З–∞–µ–≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ, –Њ—В—Б—А–Њ—З–Ї–∞ –і–Є–∞–≥–љ–Њ–Ј–∞ –Њ–Ј–љ–∞—З–∞–µ—В –љ–µ–Љ–Є–љ—Г–µ–Љ—Г—О –≥–Є–±–µ–ї—М –њ–∞—Ж–Є–µ–љ—В–∞ –Њ—В —А–∞–Ј–≤–Є–≤—И–µ–≥–Њ—Б—П —Б—Г–±—В–Њ—В–∞–ї—М–љ–Њ–≥–Њ –љ–µ–Ї—А–Њ–Ј–∞ –Ї–Є—И–µ—З–љ–Є–Ї–∞. –Ы–∞–њ–∞—А–Њ—В–Њ–Љ–Є—П –њ—А–Є –њ–∞–љ–Ї—А–µ–Њ–љ–µ–Ї—А–Њ–Ј–µ, –≤—Л–њ–Њ–ї–љ–µ–љ–љ–∞—П –≤ –њ–µ—А–≤—Л–µ —З–∞—Б—Л –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г—Е—Г–і—И–∞–µ—В –њ—А–Њ–≥–љ–Њ–Ј –ґ–Є–Ј–љ–Є –і–ї—П –±–Њ–ї—М–љ–Њ–≥–Њ . –° –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л, —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –њ–∞–љ–Ї—А–µ–Њ–љ–µ–Ї—А–Њ–Ј–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ —А–∞–љ–Њ –љ–∞—З–∞—В—М –≤–µ—Б—М –Ї–Њ–Љ–њ–ї–µ–Ї—Б –Є–љ—В–µ–љ—Б–Є–≤–љ—Л—Е –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ—Л—Е –Љ–µ—А–Њ–њ—А–Є—П—В–Є–є, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л—Е –љ–∞ –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–µ –Ј–Њ–љ—Л –љ–µ–Ї—А–Њ–Ј–∞ –Є –њ—А–µ—А—Л–≤–∞–љ–Є–µ –Ї–∞—Б–Ї–∞–і–∞ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Є—Б—В–µ–Љ–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є. –Ф–∞–љ–љ—Л–µ –Љ–љ–Њ–≥–Є—Е –∞–≤—В–Њ—А–Њ–≤ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ —В–Њ–Љ, —З—В–Њ –Є–Љ–µ–љ–љ–Њ —В–∞–Ї–Њ–є –њ–Њ–і—Е–Њ–і –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б–љ–Є–Ј–Є—В—М –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М –Њ—В —В—П–ґ–µ–ї—Л—Е —Д–Њ—А–Љ –Њ—Б—В—А–Њ–≥–Њ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–∞].
–°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –£–Ч-–і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–µ —Б–Є—Б—В–µ–Љ—Л –њ–Њ–Ј–≤–Њ–ї—П—О—В –њ–Њ–ї—Г—З–Є—В—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–є –Њ–±—К–µ–Љ –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є –Њ –Є–Ј–Љ–µ–љ–µ–љ–Є—П—Е, –њ—А–Њ–Є—Б—Е–Њ–і—П—Й–Є—Е –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –њ—А–Є —В–Њ–є –Є–ї–Є –Є–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є. –Т —Б–ї–Њ–ґ–љ—Л—Е —Б–ї—Г—З–∞—П—Е –љ–∞—А—П–і—Г —Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ —Б—Г–ґ–і–µ–љ–Є–µ–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –≤—Б–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є. –Т –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є –Њ–і–љ–Њ–є –Є–Ј —В–∞–Ї–Њ–≤—Л—Е —П–≤–ї—П–µ—В—Б—П –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–∞—П —В–Њ–љ–Ї–Њ–Є–≥–Њ–ї—М–љ–∞—П –њ—Г–љ–Ї—Ж–Є—П –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є. –Я—А–Є–≤–Њ–і–Є–Љ –і–≤–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–Љ–µ—А–∞, –љ–∞–≥–ї—П–і–љ–Њ –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є—Е –і–Њ—Б—В–Њ–Є–љ—Б—В–≤–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –і–∞–љ–љ–Њ–є –Љ–µ—В–Њ–і–Є–Ї–Є.
–С–Њ–ї—М–љ–Њ–є –І., 60 –ї–µ—В –љ–∞–њ—А–∞–≤–ї–µ–љ –≤ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–µ –Њ—В–і–µ–ї–µ–љ–Є–µ –Њ–±–ї–∞—Б—В–љ–Њ–є –њ—Б–Є—Е–Є–∞—В—А–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї—М–љ–Є—Ж–µ–є 28.04.2010 —Б –њ–Њ–і–Њ–Ј—А–µ–љ–Є–µ–Љ –љ–∞ –∞–±—Б—Ж–µ—Б—Б –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є. –£—В–Њ—З–љ–Є—В—М —Е–∞—А–∞–Ї—В–µ—А –ґ–∞–ї–Њ–± –Є –∞–љ–∞–Љ–љ–µ–Ј —Г —Б–∞–Љ–Њ–≥–Њ –±–Њ–ї—М–љ–Њ–≥–Њ –љ–µ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ –Є–Ј-–Ј–∞ –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞. –°–Њ —Б–ї–Њ–≤ –ї–µ—З–∞—Й–µ–≥–Њ –≤—А–∞—З–∞, –≤ —В–µ—З–µ–љ–Є–µ –њ–Њ—Б–ї–µ–і–љ–µ–є –љ–µ–і–µ–ї–Є –Њ—В–Љ–µ—З–µ–љ–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —А–∞–Ј–Љ–µ—А–Њ–≤ –ґ–Є–≤–Њ—В–∞, –±–Њ–ї–µ–Ј–љ–µ–љ–љ–Њ—Б—В—М –њ—А–Є –њ–∞–ї—М–њ–∞—Ж–Є–Є –≤ –≤–µ—А—Е–љ–Є—Е –Њ—В–і–µ–ї–∞—Е, –њ–Њ–≤—Л—И–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞ –і–Њ —Д–µ–±—А–Є–ї—М–љ—Л—Е —Ж–Є—Д—А, –њ–µ—А–Є–Њ–і–Є—З–µ—Б–Ї–Є вАУ —А–≤–Њ—В–∞. –Я—А–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є —Б–Њ—Б—В–Њ—П–љ–Є–µ —В—П–ґ–µ–ї–Њ–µ, –±–Њ–ї—М–љ–Њ–є –≤—П–ї—Л–є, –Ј–∞—В–Њ—А–Љ–Њ–ґ–µ–љ. –Ґ–µ–Љ–њ–µ—А–∞—В—Г—А–∞ —В–µ–ї–∞ 37,50 –°. –Ъ–Њ–ґ–љ—Л–µ –њ–Њ–Ї—А–Њ–≤—Л —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Њ–Ї—А–∞—Б–Ї–Є, —П–Ј—Л–Ї —Б—Г—Е–Њ–є. –Ф—Л—Е–∞–љ–Є–µ –≤–µ–Ј–Є–Ї—Г–ї—П—А–љ–Њ–µ, —Б–Є–Љ–Љ–µ—В—А–Є—З–љ–Њ–µ, –Њ–і—Л—И–Ї–Є –љ–µ—В. –Я—Г–ї—М—Б 96¬† —Г–і–∞—А–Њ–≤ –≤ –Љ–Є–љ—Г—В—Г, —А–Є—В–Љ–Є—З–љ—Л–є, —Б–ї–∞–±–Њ–≥–Њ –љ–∞–њ–Њ–ї–љ–µ–љ–Є—П. –Р–Ф 100\60 –Љ–Љ —А—В. —Б—В. –Ґ–Њ–љ—Л —Б–µ—А–і—Ж–∞ –њ—А–Є–≥–ї—Г—И–µ–љ—Л. –Ц–Є–≤–Њ—В —Г–≤–µ–ї–Є—З–µ–љ –≤ —А–∞–Ј–Љ–µ—А–∞—Е, –∞—Б–Є–Љ–Љ–µ—В—А–Є—З–µ–љ –Ј–∞ —Б—З–µ—В –≤–µ—А—Е–љ–Є—Е –Њ—В–і–µ–ї–Њ–≤, –≥–і–µ –њ—А–Є –њ–∞–ї—М–њ–∞—Ж–Є–Є –≤ –њ—А–Њ–µ–Ї—Ж–Є–Є –ґ–µ–ї—Г–і–Ї–∞ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ —В—Г–≥–Њ—Н–ї–∞—Б—В–Є—З–µ—Б–Ї–Њ–є –Ї–Њ–љ—Б–Є—Б—В–µ–љ—Ж–Є–Є –і–Њ 20 —Б–Љ –≤ –і–Є–∞–Љ–µ—В—А–µ. –°–Є–Љ–њ—В–Њ–Љ–Њ–≤ —А–∞–Ј–і—А–∞–ґ–µ–љ–Є—П –±—А—О—И–Є–љ—Л –љ–µ—В. –Ы–µ–є–Ї–Њ—Ж–Є—В–Њ–Ј 8,2—Е109\–ї, –і–Є–∞—Б—В–∞–Ј–∞ 64 –Х–Ф. –£–Ч–Ш –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є: —Г–Љ–µ—А–µ–љ–љ–∞—П –≥–µ–њ–∞—В–Њ–Љ–µ–≥–∞–ї–Є—П, –њ—А–Є–Ј–љ–∞–Ї–Є –ґ–Є—А–Њ–≤–Њ–≥–Њ –≥–µ–њ–∞—В–Њ–Ј–∞. –Я–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–∞—П –ґ–µ–ї–µ–Ј–∞ –љ–µ –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А—Г–µ—В—Б—П. –Т –µ–µ –њ—А–Њ–µ–Ї—Ж–Є–Є –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –ґ–Є–і–Ї–Њ—Б—В–љ–Њ–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ 17—Е15 —Б–Љ —Б —В–Њ–ї—Б—В–Њ–є, –љ–µ—А–Њ–≤–љ–Њ–є, –Љ–µ—Б—В–∞–Љ–Є ¬Ђ–≥–Њ—Д—А–Є—А–Њ–≤–∞–љ–љ–Њ–є¬ї —Б—В–µ–љ–Ї–Њ–є, –≤ –њ—А–Њ—Б–≤–µ—В–µ вАУ –Ї–Њ–ї–µ–±–ї—О—Й–∞—П—Б—П –Љ–µ–ї–Ї–Њ–Ј–µ—А–љ–Є—Б—В–∞—П –≤–Ј–≤–µ—Б—М. –Ц–Є–і–Ї–Њ—Б—В–љ–∞—П —Б—В—А—Г–Ї—В—Г—А–∞ –њ—А–Є–ї–µ–ґ–Є—В –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –Ї –±—А—О—И–љ–Њ–є —Б—В–µ–љ–Ї–µ. –Ц–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М –Є –ґ–µ–ї—З–µ–≤—Л–≤–Њ–і—П—Й–Є–µ –њ—Г—В–Є вАУ –±–µ–Ј –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є. –Я–Њ—Б–ї–µ –њ–Њ—Б—В–∞–љ–Њ–≤–Ї–Є –љ–∞–Ј–Њ–≥–∞—Б—В—А–∞–ї—М–љ–Њ–≥–Њ –Ј–Њ–љ–і–∞ –Є —Н–≤–∞–Ї—Г–∞—Ж–Є–Є 600 –Љ–ї –Ј–∞—Б—В–Њ–є–љ–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–љ–Њ–≥–Њ –Њ—В–і–µ–ї—П–µ–Љ–Њ–≥–Њ —Н—Е–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–∞—П –Ї–∞—А—В–Є–љ–∞ –±–µ–Ј –Є–Ј–Љ–µ–љ–µ–љ–Є–є. –†–∞–±–Њ—З–Є–є –і–Є–∞–≥–љ–Њ–Ј вАУ –њ—Б–µ–≤–і–Њ–Ї–Є—Б—В–∞ –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –±–Њ–ї—М—И–Є—Е —А–∞–Ј–Љ–µ—А–Њ–≤. –Я–Њ–і –£–Ч-–љ–∞–≤–µ–і–µ–љ–Є–µ–Љ, —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Љ–µ—Б—В–љ–Њ–є –∞–љ–µ—Б—В–µ–Ј–Є–Є –≤—Л–њ–Њ–ї–љ–µ–љ–∞ —В–Њ–љ–Ї–Њ–Є–≥–Њ–ї—М–љ–∞—П –њ—Г–љ–Ї—Ж–Є—П –ґ–Є–і–Ї–Њ—Б—В–љ–Њ–≥–Њ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П вАУ –њ–Њ–ї—Г—З–µ–љ–∞ —Е–∞—А–∞–Ї—В–µ—А–љ–∞—П –і–ї—П –њ–Њ—Б—В–љ–µ–Ї—А–Њ—В–Є—З–µ—Б–Ї–Є—Е –Ї–Є—Б—В –±—Г—А–∞—П –ґ–Є–і–Ї–Њ—Б—В—М. –Р–Ї—В–Є–≤–љ–Њ—Б—В—М –і–Є–∞—Б—В–∞–Ј—Л –≤ –љ–µ–є –љ–µ–≤—Л—Б–Њ–Ї–∞—П. –Я—А–Њ–Є–Ј–≤–µ–і–µ–љ–Њ –Љ–∞–ї–Њ–Є–љ–≤–∞–Ј–Є–≤–љ–Њ–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–Њ - –љ–∞—А—Г–ґ–љ–Њ–µ –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є–µ –Ї–Є—Б—В—Л —И–Є—А–Њ–Ї–Њ–њ—А–Њ—Б–≤–µ—В–љ—Л–Љ –і—А–µ–љ–∞–ґ–Њ–Љ –њ–Њ–і –£–Ч-–Ї–Њ–љ—В—А–Њ–ї–µ–Љ. –Т –і–∞–љ–љ–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є —В–Њ–љ–Ї–Њ–Є–≥–Њ–ї—М–љ–∞—П –њ—Г–љ–Ї—Ж–Є—П –њ–Њ–Ј–≤–Њ–ї–Є–ї–∞ –љ–µ —В–Њ–ї—М–Ї–Њ –≤–µ—А–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М –і–Є–∞–≥–љ–Њ–Ј, –љ–Њ –Є –Є–Ј–±–µ–ґ–∞—В—М –Њ—В–Ї—А—Л—В–Њ–≥–Њ, –±–Њ–ї–µ–µ —В—А–∞–≤–Љ–∞—В–Є—З–љ–Њ–≥–Њ¬† —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ —Г —В—П–ґ–µ–ї–Њ–≥–Њ –±–Њ–ї—М–љ–Њ–≥–Њ.
–С–Њ–ї—М–љ–∞—П –°., 89 –ї–µ—В –і–Њ—Б—В–∞–≤–ї–µ–љ–∞ –≤ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–µ –Њ—В–і–µ–ї–µ–љ–Є–µ –±—А–Є–≥–∞–і–Њ–є —Б–Ї–Њ—А–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й–Є —Б –њ–Њ–і–Њ–Ј—А–µ–љ–Є–µ–Љ –љ–∞ –Ї–Є—И–µ—З–љ—Г—О –љ–µ–њ—А–Њ—Е–Њ–і–Є–Љ–Њ—Б—В—М. –Я—А–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є –ґ–∞–ї–Њ–±—Л –љ–∞ –±–Њ–ї–Є –≤ –ґ–Є–≤–Њ—В–µ –±–µ–Ј —З–µ—В–Ї–Њ–є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є, —В–Њ—И–љ–Њ—В—Г, —Б—Г—Е–Њ—Б—В—М –≤–Њ —А—В—Г. –С–Њ–ї—М–љ–∞ –Њ–Ї–Њ–ї–Њ 5 –і–љ–µ–є. –Ю–±—Й–µ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ —В—П–ґ–µ–ї–Њ–µ, –≤—П–ї–∞—П, –љ–∞ –≤–Њ–њ—А–Њ—Б—Л –Њ—В–≤–µ—З–∞–µ—В –њ–Њ—Б–ї–µ –Љ–љ–Њ–≥–Њ–Ї—А–∞—В–љ–Њ–≥–Њ –њ–Њ–≤—В–Њ—А–µ–љ–Є—П. –Ґ–µ–Љ–њ–µ—А–∞—В—Г—А–∞ —В–µ–ї–∞ 36,90 –°. –Ъ–Њ–ґ–љ—Л–µ –њ–Њ–Ї—А–Њ–≤—Л –±–ї–µ–і–љ–Њ–≤–∞—В—Л–µ, —Б–Ї–ї–µ—А—Л —Б—Г–±–Є–Ї—В–µ—А–Є—З–љ—Л. –ѓ–Ј—Л–Ї —Б—Г—Е–Њ–є. –Ф—Л—Е–∞–љ–Є–µ –ґ–µ—Б—В–Ї–Њ–≤–∞—В–Њ–µ, –Њ—Б–ї–∞–±–ї–µ–љ–Њ –≤ –Ј–∞–і–љ–µ–љ–Є–ґ–љ–Є—Е –Њ—В–і–µ–ї–∞—Е, –Њ–і—Л—И–Ї–∞ –і–Њ 26 –≤ –Љ–Є–љ—Г—В—Г. –Ґ–Њ–љ—Л —Б–µ—А–і—Ж–∞ –≥–ї—Г—Е–Є–µ, –∞—А–Є—В–Љ–Є—З–љ—Л–µ, 110 —Г–і–∞—А–Њ–≤ –≤ –Љ–Є–љ—Г—В—Г, –і–µ—Д–Є—Ж–Є—В –њ—Г–ї—М—Б–∞ 14 —Г–і–∞—А–Њ–≤. –Р–Ф 110\70 –Љ–Љ —А—В. —Б—В. –Ц–Є–≤–Њ—В —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ –≤–Ј–і—Г—В, –Љ—П–≥–Ї–Є–є, –±–Њ–ї–µ–Ј–љ–µ–љ–љ—Л–є –≤–Њ –≤—Б–µ—Е –Њ—В–і–µ–ї–∞—Е, –љ–Њ –±–Њ–ї—М—И–µ –њ–Њ –њ—А–∞–≤–Њ–Љ—Г —Д–ї–∞–љ–≥—Г. –°–Є–Љ–њ—В–Њ–Љ –©–µ—В–Ї–Є–љ–∞ вАУ –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–є. –Ы–µ–є–Ї–Њ—Ж–Є—В–Њ–Ј 10,59\–ї, –і–Є–∞—Б—В–∞–Ј–∞ –Љ–Њ—З–Є 32 –Х–Ф, –ґ–µ–ї—З–љ—Л–µ –њ–Є–≥–Љ–µ–љ—В—Л —Б–ї–∞–±–Њ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ. –†–µ–љ—В–≥–µ–љ–Њ–≥—А–∞—Д–Є—П –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є вАУ –∞—Н—А–Њ–Ї–Њ–ї–Є—П, —З–∞—И –Ъ–ї–Њ–є–±–µ—А–∞ –љ–µ—В. –†–µ–љ—В–≥–µ–љ–Њ–≥—А–∞—Д–Є—П –≥—А—Г–і–љ–Њ–є –Ї–ї–µ—В–Ї–Є вАУ –Є–љ—Д–Є–ї—М—В—А–∞—В–Є–≤–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –љ–µ—В. –£–Ч–Ш –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є: –≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –љ–µ–±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Б–≤–Њ–±–Њ–і–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є. –£–Љ–µ—А–µ–љ–љ–Њ –≤—Л—А–∞–ґ–µ–љ–љ—Л–µ –і–Є—Д—Д—Г–Ј–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –њ–µ—З–µ–љ–Є, –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л, –њ—А–Є–Ј–љ–∞–Ї–Є –Ј–∞—Б—В–Њ—П –њ–Њ –±–Њ–ї—М—И–Њ–Љ—Г –Ї—А—Г–≥—Г –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П. –Ц–µ–ї—З–љ—Л–є –њ—Г–Ј—Л—А—М 92—Е31 –Љ–Љ, —Б—В–µ–љ–Ї–∞ 3,5 –Љ–Љ, –≤ –њ—А–Њ—Б–≤–µ—В–µ —А–∞–Ј–љ–Њ–Ї–∞–ї–Є–±–µ—А–љ—Л–µ –Ї–Њ–љ–Ї—А–µ–Љ–µ–љ—В—Л. –•–Њ–ї–µ–і–Њ—Е 5 –Љ–Љ. –Ь–µ–Ј–µ–љ—В–µ—А–Є–∞–ї—М–љ—Л–є –Ї—А–Њ–≤–Њ—В–Њ–Ї –Њ—В—З–µ—В–ї–Є–≤—Л–є. –Ь–µ–і–Є–∞–ї—М–љ–µ–µ –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Є –≤—Л—И–µ –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –ї–Њ—Ж–Є—А—Г–µ—В—Б—П –ґ–Є–і–Ї–Њ—Б—В–љ–Њ–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –±–Њ–ї–µ–µ 15 —Б–Љ –≤ –і–Є–∞–Љ–µ—В—А–µ —Б —Н—Е–Њ–≥–µ–љ–љ—Л–Љ–Є –≤–Ї–ї—О—З–µ–љ–Є—П–Љ–Є, —Б—В–µ–љ–Ї–∞ –µ–≥–Њ —З–µ—В–Ї–Њ –љ–µ –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А—Г–µ—В—Б—П. –Я—А–Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є–Є —В–µ—А–Љ–Њ–≥—А–∞—Д–Є–Є –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –ї–Њ–Ї–∞–ї—М–љ–∞—П —В–µ–Љ–њ–µ—А–∞—В—Г—А–∞ –љ–∞–і –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –Њ—З–∞–≥–Њ–Љ –њ–Њ–≤—Л—И–µ–љ–∞ –љ–∞ 10C.¬† –Ф–Є–∞–≥–љ–Њ–Ј –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–ї–Є –Љ–µ–ґ–і—Г –і–µ—Б—В—А—Г–Ї—В–Є–≤–љ—Л–Љ —Е–Њ–ї–µ—Ж–Є—Б—В–Є—В–Њ–Љ –Є –Њ—Б—В—А—Л–Љ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–Њ–Љ —В—П–ґ–µ–ї–Њ–≥–Њ —В–µ—З–µ–љ–Є—П —Б —Д–Њ—А–Љ–Є—А—Г—О—Й–Є–Љ—Б—П –Њ—Б—В—А—Л–Љ –њ–∞–љ–Ї—А–µ–∞—В–Њ–≥–µ–љ–љ—Л–Љ —Б–Ї–Њ–њ–ї–µ–љ–Є–µ–Љ –ґ–Є–і–Ї–Њ—Б—В–Є. –Я–Њ–і –£–Ч-–Ї–Њ–љ—В—А–Њ–ї–µ–Љ —З–µ—А–µ–Ј –љ–∞–Ј–Њ–≥–∞—Б—В—А–∞–ї—М–љ—Л–є –Ј–Њ–љ–і –≤–≤–µ–і–µ–љ–∞ –ґ–Є–і–Ї–Њ—Б—В—М, –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ —Б–Љ–µ—Й–µ–љ–љ—Л–є –Ї–∞—Г–і–∞–ї—М–љ–Њ –Њ—В –ґ–Є–і–Ї–Њ—Б—В–љ–Њ–≥–Њ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –ґ–µ–ї—Г–і–Њ–Ї; –ґ–Є–і–Ї–Њ—Б—В–љ–Њ–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–Њ –≤—Л—И–µ –Є –њ—А–Є–ї–µ–ґ–Є—В –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –Ї –±—А—О—И–љ–Њ–є —Б—В–µ–љ–Ї–µ. –Т—Л–њ–Њ–ї–љ–µ–љ–∞ —В–Њ–љ–Ї–Њ–Є–≥–Њ–ї—М–љ–∞—П –њ—Г–љ–Ї—Ж–Є—П вАУ –њ–Њ–ї—Г—З–µ–љ –≥–љ–Њ–є —Б —П–≤–љ–Њ–є –њ—А–Є–Љ–µ—Б—М—О –ґ–µ–ї—З–Є. –£—З–Є—В—Л–≤–∞—П –Ї—А–∞–є–љ–µ —В—П–ґ–µ–ї–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ –±–Њ–ї—М–љ–Њ–є, –≤—Л—А–∞–ґ–µ–љ–љ—Г—О —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й—Г—О –њ–∞—В–Њ–ї–Њ–≥–Є—О –≤—Л–±—А–∞–љ —Б–ї–µ–і—Г—О—Й–Є–є –Њ–±—К–µ–Љ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й–Є вАУ –≤—Б–Ї—А—Л—В–Є–µ, —Б–∞–љ–∞—Ж–Є—П, –і—А–µ–љ–Є—А–Њ–≤–∞–љ–Є–µ –∞–±—Б—Ж–µ—Б—Б–∞ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є, —Е–Њ–ї–µ—Ж–Є—Б—В–Њ—Б—В–Њ–Љ–Є—П. –Т –Њ–њ–Є—Б—Л–≤–∞–µ–Љ–Њ–Љ —Б–ї—Г—З–∞–µ –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–∞—П –њ—Г–љ–Ї—Ж–Є—П –Њ–і–љ–Њ–Ј–љ–∞—З–љ–Њ —А–µ—И–Є–ї–∞ –≤–Њ–њ—А–Њ—Б –≤—Л–±–Њ—А–∞ —В–∞–Ї—В–Є–Ї–Є –ї–µ—З–µ–љ–Є—П –≤ –њ–Њ–ї—М–Ј—Г –Њ–њ–µ—А–∞—Ж–Є–Є.
–Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —В–Њ–љ–Ї–Њ–Є–≥–Њ–ї—М–љ–∞—П –њ—Г–љ–Ї—Ж–Є—П –њ–Њ–і –£–Ч-–Ї–Њ–љ—В—А–Њ–ї–µ–Љ —В–µ—Е–љ–Є—З–µ—Б–Ї–Є –њ—А–Њ—Б—В–∞. –Я—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ–є –љ–∞—Б–∞–і–Ї–Є –Є –њ—Г–љ–Ї—Ж–Є–Њ–љ–љ–Њ–є –њ—А–Њ–≥—А–∞–Љ–Љ—Л –љ–∞ —Б–Ї–∞–љ–µ—А–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –≤—Л–њ–Њ–ї–љ–µ–љ–∞ –Љ–µ—В–Њ–і–Њ–Љ —Б–≤–Њ–±–Њ–і–љ–Њ–є —А—Г–Ї–Є. –Ь—Л –љ–µ –љ–∞–±–ї—О–і–∞–ї–Є –љ–Є –Њ–і–љ–Њ–≥–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –њ–Њ—Б–ї–µ –і–∞–љ–љ–Њ–є –њ—А–Њ—Ж–µ–і—Г—А—Л, –і–∞–ґ–µ –њ—А–Є –њ–Њ–њ–∞–і–∞–љ–Є–Є –Є–≥–ї—Л –≤ –њ—А–Њ—Б–≤–µ—В –њ–Њ–ї–Њ–≥–Њ –Њ—А–≥–∞–љ–∞.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ. –Э–∞ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ —Н—В–∞–њ–µ —А–∞–Ј–≤–Є—В–Є—П –Љ–µ–і–Є—Ж–Є–љ—Л –њ–Њ—Б—В–Њ—П–љ–љ–Њ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —Б–Њ–≤–µ—А—И–µ–љ—Б—В–≤–Њ–≤–∞–љ–Є–µ –Њ–±–Њ—А—Г–і–Њ–≤–∞–љ–Є—П, –њ—А–Є–Ј–≤–∞–љ–љ–Њ–≥–Њ –Њ–±–ї–µ–≥—З–Є—В—М –њ–Њ—Б—В–∞–љ–Њ–≤–Ї—Г –і–Є–∞–≥–љ–Њ–Ј–∞. –Ю–і–љ–∞–Ї–Њ —Б–ї–µ–њ–Њ–µ —Б—З–Є—В—Л–≤–∞–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є–є –њ—А–Є–±–Њ—А–Њ–≤, —А–∞—Б—З–µ—В —Ж–Є—Д—А –Є –Љ–Є–ї–ї–Є–Љ–µ—В—А–Њ–≤ –љ–µ–Є–Ј–±–µ–ґ–љ–Њ –Њ—В–і–∞–ї—П–µ—В –≤—А–∞—З–∞ –Њ—В –њ–∞—Ж–Є–µ–љ—В–∞, –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —З–µ–≥–Њ –≤—Л–≤–Њ–і—Л —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–∞ –≤ —А—П–і–µ —Б–ї—Г—З–∞–µ–≤ –Љ–Њ–≥—Г—В –Њ–Ї–∞–Ј–∞—В—М—Б—П —Д–Њ—А–Љ–∞–ї—М–љ—Л–Љ–Є –Є –љ–µ –њ–Њ–≤–ї–Є—П—В—М –љ–∞ —В–∞–Ї—В–Є–Ї—Г. –Т—А–∞—З—Г –£–Ч-–і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є, —А–∞–±–Њ—В–∞—О—Й–µ–Љ—Г –≤ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–Љ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ –љ–µ–Њ—В–ї–Њ–ґ–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є, –Њ—З–µ–љ—М –љ–µ–њ—А–Њ—Б—В–Њ —Б–і–µ–ї–∞—В—М —Б–≤–Њ–µ –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ, –Њ–њ–Є—А–∞—П—Б—М –ї–Є—И—М –љ–∞ –Ј–љ–∞—З–µ–љ–Є—П –љ–Њ—А–Љ—Л –Є —Б—В–∞–љ–і–∞—А—В–љ—Л–µ –Љ–µ—В–Њ–і–Є–Ї–Є –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Т–Њ –Љ–љ–Њ–≥–Є—Е —Б–ї—Г—З–∞—П—Е –Ј–∞ —Н—В–Є–Љ –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ–Љ —Б—В–Њ–Є—В —Б—Г–і—М–±–∞ –±–Њ–ї—М–љ–Њ–≥–Њ вАУ –Њ–њ–µ—А–Є—А–Њ–≤–∞—В—М –Є–ї–Є –ї–µ—З–Є—В—М –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ. –Т —Б–≤–µ—В–µ —Б–Ї–∞–Ј–∞–љ–љ–Њ–≥–Њ —Б—З–Є—В–∞–µ–Љ –Њ—З–µ–љ—М –≤–∞–ґ–љ—Л–Љ —Б–∞–Љ–Њ–µ —В–µ—Б–љ–Њ–µ —Б–Њ—В—А—Г–і–љ–Є—З–µ—Б—В–≤–Њ —Б —Е–Є—А—Г—А–≥–∞–Љ–Є, –≤–Ї–ї—О—З–∞—О—Й–µ–µ, –≤ —В–Њ–Љ —З–Є—Б–ї–µ, —Б–Њ–≤–Љ–µ—Б—В–љ—Л–є –Њ—Б–Љ–Њ—В—А —Б —Е–Є—А—Г—А–≥–Њ–Љ –њ—А–Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є–Є –£–Ч–Ш –Є –њ—А–Є—Б—Г—В—Б—В–≤–Є–µ —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–∞ –њ–Њ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –љ–∞ –Њ–њ–µ—А–∞—Ж–Є—П—Е.
1.–С–∞–≥–љ–µ–љ–Ї–Њ –°.–§., –У–Њ–ї—М—Ж–Њ–≤ –Т.–†. –Є –і—А. –Я—А–Є–љ—Ж–Є–њ—Л –ї—Г—З–µ–≤–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –≥–љ–Њ–є–љ–Њ-–љ–µ–Ї—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–∞—А–∞–њ–∞–љ–Ї—А–µ–∞—В–Є—В–∞. –Ґ–µ–Ј. –і–Њ–Ї–ї. 16 –Љ–µ–ґ–і. –Ї–Њ–љ–≥—А. —Е–Є—А—Г—А–≥–Њ–≤ - –≥–µ–њ–∞—В–Њ–ї–Њ–≥–Њ–≤. –Х–Ї–∞—В–µ—А–Є–љ–±—Г—А–≥ 2009: 54.
2.–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –њ–Њ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ. \ ¬†–Я–Њ–і —А–µ–і. –Ь–Є—В—М–Ї–Њ–≤–∞ –Т.–Т. –Ґ. 1. –Ь.: –Т–Є–і–∞—А, 1996. –°. 140-186.
3.Debus E.S., Diener H., Larena-Avellaneda A. Acute intestinal ischemia. Chirurg. 2009 Apr; 80(4): 375-85; quiz 386-7.
4.Ghisletta N., von Flue M., Eichlisberger E., Bruhwiler I., Ritz R., Harder F. Mesenteric venous thrombosis (MVT): a problem in diagnosis and manage-ment. Swiss Surg. 1996; 2(5): 223-9.
5.Lui G. A., Poniachik T. J., Quera P. R., Bermudez E. C. Mesenteric vein thrombosis: clinical manifestations, treatment and outcome. Rev Med Chil. 2005 Jan; 133(1): 17-22.
6.–Ъ—Г–љ—Ж–µ–≤–Є—З –У.–Ш., –®–Є–ї–µ–љ–Њ–Ї –Ф.–°. –Ю—Ж–µ–љ–Ї–∞ –Љ–µ—В–Њ–і–Њ–Љ –і—Г–њ–ї–µ–Ї—Б–љ–Њ–≥–Њ —Б–Ї–∞–љ–Є—А–Њ–≤–∞-–љ–Є—П –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ —З—А–µ–≤–љ–Њ–≥–Њ —Б—В–≤–Њ–ї–∞ –Є –≤–µ—А—Е–љ–µ–є –±—А—Л–ґ–µ–µ—З–љ–Њ–є –∞—А—В–µ—А–Є–Є —Г –Ј–і–Њ—А–Њ–≤—Л—Е –ї–Є—Ж. –•–Є—А—Г—А–≥–Є—П 1993; 7 –°. 48-51.
7.Perko M.J. Duplex ultrasound for assessment of superior mesenteric artery blood flow. Eur J Vasc Endovasc Surg. 2001 Feb; 21(2): 106-17.
8.Danse E.M., Kartheuser A., Paterson H.M., Laterre P.F. Color Doppler sonography of small bowel wall changes in 21 consecutive cases of acute mesenteric ischemia. JBR-BTR. 2009 Jul-Aug; 92(4): 202-6.
9.–°–∞–≤–µ–ї—М–µ–≤ –Т.–°., –У–µ–ї—М—Д–∞–љ–і –С.–†., –У–Њ–ї–Њ–≥–Њ—А—Б–Ї–Є–є –Т. –Р. –°–Є—Б—В–µ–Љ–љ–∞—П –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–∞—П —А–µ–∞–Ї—Ж–Є—П –Є —Б–µ–њ—Б–Є—Б –њ—А–Є –њ–∞–љ–Ї—А–µ–Њ–љ–µ–Ї—А–Њ–Ј–µ //–Р–љ–µ—Б—В–µ–Ј–Є–Њ–ї–Њ–≥–Є—П –Є —А–µ–∞–љ–Є–Љ–∞—В–Њ–ї–Њ–≥–Є—П. - 1999. - вДЦ6. - –°. 28-33.
10.Schneider L., Hartwig W., Flemming T., Hackert T., Fortunato F., Heck M., Gebhard M.M., Nawroth P.P., Bierhaus A., B—Мchler M.W., Werner J. Protective Effects and Anti-Inflammatory Pathways of Exogenous Calcitonin Gene-Related Peptide in Severe Necrotizing Pancreatitis. Pancreatology. 2009 Aug 14; 9(5): 662-669.
11.Vege S.S., Gardner T.B., Chari S.T., Munukuti P., Pearson R.K., Clain J.E., Petersen B.T., Baron T.H., Farnell M.B., Sarr M.G. Low mortality and high morbidity in severe acute pancreatitis without organ failure: a case for revising the Atlanta classification to include "moderately severe acute pancreatitis". Am J Gastroenterol. 2009 Mar; 104(3): 710-5.
12.–Ґ–Њ–ї—Б—В–Њ–є –Р.–Ф. –Ю—Б—В—А—Л–є –њ–∞–љ–Ї—А–µ–∞—В–Є—В. –Ґ—А—Г–і–љ–Њ—Б—В–Є, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є, –њ–µ—А—Б–њ–µ–Ї—В–Є–≤—Л. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –ї–µ–Ї—Ж–Є–Є ¬†/ ¬†–°-–Я–µ—В–µ—А–±—Г—А–≥. –Я—А–µ–і–њ—А–Є—П—В–Є–µ –°–Я–± –°–Њ—О–Ј–∞ —Е—Г–і–Њ–ґ–љ–Є–Ї–Њ–≤. 1997 –≥., - 140 —Б.
13.–С—Г—В–Ї–µ–≤–Є—З –Р.–¶., –І–∞–і–∞–µ–≤ –Р.–Я., –Ы–∞–њ–Є–љ –Р.–Ѓ., –°–≤–Є—А–Є–і–Њ–≤ –°.–Т. –Ю—В–Ї—А—Л—В—Л–µ –і—А–µ–љ–Є—А—Г—О—Й–Є–µ –Њ–њ–µ—А–∞—Ж–Є–Є –≤ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–Љ –ї–µ—З–µ–љ–Є–Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ–≥–Њ –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ–∞–љ–Ї—А–µ–Њ–љ–µ–Ї—А–Њ–Ј–∞. –Ь–Њ—Б–Ї–≤–∞. –У—А–∞–љ–Є—Ж–∞. 390 —Б.
14.–С—А—О—Е–Њ–≤–µ—Ж–Ї–Є–є –Ѓ.–Р. –Ч–љ–∞—З–µ–љ–Є–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–≥–Њ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ —Д–Њ—А–Љ –Њ—Б—В—А–Њ–≥–Њ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–∞: –Ф–Є—Б—Б. вА¶ –Ї–∞–љ–і. –Љ–µ–і. –љ–∞—Г–Ї. –Ь.: –†–Ь–Р–Я–Ю, 1998: 154.¬†
15.–С–ї–∞–≥–Њ–≤–µ—Б—В–љ–Њ–≤ –Ф.–Р., –•–≤–∞—В–Њ–≤ –Т.–С., –£–њ—Л—А–µ–≤ –Р.–Т., –У—А–Є—И–Є–љ –У.–Я., –Э–Њ–≤–Њ—Б–µ–ї –°.–Э. –Ъ–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –Њ—Б—В—А–Њ–≥–Њ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–∞ –Є –µ–≥–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є.–•–Є—А—Г—А–≥–Є—П ¬†2004; 5: 68-75.
16.–Р–≥–∞–µ–≤ –С.–Р., –Ф–ґ–∞—Д–∞—А–ї–Є –Ч.–Х. –Ъ–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –Њ—Б—В—А–Њ–≥–Њ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–∞. –•–Є—А—Г—А–≥–Є—П 2010; 4: 63-66.¬†
17.–Ъ—Г–Ј–љ–µ—Ж–Њ–≤ –Э.–Р. –Є –і—А. –≠–Ї—Б—В—А–∞–Ї–Њ—А–њ–Њ—А–∞–ї—М–љ–∞—П –і–µ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є—П —Г –±–Њ–ї—М–љ—Л—Е –і–µ—Б—В—А—Г–Ї—В–Є–≤–љ—Л–Љ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–Њ–Љ. –•–Є—А—Г—А–≥–Є—П 2005; 11: 32-36.
18.–С—А–Є—Б–Ї–Є–љ –С.–°. –Є –і—А. –≠–≤–Њ–ї—О—Ж–Є—П –≤–Ј–≥–ї—П–і–Њ–≤ –љ–∞ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ –Њ—Б—В—А–Њ–≥–Њ –і–µ—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –њ–∞–љ–Ї—А–µ–∞—В–Є—В–∞. –Т–µ—Б—В–љ –•–Є—А –Є–Љ. –Ш.–Ш.–У—А–µ–Ї–Њ–≤–∞ 2008; 167(6): 105-109.
19.Peter A. Banks. Practice Guidelines in Acute Pancreatitis. Am J Gastroenterol 2006; 101: 2379вАУ2400.
–Ф–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л—Е –Љ–µ—В–Њ–і–Є–Ї –≤ –Њ–љ–Ї–Њ—Г—А–Њ–ї–Њ–≥–Є–Є –Є –Њ–љ–Ї–Њ–≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є–Є.
- Details
- Category: –£–ї—М—В—А–∞–Ј–≤—Г–Ї –≤ —Е–Є—А—Г—А–≥–Є–Є
 
 |
    |
–Ф–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л—Е –Љ–µ—В–Њ–і–Є–Ї –≤ –Њ–љ–Ї–Њ—Г—А–Њ–ї–Њ–≥–Є–Є –Є –Њ–љ–Ї–Њ–≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є–Є.–С.–Р. –Ь–Є–љ—М–Ї–Њ.
–¶–Э–Ш —А–µ–љ—В–≥–µ–љ–Њ—А–∞–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –Є–љ—Б—В–Є—В—Г—В –Ь–Ч–°–† –†–§, –°–∞–љ–Ї—В-–Я–µ—В–µ—А–±—Г—А–≥, –†–Њ—Б—Б–Є—П |
 
–Т–≤–µ–і–µ–љ–Є–µ
 
–Ш–Ј–≤–µ—Б—В–љ—Л–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –£–Ч–Ш –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –і—А—Г–≥–Є–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є –ї—Г—З–µ–≤–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ —Б–≤—П–Ј–∞–љ—Л —Б –љ–µ–Є–љ–≤–∞–Ј–Є–≤–љ–Њ—Б—В—М—О, –±—Л—Б—В—А–Њ—В–Њ–є –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П, –±–µ–Ј–≤—А–µ–і–љ–Њ—Б—В—М—О –і–ї—П –Ј–і–Њ—А–Њ–≤—М—П –њ–∞—Ж–Є–µ–љ—В–∞. –Т—Л—Б–Њ–Ї–∞—П –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ–Њ—Б—В—М –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–Є–Ј–Ї–Њ–є —Б—В–Њ–Є–Љ–Њ—Б—В—М—О –њ–Њ–Ј–≤–Њ–ї–Є–ї–Є –Ј–∞–љ—П—В—М –µ–Љ—Г –Њ–і–љ–Њ –Є–Ј –≤–µ–і—Г—Й–Є—Е –Љ–µ—Б—В —Б—А–µ–і–Є –і—А—Г–≥–Є—Е –Љ–µ—В–Њ–і–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Я–Њ—Б–ї–µ–і–љ–Є–µ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –љ–∞—Г—З–љ–Њ-—В–µ—Е–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ–≥—А–µ—Б—Б–∞ –Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –Ї–Њ–Љ–њ—М—О—В–µ—А–љ—Л—Е —В–µ—Е–љ–Њ–ї–Њ–≥–Є–є –њ—А–Є–≤–µ–ї–Є –Ї —Б–Њ–Ј–і–∞–љ–Є—О –љ–Њ–≤–Њ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –£–Ч-–∞–њ–њ–∞—А–∞—В–Њ–≤, –Њ–±–ї–∞–і–∞—О—Й–Є—Е –≤—Л—Б–Њ–Ї–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О, —З—В–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —А–∞—Б—И–Є—А–Є–ї–Њ –Њ–±–ї–∞—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –£–Ч–Ш –≤ –Љ–µ–і–Є—Ж–Є–љ–µ –Є –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ –Є–Ј–Љ–µ–љ–Є–ї–Њ –њ–Њ–ї—Г—З–∞–µ–Љ—Г—О –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї—Г—О –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—О. –Т—Л—Б–Њ–Ї–Њ–µ –Ї–∞—З–µ—Б—В–≤–Њ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –±–ї–∞–≥–Њ–і–∞—А—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—О —Ж–Є—Д—А–Њ–≤–Њ–є —В–µ—Е–љ–Є–Ї–Є –і–ї—П –Њ–±—А–∞–±–Њ—В–Ї–Є –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –∞–Ї—Г—Б—В–Є—З–µ—Б–Ї–Є—Е —Б–Є–≥–љ–∞–ї–Њ–≤. –Т –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –њ—А–∞–Ї—В–Є–Ї—Г –≤–Њ—И–ї–Є –љ–Њ–≤—Л–µ —В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є –£–Ч–Ш: –љ–∞—В–Є–≤–љ–∞—П –Є –≤—В–Њ—А–∞—П –≥–∞—А–Љ–Њ–љ–Є–Ї–Є, –Ї–Њ–≥–µ—А–µ–љ—В–љ–Њ–µ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П, —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Є–є –і–Њ–њ–њ–ї–µ—А, –і–Њ–њ–њ–ї–µ—А–Њ–≤—Б–Ї–∞—П –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є—П —В–Ї–∞–љ–µ–є, —В—А–µ—Е–Љ–µ—А–љ–∞—П –Є –њ–∞–љ–Њ—А–∞–Љ–љ–∞—П —Н—Е–Њ–≥—А–∞—Д–Є–Є, —Н—Е–Њ–Ї–Њ–љ—В—А–∞—Б—В–љ–∞—П –∞–љ–≥–Є–Њ–≥—А–∞—Д–Є—П, —В—А–µ—Е–Љ–µ—А–љ—Л–µ —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–Є –≤ —А–µ–∞–ї—М–љ–Њ–Љ –≤—А–µ–Љ–µ–љ–Є. –Т—Б–µ –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л–µ –Є –і—А—Г–≥–Є–µ –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л–µ —Б–њ–Њ—Б–Њ–±—Л –њ–Њ–ї—Г—З–µ–љ–Є—П –£–Ч-–Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –≤–љ–Њ—Б—П—В —А–∞–Ј–ї–Є—З–љ—Л–є –≤–Ї–ї–∞–і –≤ —Г–ї—Г—З—И–µ–љ–Є–µ –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є —Б—В—А—Г–Ї—В—Г—А—Л –њ–∞—А–µ–љ—Е–Є–Љ–∞—В–Њ–Ј–љ—Л—Е –Є –њ–Њ–ї—Л—Е –Њ—А–≥–∞–љ–Њ–≤, —А–∞–Ј–ї–Є—З–љ—Л—Е —В–Ї–∞–љ–µ–є –Є —Б–Њ—Б—Г–і–Њ–≤. –Т—Л–і–µ–ї–µ–љ–Є–µ —Б–Њ—Б—Г–і–Њ–≤, –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П –Є—Е —Б—В–µ–љ–Ї–Є –Є –і–Њ–њ–њ–ї–µ—А–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–∞—П –Њ—Ж–µ–љ–Ї–∞ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –≤ –љ–Њ—А–Љ–µ –Є –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є—П—Е –Љ–Њ–ґ–µ—В –≤ —И–Є—А–Њ–Ї–Є—Е –њ—А–µ–і–µ–ї–∞—Е –љ–µ—Б—В–Є –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—О –Њ —Е–∞—А–∞–Ї—В–µ—А–µ –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є–Ї–Є –Њ—В–і–µ–ї—М–љ—Л—Е –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Є—Е –Њ–±–ї–∞—Б—В–µ–є.
 
–°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –Љ–љ–Њ–≥–Њ—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –£–Ч-–∞–њ–њ–∞—А–∞—В—Л –Њ–±–ї–∞–і–∞—О—В —Г–љ–Є–Ї–∞–ї—М–љ—Л–Љ–Є –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–Љ–Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—П–Љ–Є –Є –Љ–Њ–≥—Г—В –±—Л—В—М –њ–Њ–ї–љ–Њ—Ж–µ–љ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ—Л –њ—А–Є –≥–ї—Г–±–Њ–Ї–Њ–Љ –Ј–љ–∞–љ–Є–Є —В–µ–Њ—А–µ—В–Є—З–µ—Б–Ї–Є—Е –Њ—Б–љ–Њ–≤ –њ–Њ–ї—Г—З–µ–љ–Є—П –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П, –∞ —В–∞–Ї–ґ–µ –њ—А–Є —Г—В–Њ—З–љ–µ–љ–Є–Є –Њ–±–ї–∞—Б—В–µ–є –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П, –њ—А–µ–і–ї–∞–≥–∞–µ–Љ—Л—Е —А–∞–Ј—А–∞–±–Њ—В—З–Є–Ї–∞–Љ–Є –љ–Њ–≤—Л—Е —Н—Е–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е –Љ–µ—В–Њ–і–Є–Ї.
 
–Я–Њ–ї—Г—З–µ–љ–Є–µ —В—А–µ—Е–Љ–µ—А–љ—Л—Е —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—В–Є–≤–љ—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є —Б–Њ—Б—Г–і–Њ–≤, –≤—Л–Ј—Л–≤–∞–µ—В –±–Њ–ї—М—И–Њ–є –Є–љ—В–µ—А–µ—Б —Г –Ї–ї–Є–љ–Є—Ж–Є—Б—В–Њ–≤ –Є, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ, –Њ–љ–Ї–Њ–ї–Њ–≥–Њ–≤, —З—В–Њ —Г—Б–Ї–Њ—А—П–µ—В –Є—Е –≤–љ–µ–і—А–µ–љ–Є–µ –≤ –њ—А–∞–Ї—В–Є–Ї—Г. –Т–Њ—Б–њ—А–Є—П—В–Є–µ –Є –∞–љ–∞–ї–Є–Ј –Њ–±—К–µ–Љ–љ—Л—Е –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Є—Е —Б—В—А—Г–Ї—В—Г—А –љ–µ —Б—В–Њ–ї—М–Ї–Њ —Б–ї–Њ–ґ–љ—Л, –Ї–∞–Ї –љ–µ–њ—А–Є–≤—Л—З–љ—Л –і–ї—П –≤—А–∞—З–µ–є —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є. –≠—В–Њ –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –љ–Њ–≤—Л—Е –њ–Њ–і—Е–Њ–і–Њ–≤ –≤ –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є–Є –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –Є –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–≥–Њ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ –≤—А–∞—З–µ–±–љ–Њ–≥–Њ –љ–∞–≤—Л–Ї–∞, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–µ–≥–Њ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ–µ—А–µ–і–Њ–≤–Њ–є —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є —В–µ—Е–љ–Є–Ї–Є. –Я—А–Є —Н—В–Њ–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—З–Є—В—Л–≤–∞—В—М, —З—В–Њ –њ—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Њ–±—Й–µ–њ—А–Є–љ—П—В—Л–µ –≤ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –њ—А–Њ—Б–Љ–Њ—В—А –Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ—Л–є –∞–љ–∞–ї–Є–Ј –±–Њ–ї—М—И–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Н—Е–Њ—В–Њ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–Ј–Њ–≤ –≤ —А–µ–∞–ї—М–љ–Њ–Љ –≤—А–µ–Љ–µ–љ–Є –љ–µ –Љ–µ–љ–µ–µ —Г—В–Њ–Љ–Є—В–µ–ї–µ–љ, —З–µ–Љ –Є–Ј—Г—З–µ–љ–Є–µ –і–∞–љ–љ—Л—Е, –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –≤ –µ–і–Є–љ–Њ–Љ –±–ї–Њ–Ї–µ –Є–ї–Є —Б–µ—А–Є–Є —В–Њ–Љ–Њ–≥—А–∞–Љ–Љ –і—А—Г–≥–Њ–≥–Њ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Ж–Є—Д—А–Њ–≤—Л—Е –Ї–Њ–Љ–њ—М—О—В–µ—А–љ—Л—Е –њ—А–Њ–≥—А–∞–Љ–Љ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –њ–Њ–ї—Г—З–µ–љ–Є–µ —В—А–µ—Е–Љ–µ—А–љ—Л—Е —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤ —А–µ–∞–ї—М–љ–Њ–Љ –≤—А–µ–Љ–µ–љ–Є, –Ј–∞—В—А–∞—В–Є–≤ –љ–∞ –≤–µ—Б—М –њ—А–Њ—Ж–µ—Б—Б 20-30 —Б. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –љ–∞–Є–±–Њ–ї–µ–µ —И–Є—А–Њ–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –љ–Њ–≤—Л–µ —В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є –£–Ч–Ш –љ–∞—И–ї–Є –≤ –∞–Ї—Г—И–µ—А—Б—В–≤–µ.
 
–Ь–∞—В–µ—А–Є–∞–ї—Л –Є –Љ–µ—В–Њ–і—Л
 
–Я—А–Є –њ–Њ—Б—В—А–Њ–µ–љ–Є–Є —В—А–µ—Е–Љ–µ—А–љ—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є –њ—А–Є–Љ–µ–љ—П—О—В –ї–Є–±–Њ –∞–≤—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–є —Б–±–Њ—А –Њ–±—К–µ–Љ–љ–Њ–є –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ–≥–Њ —В—А–µ—Е–Љ–µ—А–љ–Њ–≥–Њ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –і–∞—В—З–Є–Ї–∞ –ї–Є–±–Њ –њ–Њ—Б—В—Г–њ–∞—В–µ–ї—М–љ–Њ–µ –њ–µ—А–µ–Љ–µ—Й–µ–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–Љ –Њ–±—Л—З–љ–Њ–≥–Њ –і–∞—В—З–Є–Ї–∞ —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–µ–є –Њ–±—К–µ–Љ–∞. –Ф–ї—П –Њ–±—А–∞–±–Њ—В–Ї–Є —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л—Е —В—А–µ—Е–Љ–µ—А–љ—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –∞–њ—А–Њ–±–Є—А–Њ–≤–∞–љ–љ—Л–µ –њ—А–Є –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є –Є –Љ–∞–≥–љ–Є—В–љ–Њ-—А–µ–Ј–Њ–љ–∞–љ—Б–љ–Њ–є —В–Њ–Љ–Њ–≥—А–∞—Д–Є–Є —В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є: –Љ–љ–Њ–≥–Њ–њ–ї–∞–љ–∞—А–љ–∞—П —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є—П (Multiplanar reconstruction, MPR), –њ—А–Њ–µ–Ї—Ж–Є—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є (MIP) –Є (MinIP), –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–∞—П —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є—П –Њ–±—К–µ–Ї—В–∞ (Surface shading rendering) –Є–ї–Є —В—А–µ—Е–Љ–µ—А–љ–∞—П —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є—П (3D volume rendering). –Ю—Б–Њ–±—Л–є –Є–љ—В–µ—А–µ—Б –≤ –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Д—Г–љ–Ї—Ж–Є–Є VOCALвДҐ, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є–µ –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В—М –≤–Є—А—В—Г–∞–ї—М–љ—Л–є –Њ—А–≥–∞–љ–Њ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є, –∞ —В–∞–Ї–ґ–µ —Д—Г–љ–Ї—Ж–Є–Є, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–Є–µ —В–Њ—З–љ–Њ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Њ–±—К–µ–Љ–Њ–≤.
 
–Я—А–Є –∞–љ–∞–ї–Є–Ј–µ –Њ—В–і–µ–ї—М–љ—Л—Е –Њ–±—К–µ–Ї—В–Њ–≤, –Є–Љ–µ—О—Й–Є—Е –±–Њ–ї—М—И—Г—О —А–∞–Ј–љ–Є—Ж—Г –∞–Ї—Г—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є—П, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ —В—А–µ—Е–Љ–µ—А–љ—Л–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –ї–µ–≥–Ї–Њ —Б–Њ–њ–Њ—Б—В–∞–≤–ї—П—В—М —Б –њ—А–Є–≤—Л—З–љ—Л–Љ–Є –і–≤—Г—Е–Љ–µ—А–љ—Л–Љ–Є, —В–∞–Ї –Ї–∞–Ї —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –Ї–Њ–Љ–њ—М—О—В–µ—А–љ—Л–µ —В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є –њ–Њ–Ј–≤–Њ–ї—П—О—В –≤–Ї–ї—О—З–∞—В—М –≤–Њ—Б–њ—А–Њ–Є–Ј–≤–µ–і–µ–љ–Є–µ –Њ–±—К–µ–Љ–∞ –Є —В–µ–љ–µ–≤–Њ–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–µ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є.
 
–Я–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л–є —А–µ–ґ–Є–Љ "Surface" –њ—А–µ–і–љ–∞–Ј–љ–∞—З–µ–љ –і–ї—П –Њ—В–Њ–±—А–∞–ґ–µ–љ–Є—П –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Њ–±—К–µ–Љ–љ–Њ–≥–Њ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П. –Т —Н—В–Є—Е —Б–ї—Г—З–∞—П—Е –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В –і–≤—Г—Е–Љ–µ—А–љ—Л–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –Є –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В –Є—Е —В—А–µ—Е–Љ–µ—А–љ—Г—О –∞–љ–∞—В–Њ–Љ–Є—О –њ–Њ–і –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ—Л–Љ —Г–≥–ї–Њ–Љ –њ—А–Њ–µ–Ї—Ж–Є–Є —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –≤–∞—А–Є–∞–љ—В–∞–Љ–Є –Њ—Б–≤–µ—Й–µ–љ–Є—П –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Є –≥–ї—Г–±–Є–љ—Л –≥–Є–њ–Њ—В–µ—В–Є—З–µ—Б–Ї–Є–Љ –Є—Б—В–Њ—З–љ–Є–Ї–Њ–Љ —Б–≤–µ—В–∞ –Є–ї–Є –≤—А–∞—Й–∞—В–µ–ї—М–љ–Њ–≥–Њ –і–≤–Є–ґ–µ–љ–Є—П –Є–Ј—Г—З–∞–µ–Љ–Њ–є —Б—В—А—Г–Ї—В—Г—А—Л.
 
–†–µ–ґ–Є–Љ "Maximum" –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –Њ—Ж–µ–љ–Ї—Г –≤–Ј–∞–Є–Љ–Њ—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–Є—П –≥–Є–њ–µ—А—Н—Е–Њ–≥–µ–љ–љ—Л—Е —Б–Є–≥–љ–∞–ї–Њ–≤ –≤–љ—Г—В—А–Є –≥–Є–њ–Њ—Н—Е–Њ–≥–µ–љ–љ—Л—Е, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Њ—Ж–µ–љ–Є–≤–∞—В—М —Б—В—А—Г–Ї—В—Г—А—Г –Є —Н—Е–Њ–≥–µ–љ–љ–Њ—Б—В—М —Б–Є–≥–љ–∞–ї–Њ–≤ –≤ –Њ–±—К–µ–Љ–µ. –Я—А–Њ–Ј—А–∞—З–љ–Њ—Б—В—М –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П —В–µ–Љ, —З—В–Њ –њ–Њ —Е–Њ–і—Г –≥–Є–њ–Њ—В–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –ї—Г—З–∞ –≤—Л–±–Є—А–∞–µ—В—Б—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М —Б–∞–Љ–Њ–≥–Њ —П—А–Ї–Њ–≥–Њ —Б–Є–≥–љ–∞–ї–∞.
 
–Т –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –±–Њ–ї—М—И–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–µ—В –Њ—Ж–µ–љ–Ї–∞ —Б–Њ—Б—В–Њ—П–љ–Є—П –Ї—А–Њ–≤–Њ—Б–љ–∞–±–ґ–µ–љ–Є—П –њ–Њ—А–∞–ґ–µ–љ–љ—Л—Е –Њ—А–≥–∞–љ–Њ–≤ –Є —В–Ї–∞–љ–µ–є. –Т—Л—П–≤–ї–µ–љ–Є–µ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є –њ—А–Є —А–∞–Ї–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ—А–Њ–≤–Њ–і–Є—В—М –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ—Г—О –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї—Г –Љ–µ–ґ–і—Г –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ–Є –Є –љ–µ–Њ–њ–ї–∞—Б—В–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Њ—Ж–µ—Б—Б–∞–Љ–Є. –•–∞—А–∞–Ї—В–µ—А –≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є –Њ–њ—Г—Е–Њ–ї–µ–є —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –Ї—А–Є—В–µ—А–Є–µ–≤ –Є—Е —А–Њ—Б—В–∞ –Є –Є–љ–≤–∞–Ј–Є–≤–љ–Њ—Б—В–Є, –њ–Њ—Н—В–Њ–Љ—Г –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П –Њ –љ–µ–є —З–∞—Б—В–Њ —Б—В–∞–љ–Њ–≤–Є—В—Б—П –Њ–њ—А–µ–і–µ–ї—П—О—Й–µ–є –≤ —Г—В–Њ—З–љ—П—О—Й–µ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ.
 
–Ф–ї—П –Њ–њ—Г—Е–Њ–ї–µ–≤—Л—Е —Б–Њ—Б—Г–і–Њ–≤ —Е–∞—А–∞–Ї—В–µ—А–љ–Њ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –≤–µ—В–≤–ї–µ–љ–Є–µ, —А–∞–Ј–ї–Є—З–љ—Л–є –Ї–∞–ї–Є–±—А, –Є–Ј–≤–Є—В–Њ–є —Е–Њ–і, —Б–ї–µ–њ—Л–µ –Ї–∞—А–Љ–∞–љ—Л –≤–Љ–µ—Б—В–Њ –Ї–Њ–љ—Ж–µ–≤—Л—Е –∞—А—В–µ—А–Є–Њ–ї, –∞ —В–∞–Ї–ґ–µ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —Б—В—А–Њ–µ–љ–Є—П —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є. –Т—Л—Б–Њ–Ї–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Є —В–Њ—З–љ–Њ—Б—В—М—О –≤ –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є –Љ–µ–ї–Ї–Є—Е —Б–Њ—Б—Г–і–Њ–≤ –Њ–±–ї–∞–і–∞—О—В –Љ–µ—В–Њ–і–Є–Ї–Є —Ж–≤–µ—В–Њ–≤–Њ–≥–Њ (–¶–Ф–Ъ) –Є —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–∞—А—В–Є—А–Њ–≤–∞–љ–Є—П.
 
–Я–Њ–ї—Г—З–µ–љ–Є–µ –њ—А–Є –£–Ч–Ш —Б –њ–Њ–Љ–Њ—Й—М—О –і–Њ–њ–њ–ї–µ—А–Њ–≤—Б–Ї–Њ–≥–Њ –Ї–∞—А—В–Є—А–Њ–≤–∞–љ–Є—П –Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є —Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б—В—А—Г–Ї—В—Г—А —А–∞–Ј–љ–Њ–≥–Њ –Ї–∞–ї–Є–±—А–∞ —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–µ–Љ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –Є –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є —В—А–µ—Е–Љ–µ—А–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–µ–є –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –њ–µ—А–µ–є—В–Є –Ї –љ–Њ–≤–Њ–є –Њ—Ж–µ–љ–Ї–µ —Б—В–µ–њ–µ–љ–Є –≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є –Њ—В–і–µ–ї—М–љ—Л—Е –Њ–±–ї–∞—Б—В–µ–є —Б –њ–Њ—Б—В—А–Њ–µ–љ–Є–µ–Љ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ–љ–љ–Њ–є –Ї–∞—А—В—Л —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –і–µ—А–µ–≤–∞. –Я—А–Є —Н—В–Њ–Љ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –≤—Л–њ–Њ–ї–љ–µ–љ–Њ –Ї–∞–Ї –≤ –Т-—А–µ–ґ–Є–Љ–µ, —В–∞–Ї –Є –≤ —А–µ–ґ–Є–Љ–µ —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–∞—А—В–Є—А–Њ–≤–∞–љ–Є—П. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–≥–Њ —Б–ї–Њ–ґ–µ–љ–Є—П —А–µ–ґ–Є–Љ–Њ–≤ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Ж–≤–µ—В–љ–Њ–≥–Њ –Ї–Њ–ї–Њ—А–∞–є–Ј–Є–љ–≥–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–≤–µ—А–µ–љ–љ–Њ –Њ–њ—А–µ–і–µ–ї—П—В—М –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї—Г—О –њ—А–Є–љ–∞–і–ї–µ–ґ–љ–Њ—Б—В—М –Ј–Њ–љ —Б –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–µ–є. –Ю–±—А–∞–±–Њ—В–∞–≤ –≤—Б–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –љ–∞ —А–∞–±–Њ—З–µ–є –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є —Б—В–∞–љ—Ж–Є–Є, –Є–Љ–µ–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ–Њ–ї—Г—З–µ–љ–Є—П —В—А–µ—Е–Љ–µ—А–љ—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є –Ї–∞–Ї –Њ—А–≥–∞–љ–∞, —В–∞–Ї –Є –µ–≥–Њ —Б–Њ—Б—Г–і–Њ–≤. –Я—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ–љ–љ–∞—П –Є–ї–Є –Њ–±—К–µ–Љ–љ–∞—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П –Њ —Е–Њ–і–µ –Ї—А—Г–њ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤, –Є–Ј—Г—З–µ–љ–Є–µ –≤–Ј–∞–Є–Љ–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П —Б–Њ—Б—Г–і–Њ–≤ –Њ—А–≥–∞–љ–∞ –Є –Њ–њ—Г—Е–Њ–ї–Є —П–≤–ї—П—О—В—Б—П –Њ–њ—А–µ–і–µ–ї—П—О—Й–Є–Љ–Є –і–ї—П —Е–Є—А—Г—А–≥–∞ –њ—А–Є –њ–ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–Є –Њ–њ–µ—А–∞—Ж–Є–Є.
 
–Я–Њ–і–µ–ї–Є–Љ—Б—П —Б–Њ–±—Б—В–≤–µ–љ–љ—Л–Љ –Њ–њ—Л—В–Њ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –≤ –Ї–ї–Є–љ–Є–Ї–µ –Њ—В–і–µ–ї—М–љ—Л—Е —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –Љ–µ—В–Њ–і–Є–Ї —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Љ–Њ—З–µ–≤–Њ–≥–Њ –њ—Г–Ј—Л—А—П, –њ—А–µ–і—Б—В–∞—В–µ–ї—М–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –Є —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є –њ—А–Є –Є—Е –Њ–њ—Г—Е–Њ–ї–µ–≤–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є. –Я—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –Є –≤—Л–≤–Њ–і—Л –±–∞–Ј–Є—А—Г—О—В—Б—П –љ–∞ —А–µ–Ј—Г–ї—М—В–∞—В–∞—Е —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –≤—А–∞—З–µ–є –Є –∞—Б–њ–Є—А–∞–љ—В–Њ–≤, –≤—Л–њ–Њ–ї–љ–µ–љ–љ—Л—Е –≤ –Њ—В–і–µ–ї–µ –ї—Г—З–µ–≤–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –¶–Э–Ш–†–†–Ш, –њ—А–Є —Г—З–∞—Б—В–Є–Є —Б–Њ—В—А—Г–і–љ–Є–Ї–Њ–≤ –Њ—В–і–µ–ї–∞ –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є –Є –Є–љ—В–µ—А–≤–µ–љ—Ж–Є–Њ–љ–љ–Њ–є —А–∞–і–Є–Њ–ї–Њ–≥–Є–Є –Є —А–∞–і–Є–∞—Ж–Є–Њ–љ–љ–Њ–є –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є–Є.
 
–Т¬† –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –і–ї—П –Њ—Ж–µ–љ–Ї–Є —Б—В–µ–њ–µ–љ–Є –≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є –Њ–њ—Г—Е–Њ–ї–Є –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ¬† –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Њ—Б—М —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–µ –Ї–∞—А—В–Є—А–Њ–≤–∞–љ–Є–µ, –Ї–Њ—В–Њ—А–Њ–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –¶–Ф–Ъ –Є–Љ–µ–µ—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –њ–Њ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є —В–Њ—З–љ–Њ—Б—В–Є –њ–µ—А–µ–і–∞—З–Є –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є. –Я—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ–Њ–µ –Њ—В–ї–Є—З–Є–µ —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–∞—А—В–Є—А–Њ–≤–∞–љ–Є—П –Њ—В –і—А—Г–≥–Є—Е –і–Њ–њ–њ–ї–µ—А–Њ–≤—Б–Ї–Є—Е –Љ–µ—В–Њ–і–Є–Ї –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ —В–Њ–Љ, —З—В–Њ –≤ –µ–≥–Њ –Њ—Б–љ–Њ–≤–µ –ї–µ–ґ–Є—В –Њ—Ж–µ–љ–Ї–∞ –љ–µ —З–∞—Б—В–Њ—В–љ–Њ–≥–Њ —Б–і–≤–Є–≥–∞, –∞ –∞–Љ–њ–ї–Є—В—Г–і—Л —Н—Е–Њ—Б–Є–≥–љ–∞–ї–∞, –Ї–Њ—В–Њ—А–∞—П –Њ—В—А–∞–ґ–∞–µ—В –њ–ї–Њ—В–љ–Њ—Б—В—М —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ –≤ –Ј–∞–і–∞–љ–љ–Њ–Љ –Њ–±—К–µ–Љ–µ. –Ю—Ж–µ–љ–Ї–∞ –њ–Њ –∞–Љ–њ–ї–Є—В—Г–і–µ –і–∞–µ—В –Љ–µ–љ—М—И–µ —И—Г–Љ–Њ–≤, —З–µ–Љ –Њ—Ж–µ–љ–Ї–∞ –њ–Њ —Б–і–≤–Є–≥—Г —З–∞—Б—В–Њ—В. –Р–Љ–њ–ї–Є—В—Г–і–∞ —Б–Є–≥–љ–∞–ї–Њ–≤ –Њ—В —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ –Љ–µ–љ–µ–µ –Ј–∞–≤–Є—Б–Є–Љ–∞ –Њ—В —З–∞—Б—В–Њ—В—Л –Ї–∞–і—А–Њ–≤, —З–µ–Љ —З–∞—Б—В–Њ—В–∞ —Б–Є–≥–љ–∞–ї–Њ–≤.
 
–Ф–ї—П –њ—А–Є–Љ–µ—А–Њ–≤ –њ—А–Є–≤–Њ–і–Є–Љ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П —Б —В—А–µ—Е–Љ–µ—А–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–µ–є –њ—А–Є –Њ–њ—Г—Е–Њ–ї–µ–≤–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є –Њ—В–і–µ–ї—М–љ—Л—Е –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Є—Е –Њ–±–ї–∞—Б—В–µ–є. –£–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б —В—А–µ—Е–Љ–µ—А–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–µ–є –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ —А–∞–Ї–∞ –Љ–Њ—З–µ–≤–Њ–≥–Њ –њ—Г–Ј—Л—А—П (—А–Є—Б. 1, 2). –£–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ —Б —В—А–µ—Е–Љ–µ—А–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–µ–є –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П —П–≤–ї—П–µ—В—Б—П –≤—Л—Б–Њ–Ї–Њ–Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ —А–∞–Ї–∞ –Љ–Њ—З–µ–≤–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Є —Б—В–µ–њ–µ–љ–Є –Љ–µ—Б—В–љ–Њ–≥–Њ –µ–≥–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—П. –Т —А–µ–ґ–Є–Љ–µ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–Є —Б–Њ–Ј–і–∞—О—В—Б—П –≤–Є—А—В—Г–∞–ї—М–љ—Л–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –Њ–њ—Г—Е–Њ–ї–Є, –≤–µ—Б—М–Љ–∞ –±–ї–Є–Ј–Ї–Є–µ –Ї —А–µ–∞–ї—М–љ—Л–Љ, –њ–Њ–ї—Г—З–∞–µ–Љ—Л–Љ –њ—А–Є —Ж–Є—Б—В–Њ—Б–Ї–Њ–њ–Є–Є.
 
|
|
 
–£–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–∞—П –∞–љ–≥–Є–Њ–≥—А–∞—Д–Є—П –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ —А–∞–Ї–∞ –њ—А–µ–і—Б—В–∞—В–µ–ї—М–љ–Њ–є –ґ–µ–ї–µ–Ј—Л (—А–Є—Б. 3, 4).
 
|
|
 
–Ф–Њ–Ї–∞–Ј–∞–љ–∞ –≤—Л—Б–Њ–Ї–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л—Е –Љ–µ—В–Њ–і–Є–Ї —Б –≤–Ї–ї—О—З–µ–љ–Є–µ–Љ –Ґ–†–£–Ч–Ш –≤ —А–µ–ґ–Є–Љ–µ —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–∞—А—В–Є—А–Њ–≤–∞–љ–Є—П —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є —В—А–µ—Е–Љ–µ—А–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–µ–є –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ —А–∞–Ї–∞ –њ—А–µ–і—Б—В–∞—В–µ–ї—М–љ–Њ–є –ґ–µ–ї–µ–Ј—Л (—А–Є—Б. 5) –љ–∞ —А–∞–Ј–љ—Л—Е —Б—В–∞–і–Є—П—Е —А–∞–Ј–≤–Є—В–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Ґ–†–£–Ч–Ш —Б —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є –∞–љ–≥–Є–Њ–≥—А–∞—Д–Є–µ–є —П–≤–ї—П—О—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ —В–Њ—З–љ—Л–Љ–Є –Љ–µ—В–Њ–і–Є–Ї–∞–Љ–Є –≤ —А–∞–љ–љ–µ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Љ–µ—Б—В–љ–Њ–≥–Њ —А–µ—Ж–Є–і–Є–≤–∞ —А–∞–Ї–∞ –њ—А–µ–і—Б—В–∞—В–µ–ї—М–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –њ–Њ—Б–ї–µ —А–∞–і–Є–Ї–∞–ї—М–љ–Њ–є –њ—А–Њ—Б—В–∞—В—Н–Ї—В–Њ–Љ–Є–Є.
 
|
 
–£–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤ –Њ—Ж–µ–љ–Ї–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Е–Є–Љ–Є–Њ–ї—Г—З–µ–≤–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П —А–∞–Ї–∞ —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є (—А–Є—Б. 6). –Э–∞ –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П—Е —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є –Њ–і–љ–Њ–є –Є —В–Њ–є –ґ–µ –±–Њ–ї—М–љ–Њ–є –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г–µ—В—Б—П —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Њ–±—К–µ–Љ–∞ –Њ–њ—Г—Е–Њ–ї–Є –Є —Б—В–µ–њ–µ–љ–Є –µ–µ –≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–є —Н–љ–і–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є —Е–Є–Љ–Є–Њ—Н–Љ–±–Њ–ї–Є–Ј–∞—Ж–Є–Є –Є —Б–Њ—З–µ—В–∞–љ–љ–Њ–≥–Њ —Е–Є–Љ–Є–Њ–ї—Г—З–µ–≤–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П.
 
|
 
–Ъ–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–µ –£–Ч–Ш —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–∞—А—В–Є—А–Њ–≤–∞–љ–Є—П –Є –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є —В—А–µ—Е–Љ–µ—А–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–µ–є –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –Љ–Њ–ґ–µ—В –±—Л—В—М —Б —Г—Б–њ–µ—Е–Њ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Њ –њ—А–Є –Љ–Њ–љ–Є—В–Њ—А–Є–љ–≥–µ –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —Е–Є–Љ–Є–Њ–ї—Г—З–µ–≤–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е —А–∞–Ї–Њ–Љ —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ–Њ–ї—Г—З–∞—В—М –Њ–±—К–µ–Ї—В–Є–≤–љ—Г—О –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—О –Њ –і–Є–љ–∞–Љ–Є–Ї–µ —А–µ–≥—А–µ—Б—Б–Є–Є –Њ–±—К–µ–Љ–∞ –Є —Б—В–µ–њ–µ–љ–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Ї—А–Њ–≤–Њ—Б–љ–∞–±–ґ–µ–љ–Є—П –Њ–њ—Г—Е–Њ–ї–Є.
 
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ –Њ –Є–Љ–µ—О—Й–Є—Е—Б—П –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є—П—Е —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –і–∞–≤–∞—В—М –њ–Њ—Б–ї–µ —Б–±–Њ—А–∞ –≤—Б–µ–є –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–є –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є, –њ—А–Є —Н—В–Њ–Љ –±–Њ–ї–µ–µ –љ–∞–≥–ї—П–і–љ—Л–µ, —Б–ї–Њ–ґ–љ—Л–µ –Є –Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –Љ–Њ–ґ–љ–Њ –њ–Њ–ї—Г—З–∞—В—М –њ–Њ—Б–ї–µ –Њ–±—А–∞–±–Њ—В–Ї–Є –≤—Б–µ—Е –і–∞–љ–љ—Л—Е –љ–∞ –њ–µ—А—Б–Њ–љ–∞–ї—М–љ–Њ–Љ –Ї–Њ–Љ–њ—М—О—В–µ—А–µ —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ —А–∞–Ј–ї–Є—З–љ—Л—Е —А–µ–ґ–Є–Љ–Њ–≤ –≤–Њ—Б–њ—А–Њ–Є–Ј–≤–µ–і–µ–љ–Є—П –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–є –Њ—Ж–µ–љ–Ї–Њ–є —Б—В–µ–њ–µ–љ–Є –≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –∞–љ–≥–Є–Њ–≥–Є—Б—В–Њ–≥—А–∞–Љ–Љ—Л. –Т —Ж–µ–ї–Њ–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є—П –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е —Б—В—А—Г–Ї—В—Г—А –љ–∞ –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ—Л—Е —Н—Е–Њ—В–Њ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–Ј–∞—Е –њ—А–Є —В—А–µ—Е–Љ–µ—А–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–Є —П–≤–ї—П–µ—В—Б—П –≤–∞–ґ–љ—Л–Љ, –∞ –њ–Њ—А–Њ–є –Є —А–µ—И–∞—О—Й–Є–Љ –њ–Њ —Б–≤–Њ–µ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є –і–Њ–њ–Њ–ї–љ–µ–љ–Є–µ–Љ –Ї –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є, –њ–Њ–ї—Г—З–∞–µ–Љ–Њ–є –њ—А–Є –Њ–±—Л—З–љ–Њ–Љ –і–≤—Г—Е–Љ–µ—А–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є.
 
–°—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ–Љ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л—Е —Б–Ї–∞–љ–µ—А–Њ–≤ –њ–Њ—Б–ї–µ–і–љ–µ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П —П–≤–ї—П–µ—В—Б—П –Є—Е –Њ—Б–љ–∞—Й–µ–љ–Є–µ —Г–і–Њ–±–љ—Л–Љ–Є —Б–Є—Б—В–µ–Љ–∞–Љ–Є –∞—А—Е–Є–≤–∞—Ж–Є–Є –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є, –Њ–±–ї–∞–і–∞—О—Й–Є–Љ–Є —И–Є—А–Њ–Ї–Є–Љ–Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—П–Љ–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –≤—Б–µ–≥–Њ –Њ–±—К–µ–Љ–∞ –і–∞–љ–љ—Л—Е, –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –і—А—Г–≥–Є–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—П–Љ–Є –±–µ–Ј —Г—З–∞—Б—В–Є—П –±–Њ–ї—М–љ—Л—Е, –Є –њ–Њ—Б—В—А–Њ–µ–љ–Є–µ –љ–Њ–≤—Л—Е –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е –£–Ч-–Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є. –° –Њ–і–љ–Њ–є —Б—В–Њ—А–Њ–љ—Л, —Н—В–Њ —Б–Њ–Ї—А–∞—Й–∞–µ—В –≤—А–µ–Љ—П –љ–∞ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Б –і—А—Г–≥–Њ–є - –Љ–Њ–ґ–µ—В –±—Л—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Њ –і–ї—П —Б—В–∞–љ–і–∞—А—В–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –Ї –£–Ч–Ш.
 
–Ь–Њ–ґ–љ–Њ —Г—В–≤–µ—А–ґ–і–∞—В—М, —З—В–Њ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Ї –љ–∞—Б—В–Њ—П—Й–µ–Љ—Г –≤—А–µ–Љ–µ–љ–Є –Њ–±–Њ–≥–∞—В–Є–ї–∞—Б—М –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ –љ–Њ–≤—Л–Љ–Є –Љ–µ—В–Њ–і–Є–Ї–∞–Љ–Є, –љ–µ—Б—Г—Й–Є–Љ–Є —З—А–µ–Ј–≤—Л—З–∞–є–љ–Њ –≤–∞–ґ–љ—Г—О –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї—Г—О –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—О –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –њ—А–Є –ї—О–±—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –Є –Ј–∞—Б—В–∞–≤–ї—П—О—Й–Є–Љ–Є –Ј–∞–љ–Њ–≤–Њ –њ–µ—А–µ—Б–Љ–Њ—В—А–µ—В—М —А–Њ–ї—М —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–µ —Б—А–µ–і—Б—В–≤ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є.
 
–°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –Љ–µ—В–Њ–і—Л —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б –Є—Е –≤—Л—Б–Њ–Ї–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–є –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ–Њ—Б—В—М—О –Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–µ–≤—Л—Б–Њ–Ї–Њ–є —Б—В–Њ–Є–Љ–Њ—Б—В—М—О, –∞ –њ–Њ—В–Њ–Љ—Г –Є –±–Њ–ї–µ–µ –і–Њ—Б—В—Г–њ–љ–Њ–є, –≤–Њ –Љ–љ–Њ–≥–Њ–Љ –Ј–∞–Љ–µ–љ–Є–ї–Є –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ –Љ–∞–≥–љ–Є—В–љ–Њ-—А–µ–Ј–Њ–љ–∞–љ—Б–љ—Г—О –Є —А–µ–љ—В–≥–µ–љ–Њ–≤—Б–Ї—Г—О –Ї–Њ–Љ–њ—М—О—В–µ—А–љ—Г—О —В–Њ–Љ–Њ–≥—А–∞—Д–Є—О –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –њ–∞—В–Њ–ї–Њ–≥–Є–Є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л—Е –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–є, –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –Њ—А–≥–∞–љ–Њ–≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –Є –Љ–∞–ї–Њ–≥–Њ —В–∞–Ј–∞. –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—З–Є—В—Л–≤–∞—В—М, —З—В–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –±–Њ–ї–µ–µ —Б–ї–Њ–ґ–љ—Л—Е —В–µ—Е–љ–Њ–ї–Њ–≥–Є–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є –Ј–∞—В—А—Г–і–љ–µ–љ–Њ, –Є–Ј-–Ј–∞ –≤—Л—Б–Њ–Ї–Њ–є —Б—В–Њ–Є–Љ–Њ—Б—В–Є –∞–њ–њ–∞—А–∞—В—Г—А—Л –Є, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є.
 
–Я—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–µ –≤—Л—И–µ —Б–њ–Њ—Б–Њ–±—Л —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤–љ–µ–і—А–µ–љ—Л –Є —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –≤ –њ–Њ–≤—Б–µ–і–љ–µ–≤–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –¶–Э–Ш–†–†–Ш. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –љ–Њ–≤—Л—Е —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л—Е —В–µ—Е–љ–Њ–ї–Њ–≥–Є–є –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –і—А—Г–≥–Є—Е –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є–є —А–∞–Ј–ї–Є—З–љ—Л—Е –Њ—А–≥–∞–љ–Њ–≤ –Є —Б–Є—Б—В–µ–Љ –∞–Ї—В–Є–≤–љ–Њ –Є–Ј—Г—З–∞—О—В—Б—П –≤ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –љ–∞—Г—З–љ—Л—Е —Ж–µ–љ—В—А–∞—Е –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ –Є –Ј–∞ —А—Г–±–µ–ґ–Њ–Љ. –Ь–Њ–ґ–љ–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ, –±–ї–∞–≥–Њ–і–∞—А—П –њ—А–Њ–≥—А–µ—Б—Б—Г –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є —В–µ—Е–љ–Є–Ї–Є, –Љ–µ—В–Њ–і–Є–Ї–Є –£–Ч–Ш, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –њ–Њ–ї—Г—З–µ–љ–Є–µ–Љ —В—А–µ—Е–Љ–µ—А–љ—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є, –Ї–Њ—В–Њ—А—Л–µ –Њ–±–ї–∞–і–∞—О—В –Ї –љ–∞—Б—В–Њ—П—Й–µ–Љ—Г –≤—А–µ–Љ–µ–љ–Є –љ–∞–≥–ї—П–і–љ–Њ—Б—В—М—О –Є –≤—Л—Б–Њ–Ї–Њ–є —Б—В–µ–њ–µ–љ—М—О –љ–∞–і–µ–ґ–љ–Њ—Б—В–Є, –≤ –±–ї–Є–ґ–∞–є—И–µ–Љ –±—Г–і—Г—Й–µ–Љ –±—Г–і—Г—В –Њ—В–љ–µ—Б–µ–љ—Л –Ї —А–∞–Ј—А—П–і—Г –Њ–±—Л—З–љ—Л—Е.