–Ш—Б—В–Њ—З–љ–Є–Ї: http://medicalplanet.su/xirurgia/234.html MedicalPlanet
 
–Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –∞–±—Б—Ж–µ—Б—Б–Њ–≤ –њ–∞—А–µ–љ—Е–Є–Љ–∞—В–Њ–Ј–љ—Л—Е –Њ—А–≥–∞–љ–Њ–≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є .
–Т –∞–±—Б–Њ–ї—О—В–љ–Њ–Љ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ –љ–∞–±–ї—О–і–µ–љ–Є–є –∞–±—Б—Ж–µ—Б—Б—Л —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—В—Б—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–Њ–є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є. –Я–µ—З–µ–љ—М –Є —Б–µ–ї–µ–Ј–µ–љ–Ї–∞ –њ—А–Є —Б–Њ–±–ї—О–і–µ–љ–Є–Є –Љ–µ—В–Њ–і–Є–Ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –і–Њ—Б—В—Г–њ–љ—Л –і–ї—П –£–Ч–Ш –≤–Њ –≤—Б–µ—Е –Њ—В–і–µ–ї–∞—Е. –Ф–ї—П –±–Њ–ї–µ–µ –і–µ—В–∞–ї—М–љ–Њ–≥–Њ –Њ—Б–Љ–Њ—В—А–∞ –њ–Њ–і–і–Є–∞—Д—А–∞–≥–Љ–∞–ї—М–љ—Л—Е –Њ—В–і–µ–ї–Њ–≤ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –њ—А–Є–µ–Љ—Л "–њ–Њ–ї–Є–њ–Њ–Ј–Є—Ж–Є–Њ–љ–љ–Њ—Б—В–Є". –С–Њ–ї—М–љ—Л–µ —Г–Ї–ї–∞–і—Л–≤–∞—О—В—Б—П –љ–∞ –њ—А–∞–≤—Л–є –Є–ї–Є –ї–µ–≤—Л–є –±–Њ–Ї, —А—Г–Ї—Г –Ј–∞–њ—А–Њ–Ї–Є–і—Л–≤–∞—О—В –≤–≤–µ—А—Е —Б –љ–µ–±–Њ–ї—М—И–Є–Љ —Б–≥–Є–±–∞–љ–Є–µ–Љ —В—Г–ї–Њ–≤–Є—Й–∞. –Т—Л–і–Њ—Е –њ–Њ—Б–ї–µ –≥–ї—Г–±–Њ–Ї–Њ–≥–Њ –≤–і–Њ—Е–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –Њ–±–Ј–Њ—А. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і—П—В —Б–µ–Ї—В–Њ—А–љ—Л–Љ –і–∞—В—З–Є–Ї–Њ–Љ –њ–Њ –Љ–µ–ґ—А–µ–±–µ—А–љ—Л–Љ –њ—А–Њ–Љ–µ–ґ—Г—В–Ї–∞–Љ –њ–Њ –њ–Њ–і–Љ—Л—И–µ—З–љ—Л–Љ –ї–Є–љ–Є—П–Љ. –Я—А–Є –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –њ—А–Њ–≤–Њ–і—П—В —В–Њ–њ–Є—З–µ—Б–Ї–Є–є –і–Є–∞–≥–љ–Њ–Ј –і–ї—П –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–Є—П –≤–љ—Г—В—А–Є–Њ—А–≥–∞–љ–љ—Л—Е –∞–±—Б—Ж–µ—Б—Б–Њ–≤ —Б –∞–±—Б—Ж–µ—Б—Б–∞–Љ–Є –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є. –Я–Њ–і–њ–µ—З–µ–љ–Њ—З–љ—Л–µ –∞–±—Б—Ж–µ—Б—Б—Л —З–∞—Й–µ –≤—Б–µ–≥–Њ –љ–µ–±–Њ–ї—М—И–Њ–≥–Њ —А–∞–Ј–Љ–µ—А–∞, –Њ–Ї—А—Г–≥–ї–Њ–є –Є–ї–Є –њ–Њ–ї–Є—Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ—Л, –љ–µ–Њ–і–љ–Њ—А–Њ–і–љ–Њ–є —Б—В—А—Г–Ї—В—Г—А—Л. –≠—Е–Њ–≥–µ–љ–љ–Њ—Б—В—М –Є—Е —Б–љ–Є–ґ–µ–љ–∞. –Ъ–Њ–љ—В—Г—А —З–µ—В–Ї–Є–є –Є –љ–µ—А–Њ–≤–љ—Л–є. –•–Њ—А–Њ—И–Њ –≤—Л—А–∞–ґ–µ–љ–∞ –Ї–∞–њ—Б—Г–ї–∞ –≤—Л—Б–Њ–Ї–Њ–є —Н—Е–Њ–≥–µ–љ–љ–Њ—Б—В–Є. –Я–Њ–і–њ–µ—З–µ–љ–Њ—З–љ—Л–µ –∞–±—Б—Ж–µ—Б—Б—Л —З–∞—Й–µ, —З–µ–Љ –≤–љ—Г—В—А–Є–њ–µ—З–µ–љ–Њ—З–љ—Л–µ, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—В—Б—П –≤—Л–њ–Њ—В–Њ–Љ –≤ –њ—А–∞–≤—Л—Е –Њ—В–і–µ–ї–∞—Е –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є. –∞–±—Б—Ж–µ—Б—Б –њ–µ—З–µ–љ–Є –Я—А–Є –њ–Њ–і–Њ–Ј—А–µ–љ–Є–Є –љ–∞ –∞–±—Б—Ж–µ—Б—Б—Л —Б–µ–ї–µ–Ј–µ–љ–Ї–Є (—Г—З–Є—В—Л–≤–∞—П –Є—Е —А–µ–і–Ї–Њ—Б—В—М) –≤ —Б–Њ–Љ–љ–Є—В–µ–ї—М–љ—Л—Е —Б–ї—Г—З–∞—П—Е –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є–љ–Є–Љ–∞—В—М –≤–Њ –≤–љ–Є–Љ–∞–љ–Є–µ, —З—В–Њ –£–Ч-–Ї–∞—А—В–Є–љ—Л –∞–±—Б—Ж–µ—Б—Б–∞ —Б–µ–ї–µ–Ј–µ–љ–Ї–Є –Є –і–љ–∞ –ґ–µ–ї—Г–і–Ї–∞ —Б—Е–Њ–і–љ—Л. –Ф–ї—П —Н—В–Њ–≥–Њ –£–Ч–Ш –≤—Л–њ–Њ–ї–љ—П—О—В –≤ –і–Є–љ–∞–Љ–Є–Ї–µ —З–µ—А–µ–Ј 30 –Љ–Є–љ –њ–Њ—Б–ї–µ –Њ–±–Є–ї—М–љ–Њ–≥–Њ –њ–Є—В—М—П. –Т —Б–ї—Г—З–∞—П—Е, –Ї–Њ–≥–і–∞ –љ–∞–њ–Њ–ї–љ–µ–љ–Є–µ –ґ–µ–ї—Г–і–Ї–∞ –±—Л–≤–∞–µ—В –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Њ, –≤ –ґ–µ–ї—Г–і–Њ—З–љ—Л–є –Ј–Њ–љ–і –≤–≤–Њ–і—П—В 20,0 –Љ–ї –≥–ї—О–Ї–Њ–Ј—Л. –Ф–Є–∞–≥–љ–Њ–Ј —Г—В–Њ—З–љ—П—О—В –њ–Њ –љ–∞–ї–Є—З–Є—О –Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Є—О –њ–µ—А–µ–і–≤–Є–ґ–µ–љ–Є—П –≤–≤–Њ–і–Є–Љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–Є. –Ь–µ–ї–Ї–Є–µ, –і–Њ 15 –Љ–Љ –≤ –і–Є–∞–Љ–µ—В—А–µ, –∞–±—Б—Ж–µ—Б—Б—Л –њ–µ—З–µ–љ–Є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А—Г—О—В —Б —Б–µ–њ—В–Є—З–µ—Б–Ї–Є–Љ–Є –Њ—З–∞–≥–∞–Љ–Є. –Я–Њ—Б–ї–µ–і–љ–Є–µ –Њ—В–ї–Є—З–∞—О—В –љ–µ–±–Њ–ї—М—И–Њ–є –і–Є–∞–Љ–µ—В—А (–і–Њ 10вАФ15 –Љ–Љ), –њ—А–∞–≤–Є–ї—М–љ–∞—П —Д–Њ—А–Љ–∞, —А–Њ–≤–љ—Л–µ, —З–µ—В–Ї–Є–µ –Ї–Њ–љ—В—Г—А—Л, –Њ–і–љ–Њ—А–Њ–і–љ–∞—П —Б—В—А—Г–Ї—В—Г—А–∞ –Є –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Б–љ–Є–ґ–µ–љ–љ–∞—П —Н—Е–Њ–≥–µ–љ–љ–Њ—Б—В—М, –∞ —В–∞–Ї–ґ–µ –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Н—Е–Њ–≥–µ–љ–љ–Њ–є –Ї–∞–њ—Б—Г–ї—Л –Є –Ј–Њ–љ—Л –њ–µ—А–Є—Д–Њ–Ї–∞–ї—М–љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П. –Ю–љ–Є –Љ–Њ–≥—Г—В –±—Л—В—М –µ–і–Є–љ–Є—З–љ—Л–Љ–Є –Є –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л–Љ–Є. –Э–Њ –≥–ї–∞–≤–љ–Њ–µ –Є—Е –Њ—В–ї–Є—З–Є–µ –Њ—В –∞–±—Б—Ж–µ—Б—Б–Њ–≤ –њ–µ—З–µ–љ–Є –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ –±—Л—Б—В—А–Њ—В–µ –њ–Њ—П–≤–ї–µ–љ–Є—П –Є –Њ–±—А–∞—В–љ–Њ–≥–Њ —А–∞–Ј–≤–Є—В–Є—П –њ—А–Є –∞–і–µ–Ї–≤–∞—В–љ–Њ–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є. –Ь—Л –љ–∞–±–ї—О–і–∞–ї–Є —Б–µ–њ—В–Є—З–µ—Б–Ї–Є–µ –Њ—З–∞–≥–Є –≤ –њ–µ—З–µ–љ–Є —Г 4 –±–Њ–ї—М–љ—Л—Е —Г 2—Б —Б–µ–њ—Б–Є—Б–Њ–Љ –Є –∞–±—Б—Ж–µ—Б—Б–∞–Љ–Є –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –Є —Г 2 —Б —А–∞–Ј–ї–Є—В—Л–Љ –≥–љ–Њ–є–љ—Л–Љ –њ–µ—А–Є—В–Њ–љ–Є—В–Њ–Љ. –Э–Є –≤ –Њ–і–љ–Њ–Љ —Б–ї—Г—З–∞–µ —В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є–Є –≤ –∞–±—Б—Ж–µ—Б—Б –љ–µ –њ—А–Њ–Є–Ј–Њ—И–ї–Њ. –Ш–Ј —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Г –±–Њ–ї—М–љ—Л—Е —Б –≤–љ—Г—В—А–Є–Њ—А–≥–∞–љ–љ—Л–Љ–Є –∞–±—Б—Ж–µ—Б—Б–∞–Љ–Є –Њ—В–Љ–µ—З–µ–љ–Њ: —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –њ–Њ—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –Њ—А–≥–∞–љ–∞; –Ј–∞–Ї—А—Г–≥–ї–µ–љ–Є–µ –љ–Є–ґ–љ–µ–≥–Њ –Ї—А–∞—П –њ–µ—З–µ–љ–Є; –і–Є—Д—Д—Г–Ј–љ–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Н—Е–Њ–≥–µ–љ–љ–Њ—Б—В–Є –њ–∞—А–µ–љ—Е–Є–Љ—Л –њ–µ—З–µ–љ–Є; —А–µ–∞–Ї—В–Є–≤–љ–Њ–µ —Г—В–Њ–ї—Й–µ–љ–Є–µ –Є –њ–Њ–≤—Л—И–µ–љ–Є–µ —Н—Е–Њ–≥–µ–љ–љ–Њ—Б—В–Є —Б—В–µ–љ–Ї–Є –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П; —А–µ–∞–Ї—В–Є–≤–љ—Л–є –≤—Л–њ–Њ—В –≤ –њ–ї–µ–≤—А–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є (—Г –±–Њ–ї—М–љ—Л—Е —Б –∞–±—Б—Ж–µ—Б—Б–∞–Љ–Є VII –Є VIII —Б–µ–≥–Љ–µ–љ—В–Њ–≤ –њ–µ—З–µ–љ–Є). –£ 1 —А–µ–±–µ–љ–Ї–∞ –ї–Њ—Ж–Є—А–Њ–≤–∞–ї–Є—Б—М —Г–≤–µ–ї–Є—З–µ–љ–љ—Л–µ –ї–Є–Љ—Д–∞—В–Є—З–µ—Б–Ї–Є–µ —Г–Ј–ї—Л –њ–Њ —Е–Њ–і—Г –≤–Њ—А–Њ—В–љ–Њ–є –≤–µ–љ—Л. –£ –њ–µ—А–≤–Є—З–љ–Њ –љ–µ–Њ–њ–µ—А–Є—А–Њ–≤–∞–љ–љ—Л—Е –±–Њ–ї—М–љ—Л—Е –њ—А–Њ–≤–Њ–і–Є–ї—Б—П –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј –Љ–µ–ґ–і—Г –∞–±—Б—Ж–µ—Б—Б–Њ–Љ –Є –≥–µ–Љ–∞—В–Њ–Љ–Њ–є. –£–Ч-—Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–∞ —Н—В–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Њ—З–µ–љ—М —Б—Е–Њ–ґ–∞. –Я—А–Є –≥–µ–Љ–∞—В–Њ–Љ–∞—Е –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Б—А–Њ–Ї–∞ —Б—Г—Й–µ—Б—В–≤–Њ–≤–∞–љ–Є—П —Н—Е–Њ–≥–µ–љ–љ–Њ—Б—В—М —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–≥–Њ –≤–∞—А—М–Є—А—Г–µ—В –Њ—В –љ–Є–Ј–Ї–Њ–є –і–Њ –µ–µ –њ–Њ–ї–љ–Њ–≥–Њ –Њ—В—Б—Г—В—Б—В–≤–Є—П, —Б—В—А—Г–Ї—В—Г—А–∞ –±–Њ–ї–µ–µ –Њ–і–љ–Њ—А–Њ–і–љ–∞, –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В –Ј–Њ–љ–∞ –њ–µ—А–Є—Д–Њ–Ї–∞–ї—М–љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П.
 
–Ш—Б—В–Њ—З–љ–Є–Ї: http://medicalplanet.su/xirurgia/234.html MedicalPlanet
 
 |
    |
–Ф–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л—Е –Љ–µ—В–Њ–і–Є–Ї –≤ –Њ–љ–Ї–Њ—Г—А–Њ–ї–Њ–≥–Є–Є –Є –Њ–љ–Ї–Њ–≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є–Є.–С.–Р. –Ь–Є–љ—М–Ї–Њ.
–¶–Э–Ш —А–µ–љ—В–≥–µ–љ–Њ—А–∞–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –Є–љ—Б—В–Є—В—Г—В –Ь–Ч–°–† –†–§, –°–∞–љ–Ї—В-–Я–µ—В–µ—А–±—Г—А–≥, –†–Њ—Б—Б–Є—П |
 
–Т–≤–µ–і–µ–љ–Є–µ
 
–Ш–Ј–≤–µ—Б—В–љ—Л–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –£–Ч–Ш –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –і—А—Г–≥–Є–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є –ї—Г—З–µ–≤–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ —Б–≤—П–Ј–∞–љ—Л —Б –љ–µ–Є–љ–≤–∞–Ј–Є–≤–љ–Њ—Б—В—М—О, –±—Л—Б—В—А–Њ—В–Њ–є –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П, –±–µ–Ј–≤—А–µ–і–љ–Њ—Б—В—М—О –і–ї—П –Ј–і–Њ—А–Њ–≤—М—П –њ–∞—Ж–Є–µ–љ—В–∞. –Т—Л—Б–Њ–Ї–∞—П –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ–Њ—Б—В—М –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–Є–Ј–Ї–Њ–є —Б—В–Њ–Є–Љ–Њ—Б—В—М—О –њ–Њ–Ј–≤–Њ–ї–Є–ї–Є –Ј–∞–љ—П—В—М –µ–Љ—Г –Њ–і–љ–Њ –Є–Ј –≤–µ–і—Г—Й–Є—Е –Љ–µ—Б—В —Б—А–µ–і–Є –і—А—Г–≥–Є—Е –Љ–µ—В–Њ–і–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Я–Њ—Б–ї–µ–і–љ–Є–µ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –љ–∞—Г—З–љ–Њ-—В–µ—Е–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ–≥—А–µ—Б—Б–∞ –Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –Ї–Њ–Љ–њ—М—О—В–µ—А–љ—Л—Е —В–µ—Е–љ–Њ–ї–Њ–≥–Є–є –њ—А–Є–≤–µ–ї–Є –Ї —Б–Њ–Ј–і–∞–љ–Є—О –љ–Њ–≤–Њ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –£–Ч-–∞–њ–њ–∞—А–∞—В–Њ–≤, –Њ–±–ї–∞–і–∞—О—Й–Є—Е –≤—Л—Б–Њ–Ї–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О, —З—В–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —А–∞—Б—И–Є—А–Є–ї–Њ –Њ–±–ї–∞—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –£–Ч–Ш –≤ –Љ–µ–і–Є—Ж–Є–љ–µ –Є –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ –Є–Ј–Љ–µ–љ–Є–ї–Њ –њ–Њ–ї—Г—З–∞–µ–Љ—Г—О –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї—Г—О –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—О. –Т—Л—Б–Њ–Ї–Њ–µ –Ї–∞—З–µ—Б—В–≤–Њ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –±–ї–∞–≥–Њ–і–∞—А—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—О —Ж–Є—Д—А–Њ–≤–Њ–є —В–µ—Е–љ–Є–Ї–Є –і–ї—П –Њ–±—А–∞–±–Њ—В–Ї–Є –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –∞–Ї—Г—Б—В–Є—З–µ—Б–Ї–Є—Е —Б–Є–≥–љ–∞–ї–Њ–≤. –Т –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –њ—А–∞–Ї—В–Є–Ї—Г –≤–Њ—И–ї–Є –љ–Њ–≤—Л–µ —В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є –£–Ч–Ш: –љ–∞—В–Є–≤–љ–∞—П –Є –≤—В–Њ—А–∞—П –≥–∞—А–Љ–Њ–љ–Є–Ї–Є, –Ї–Њ–≥–µ—А–µ–љ—В–љ–Њ–µ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П, —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Є–є –і–Њ–њ–њ–ї–µ—А, –і–Њ–њ–њ–ї–µ—А–Њ–≤—Б–Ї–∞—П –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є—П —В–Ї–∞–љ–µ–є, —В—А–µ—Е–Љ–µ—А–љ–∞—П –Є –њ–∞–љ–Њ—А–∞–Љ–љ–∞—П —Н—Е–Њ–≥—А–∞—Д–Є–Є, —Н—Е–Њ–Ї–Њ–љ—В—А–∞—Б—В–љ–∞—П –∞–љ–≥–Є–Њ–≥—А–∞—Д–Є—П, —В—А–µ—Е–Љ–µ—А–љ—Л–µ —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–Є –≤ —А–µ–∞–ї—М–љ–Њ–Љ –≤—А–µ–Љ–µ–љ–Є. –Т—Б–µ –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л–µ –Є –і—А—Г–≥–Є–µ –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л–µ —Б–њ–Њ—Б–Њ–±—Л –њ–Њ–ї—Г—З–µ–љ–Є—П –£–Ч-–Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –≤–љ–Њ—Б—П—В —А–∞–Ј–ї–Є—З–љ—Л–є –≤–Ї–ї–∞–і –≤ —Г–ї—Г—З—И–µ–љ–Є–µ –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є —Б—В—А—Г–Ї—В—Г—А—Л –њ–∞—А–µ–љ—Е–Є–Љ–∞—В–Њ–Ј–љ—Л—Е –Є –њ–Њ–ї—Л—Е –Њ—А–≥–∞–љ–Њ–≤, —А–∞–Ј–ї–Є—З–љ—Л—Е —В–Ї–∞–љ–µ–є –Є —Б–Њ—Б—Г–і–Њ–≤. –Т—Л–і–µ–ї–µ–љ–Є–µ —Б–Њ—Б—Г–і–Њ–≤, –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П –Є—Е —Б—В–µ–љ–Ї–Є –Є –і–Њ–њ–њ–ї–µ—А–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–∞—П –Њ—Ж–µ–љ–Ї–∞ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –≤ –љ–Њ—А–Љ–µ –Є –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є—П—Е –Љ–Њ–ґ–µ—В –≤ —И–Є—А–Њ–Ї–Є—Е –њ—А–µ–і–µ–ї–∞—Е –љ–µ—Б—В–Є –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—О –Њ —Е–∞—А–∞–Ї—В–µ—А–µ –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є–Ї–Є –Њ—В–і–µ–ї—М–љ—Л—Е –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Є—Е –Њ–±–ї–∞—Б—В–µ–є.
 
–°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –Љ–љ–Њ–≥–Њ—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –£–Ч-–∞–њ–њ–∞—А–∞—В—Л –Њ–±–ї–∞–і–∞—О—В —Г–љ–Є–Ї–∞–ї—М–љ—Л–Љ–Є –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–Љ–Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—П–Љ–Є –Є –Љ–Њ–≥—Г—В –±—Л—В—М –њ–Њ–ї–љ–Њ—Ж–µ–љ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ—Л –њ—А–Є –≥–ї—Г–±–Њ–Ї–Њ–Љ –Ј–љ–∞–љ–Є–Є —В–µ–Њ—А–µ—В–Є—З–µ—Б–Ї–Є—Е –Њ—Б–љ–Њ–≤ –њ–Њ–ї—Г—З–µ–љ–Є—П –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П, –∞ —В–∞–Ї–ґ–µ –њ—А–Є —Г—В–Њ—З–љ–µ–љ–Є–Є –Њ–±–ї–∞—Б—В–µ–є –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П, –њ—А–µ–і–ї–∞–≥–∞–µ–Љ—Л—Е —А–∞–Ј—А–∞–±–Њ—В—З–Є–Ї–∞–Љ–Є –љ–Њ–≤—Л—Е —Н—Е–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е –Љ–µ—В–Њ–і–Є–Ї.
 
–Я–Њ–ї—Г—З–µ–љ–Є–µ —В—А–µ—Е–Љ–µ—А–љ—Л—Е —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—В–Є–≤–љ—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є —Б–Њ—Б—Г–і–Њ–≤, –≤—Л–Ј—Л–≤–∞–µ—В –±–Њ–ї—М—И–Њ–є –Є–љ—В–µ—А–µ—Б —Г –Ї–ї–Є–љ–Є—Ж–Є—Б—В–Њ–≤ –Є, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ, –Њ–љ–Ї–Њ–ї–Њ–≥–Њ–≤, —З—В–Њ —Г—Б–Ї–Њ—А—П–µ—В –Є—Е –≤–љ–µ–і—А–µ–љ–Є–µ –≤ –њ—А–∞–Ї—В–Є–Ї—Г. –Т–Њ—Б–њ—А–Є—П—В–Є–µ –Є –∞–љ–∞–ї–Є–Ј –Њ–±—К–µ–Љ–љ—Л—Е –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Є—Е —Б—В—А—Г–Ї—В—Г—А –љ–µ —Б—В–Њ–ї—М–Ї–Њ —Б–ї–Њ–ґ–љ—Л, –Ї–∞–Ї –љ–µ–њ—А–Є–≤—Л—З–љ—Л –і–ї—П –≤—А–∞—З–µ–є —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є. –≠—В–Њ –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –љ–Њ–≤—Л—Е –њ–Њ–і—Е–Њ–і–Њ–≤ –≤ –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є–Є –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –Є –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–≥–Њ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ –≤—А–∞—З–µ–±–љ–Њ–≥–Њ –љ–∞–≤—Л–Ї–∞, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–µ–≥–Њ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ–µ—А–µ–і–Њ–≤–Њ–є —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є —В–µ—Е–љ–Є–Ї–Є. –Я—А–Є —Н—В–Њ–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—З–Є—В—Л–≤–∞—В—М, —З—В–Њ –њ—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Њ–±—Й–µ–њ—А–Є–љ—П—В—Л–µ –≤ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –њ—А–Њ—Б–Љ–Њ—В—А –Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ—Л–є –∞–љ–∞–ї–Є–Ј –±–Њ–ї—М—И–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Н—Е–Њ—В–Њ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–Ј–Њ–≤ –≤ —А–µ–∞–ї—М–љ–Њ–Љ –≤—А–µ–Љ–µ–љ–Є –љ–µ –Љ–µ–љ–µ–µ —Г—В–Њ–Љ–Є—В–µ–ї–µ–љ, —З–µ–Љ –Є–Ј—Г—З–µ–љ–Є–µ –і–∞–љ–љ—Л—Е, –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –≤ –µ–і–Є–љ–Њ–Љ –±–ї–Њ–Ї–µ –Є–ї–Є —Б–µ—А–Є–Є —В–Њ–Љ–Њ–≥—А–∞–Љ–Љ –і—А—Г–≥–Њ–≥–Њ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Ж–Є—Д—А–Њ–≤—Л—Е –Ї–Њ–Љ–њ—М—О—В–µ—А–љ—Л—Е –њ—А–Њ–≥—А–∞–Љ–Љ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –њ–Њ–ї—Г—З–µ–љ–Є–µ —В—А–µ—Е–Љ–µ—А–љ—Л—Е —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤ —А–µ–∞–ї—М–љ–Њ–Љ –≤—А–µ–Љ–µ–љ–Є, –Ј–∞—В—А–∞—В–Є–≤ –љ–∞ –≤–µ—Б—М –њ—А–Њ—Ж–µ—Б—Б 20-30 —Б. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –љ–∞–Є–±–Њ–ї–µ–µ —И–Є—А–Њ–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –љ–Њ–≤—Л–µ —В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є –£–Ч–Ш –љ–∞—И–ї–Є –≤ –∞–Ї—Г—И–µ—А—Б—В–≤–µ.
 
–Ь–∞—В–µ—А–Є–∞–ї—Л –Є –Љ–µ—В–Њ–і—Л
 
–Я—А–Є –њ–Њ—Б—В—А–Њ–µ–љ–Є–Є —В—А–µ—Е–Љ–µ—А–љ—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є –њ—А–Є–Љ–µ–љ—П—О—В –ї–Є–±–Њ –∞–≤—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–є —Б–±–Њ—А –Њ–±—К–µ–Љ–љ–Њ–є –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ–≥–Њ —В—А–µ—Е–Љ–µ—А–љ–Њ–≥–Њ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –і–∞—В—З–Є–Ї–∞ –ї–Є–±–Њ –њ–Њ—Б—В—Г–њ–∞—В–µ–ї—М–љ–Њ–µ –њ–µ—А–µ–Љ–µ—Й–µ–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–Љ –Њ–±—Л—З–љ–Њ–≥–Њ –і–∞—В—З–Є–Ї–∞ —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–µ–є –Њ–±—К–µ–Љ–∞. –Ф–ї—П –Њ–±—А–∞–±–Њ—В–Ї–Є —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л—Е —В—А–µ—Е–Љ–µ—А–љ—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –∞–њ—А–Њ–±–Є—А–Њ–≤–∞–љ–љ—Л–µ –њ—А–Є –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є –Є –Љ–∞–≥–љ–Є—В–љ–Њ-—А–µ–Ј–Њ–љ–∞–љ—Б–љ–Њ–є —В–Њ–Љ–Њ–≥—А–∞—Д–Є–Є —В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є: –Љ–љ–Њ–≥–Њ–њ–ї–∞–љ–∞—А–љ–∞—П —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є—П (Multiplanar reconstruction, MPR), –њ—А–Њ–µ–Ї—Ж–Є—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є (MIP) –Є (MinIP), –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–∞—П —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є—П –Њ–±—К–µ–Ї—В–∞ (Surface shading rendering) –Є–ї–Є —В—А–µ—Е–Љ–µ—А–љ–∞—П —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є—П (3D volume rendering). –Ю—Б–Њ–±—Л–є –Є–љ—В–µ—А–µ—Б –≤ –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Д—Г–љ–Ї—Ж–Є–Є VOCALвДҐ, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є–µ –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В—М –≤–Є—А—В—Г–∞–ї—М–љ—Л–є –Њ—А–≥–∞–љ–Њ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є, –∞ —В–∞–Ї–ґ–µ —Д—Г–љ–Ї—Ж–Є–Є, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–Є–µ —В–Њ—З–љ–Њ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Њ–±—К–µ–Љ–Њ–≤.
 
–Я—А–Є –∞–љ–∞–ї–Є–Ј–µ –Њ—В–і–µ–ї—М–љ—Л—Е –Њ–±—К–µ–Ї—В–Њ–≤, –Є–Љ–µ—О—Й–Є—Е –±–Њ–ї—М—И—Г—О —А–∞–Ј–љ–Є—Ж—Г –∞–Ї—Г—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є—П, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ —В—А–µ—Е–Љ–µ—А–љ—Л–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –ї–µ–≥–Ї–Њ —Б–Њ–њ–Њ—Б—В–∞–≤–ї—П—В—М —Б –њ—А–Є–≤—Л—З–љ—Л–Љ–Є –і–≤—Г—Е–Љ–µ—А–љ—Л–Љ–Є, —В–∞–Ї –Ї–∞–Ї —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –Ї–Њ–Љ–њ—М—О—В–µ—А–љ—Л–µ —В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є –њ–Њ–Ј–≤–Њ–ї—П—О—В –≤–Ї–ї—О—З–∞—В—М –≤–Њ—Б–њ—А–Њ–Є–Ј–≤–µ–і–µ–љ–Є–µ –Њ–±—К–µ–Љ–∞ –Є —В–µ–љ–µ–≤–Њ–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–µ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є.
 
–Я–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л–є —А–µ–ґ–Є–Љ "Surface" –њ—А–µ–і–љ–∞–Ј–љ–∞—З–µ–љ –і–ї—П –Њ—В–Њ–±—А–∞–ґ–µ–љ–Є—П –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Њ–±—К–µ–Љ–љ–Њ–≥–Њ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П. –Т —Н—В–Є—Е —Б–ї—Г—З–∞—П—Е –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В –і–≤—Г—Е–Љ–µ—А–љ—Л–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –Є –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В –Є—Е —В—А–µ—Е–Љ–µ—А–љ—Г—О –∞–љ–∞—В–Њ–Љ–Є—О –њ–Њ–і –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ—Л–Љ —Г–≥–ї–Њ–Љ –њ—А–Њ–µ–Ї—Ж–Є–Є —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –≤–∞—А–Є–∞–љ—В–∞–Љ–Є –Њ—Б–≤–µ—Й–µ–љ–Є—П –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Є –≥–ї—Г–±–Є–љ—Л –≥–Є–њ–Њ—В–µ—В–Є—З–µ—Б–Ї–Є–Љ –Є—Б—В–Њ—З–љ–Є–Ї–Њ–Љ —Б–≤–µ—В–∞ –Є–ї–Є –≤—А–∞—Й–∞—В–µ–ї—М–љ–Њ–≥–Њ –і–≤–Є–ґ–µ–љ–Є—П –Є–Ј—Г—З–∞–µ–Љ–Њ–є —Б—В—А—Г–Ї—В—Г—А—Л.
 
–†–µ–ґ–Є–Љ "Maximum" –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –Њ—Ж–µ–љ–Ї—Г –≤–Ј–∞–Є–Љ–Њ—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–Є—П –≥–Є–њ–µ—А—Н—Е–Њ–≥–µ–љ–љ—Л—Е —Б–Є–≥–љ–∞–ї–Њ–≤ –≤–љ—Г—В—А–Є –≥–Є–њ–Њ—Н—Е–Њ–≥–µ–љ–љ—Л—Е, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Њ—Ж–µ–љ–Є–≤–∞—В—М —Б—В—А—Г–Ї—В—Г—А—Г –Є —Н—Е–Њ–≥–µ–љ–љ–Њ—Б—В—М —Б–Є–≥–љ–∞–ї–Њ–≤ –≤ –Њ–±—К–µ–Љ–µ. –Я—А–Њ–Ј—А–∞—З–љ–Њ—Б—В—М –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П —В–µ–Љ, —З—В–Њ –њ–Њ —Е–Њ–і—Г –≥–Є–њ–Њ—В–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –ї—Г—З–∞ –≤—Л–±–Є—А–∞–µ—В—Б—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М —Б–∞–Љ–Њ–≥–Њ —П—А–Ї–Њ–≥–Њ —Б–Є–≥–љ–∞–ї–∞.
 
–Т –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –±–Њ–ї—М—И–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–µ—В –Њ—Ж–µ–љ–Ї–∞ —Б–Њ—Б—В–Њ—П–љ–Є—П –Ї—А–Њ–≤–Њ—Б–љ–∞–±–ґ–µ–љ–Є—П –њ–Њ—А–∞–ґ–µ–љ–љ—Л—Е –Њ—А–≥–∞–љ–Њ–≤ –Є —В–Ї–∞–љ–µ–є. –Т—Л—П–≤–ї–µ–љ–Є–µ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є –њ—А–Є —А–∞–Ї–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ—А–Њ–≤–Њ–і–Є—В—М –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ—Г—О –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї—Г –Љ–µ–ґ–і—Г –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ–Є –Є –љ–µ–Њ–њ–ї–∞—Б—В–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Њ—Ж–µ—Б—Б–∞–Љ–Є. –•–∞—А–∞–Ї—В–µ—А –≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є –Њ–њ—Г—Е–Њ–ї–µ–є —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –Ї—А–Є—В–µ—А–Є–µ–≤ –Є—Е —А–Њ—Б—В–∞ –Є –Є–љ–≤–∞–Ј–Є–≤–љ–Њ—Б—В–Є, –њ–Њ—Н—В–Њ–Љ—Г –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П –Њ –љ–µ–є —З–∞—Б—В–Њ —Б—В–∞–љ–Њ–≤–Є—В—Б—П –Њ–њ—А–µ–і–µ–ї—П—О—Й–µ–є –≤ —Г—В–Њ—З–љ—П—О—Й–µ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ.
 
–Ф–ї—П –Њ–њ—Г—Е–Њ–ї–µ–≤—Л—Е —Б–Њ—Б—Г–і–Њ–≤ —Е–∞—А–∞–Ї—В–µ—А–љ–Њ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –≤–µ—В–≤–ї–µ–љ–Є–µ, —А–∞–Ј–ї–Є—З–љ—Л–є –Ї–∞–ї–Є–±—А, –Є–Ј–≤–Є—В–Њ–є —Е–Њ–і, —Б–ї–µ–њ—Л–µ –Ї–∞—А–Љ–∞–љ—Л –≤–Љ–µ—Б—В–Њ –Ї–Њ–љ—Ж–µ–≤—Л—Е –∞—А—В–µ—А–Є–Њ–ї, –∞ —В–∞–Ї–ґ–µ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —Б—В—А–Њ–µ–љ–Є—П —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є. –Т—Л—Б–Њ–Ї–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Є —В–Њ—З–љ–Њ—Б—В—М—О –≤ –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є –Љ–µ–ї–Ї–Є—Е —Б–Њ—Б—Г–і–Њ–≤ –Њ–±–ї–∞–і–∞—О—В –Љ–µ—В–Њ–і–Є–Ї–Є —Ж–≤–µ—В–Њ–≤–Њ–≥–Њ (–¶–Ф–Ъ) –Є —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–∞—А—В–Є—А–Њ–≤–∞–љ–Є—П.
 
–Я–Њ–ї—Г—З–µ–љ–Є–µ –њ—А–Є –£–Ч–Ш —Б –њ–Њ–Љ–Њ—Й—М—О –і–Њ–њ–њ–ї–µ—А–Њ–≤—Б–Ї–Њ–≥–Њ –Ї–∞—А—В–Є—А–Њ–≤–∞–љ–Є—П –Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є —Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б—В—А—Г–Ї—В—Г—А —А–∞–Ј–љ–Њ–≥–Њ –Ї–∞–ї–Є–±—А–∞ —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–µ–Љ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –Є –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є —В—А–µ—Е–Љ–µ—А–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–µ–є –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –њ–µ—А–µ–є—В–Є –Ї –љ–Њ–≤–Њ–є –Њ—Ж–µ–љ–Ї–µ —Б—В–µ–њ–µ–љ–Є –≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є –Њ—В–і–µ–ї—М–љ—Л—Е –Њ–±–ї–∞—Б—В–µ–є —Б –њ–Њ—Б—В—А–Њ–µ–љ–Є–µ–Љ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ–љ–љ–Њ–є –Ї–∞—А—В—Л —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –і–µ—А–µ–≤–∞. –Я—А–Є —Н—В–Њ–Љ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –≤—Л–њ–Њ–ї–љ–µ–љ–Њ –Ї–∞–Ї –≤ –Т-—А–µ–ґ–Є–Љ–µ, —В–∞–Ї –Є –≤ —А–µ–ґ–Є–Љ–µ —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–∞—А—В–Є—А–Њ–≤–∞–љ–Є—П. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–≥–Њ —Б–ї–Њ–ґ–µ–љ–Є—П —А–µ–ґ–Є–Љ–Њ–≤ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Ж–≤–µ—В–љ–Њ–≥–Њ –Ї–Њ–ї–Њ—А–∞–є–Ј–Є–љ–≥–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–≤–µ—А–µ–љ–љ–Њ –Њ–њ—А–µ–і–µ–ї—П—В—М –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї—Г—О –њ—А–Є–љ–∞–і–ї–µ–ґ–љ–Њ—Б—В—М –Ј–Њ–љ —Б –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–µ–є. –Ю–±—А–∞–±–Њ—В–∞–≤ –≤—Б–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –љ–∞ —А–∞–±–Њ—З–µ–є –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є —Б—В–∞–љ—Ж–Є–Є, –Є–Љ–µ–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ–Њ–ї—Г—З–µ–љ–Є—П —В—А–µ—Е–Љ–µ—А–љ—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є –Ї–∞–Ї –Њ—А–≥–∞–љ–∞, —В–∞–Ї –Є –µ–≥–Њ —Б–Њ—Б—Г–і–Њ–≤. –Я—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ–љ–љ–∞—П –Є–ї–Є –Њ–±—К–µ–Љ–љ–∞—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П –Њ —Е–Њ–і–µ –Ї—А—Г–њ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤, –Є–Ј—Г—З–µ–љ–Є–µ –≤–Ј–∞–Є–Љ–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П —Б–Њ—Б—Г–і–Њ–≤ –Њ—А–≥–∞–љ–∞ –Є –Њ–њ—Г—Е–Њ–ї–Є —П–≤–ї—П—О—В—Б—П –Њ–њ—А–µ–і–µ–ї—П—О—Й–Є–Љ–Є –і–ї—П —Е–Є—А—Г—А–≥–∞ –њ—А–Є –њ–ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–Є –Њ–њ–µ—А–∞—Ж–Є–Є.
 
–Я–Њ–і–µ–ї–Є–Љ—Б—П —Б–Њ–±—Б—В–≤–µ–љ–љ—Л–Љ –Њ–њ—Л—В–Њ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –≤ –Ї–ї–Є–љ–Є–Ї–µ –Њ—В–і–µ–ї—М–љ—Л—Е —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –Љ–µ—В–Њ–і–Є–Ї —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Љ–Њ—З–µ–≤–Њ–≥–Њ –њ—Г–Ј—Л—А—П, –њ—А–µ–і—Б—В–∞—В–µ–ї—М–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –Є —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є –њ—А–Є –Є—Е –Њ–њ—Г—Е–Њ–ї–µ–≤–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є. –Я—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –Є –≤—Л–≤–Њ–і—Л –±–∞–Ј–Є—А—Г—О—В—Б—П –љ–∞ —А–µ–Ј—Г–ї—М—В–∞—В–∞—Е —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –≤—А–∞—З–µ–є –Є –∞—Б–њ–Є—А–∞–љ—В–Њ–≤, –≤—Л–њ–Њ–ї–љ–µ–љ–љ—Л—Е –≤ –Њ—В–і–µ–ї–µ –ї—Г—З–µ–≤–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –¶–Э–Ш–†–†–Ш, –њ—А–Є —Г—З–∞—Б—В–Є–Є —Б–Њ—В—А—Г–і–љ–Є–Ї–Њ–≤ –Њ—В–і–µ–ї–∞ –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є –Є –Є–љ—В–µ—А–≤–µ–љ—Ж–Є–Њ–љ–љ–Њ–є —А–∞–і–Є–Њ–ї–Њ–≥–Є–Є –Є —А–∞–і–Є–∞—Ж–Є–Њ–љ–љ–Њ–є –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є–Є.
 
–Т¬† –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –і–ї—П –Њ—Ж–µ–љ–Ї–Є —Б—В–µ–њ–µ–љ–Є –≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є –Њ–њ—Г—Е–Њ–ї–Є –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ¬† –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Њ—Б—М —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–µ –Ї–∞—А—В–Є—А–Њ–≤–∞–љ–Є–µ, –Ї–Њ—В–Њ—А–Њ–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –¶–Ф–Ъ –Є–Љ–µ–µ—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –њ–Њ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є —В–Њ—З–љ–Њ—Б—В–Є –њ–µ—А–µ–і–∞—З–Є –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є. –Я—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ–Њ–µ –Њ—В–ї–Є—З–Є–µ —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–∞—А—В–Є—А–Њ–≤–∞–љ–Є—П –Њ—В –і—А—Г–≥–Є—Е –і–Њ–њ–њ–ї–µ—А–Њ–≤—Б–Ї–Є—Е –Љ–µ—В–Њ–і–Є–Ї –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ —В–Њ–Љ, —З—В–Њ –≤ –µ–≥–Њ –Њ—Б–љ–Њ–≤–µ –ї–µ–ґ–Є—В –Њ—Ж–µ–љ–Ї–∞ –љ–µ —З–∞—Б—В–Њ—В–љ–Њ–≥–Њ —Б–і–≤–Є–≥–∞, –∞ –∞–Љ–њ–ї–Є—В—Г–і—Л —Н—Е–Њ—Б–Є–≥–љ–∞–ї–∞, –Ї–Њ—В–Њ—А–∞—П –Њ—В—А–∞–ґ–∞–µ—В –њ–ї–Њ—В–љ–Њ—Б—В—М —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ –≤ –Ј–∞–і–∞–љ–љ–Њ–Љ –Њ–±—К–µ–Љ–µ. –Ю—Ж–µ–љ–Ї–∞ –њ–Њ –∞–Љ–њ–ї–Є—В—Г–і–µ –і–∞–µ—В –Љ–µ–љ—М—И–µ —И—Г–Љ–Њ–≤, —З–µ–Љ –Њ—Ж–µ–љ–Ї–∞ –њ–Њ —Б–і–≤–Є–≥—Г —З–∞—Б—В–Њ—В. –Р–Љ–њ–ї–Є—В—Г–і–∞ —Б–Є–≥–љ–∞–ї–Њ–≤ –Њ—В —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ –Љ–µ–љ–µ–µ –Ј–∞–≤–Є—Б–Є–Љ–∞ –Њ—В —З–∞—Б—В–Њ—В—Л –Ї–∞–і—А–Њ–≤, —З–µ–Љ —З–∞—Б—В–Њ—В–∞ —Б–Є–≥–љ–∞–ї–Њ–≤.
 
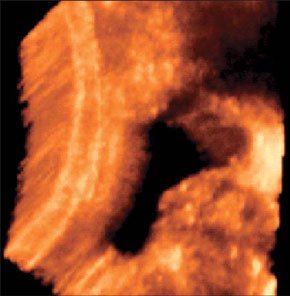
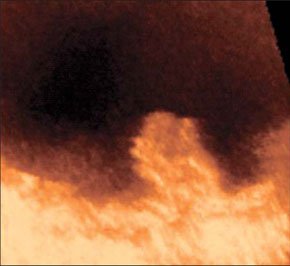
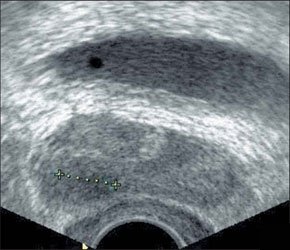
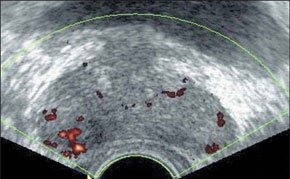
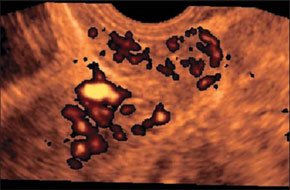
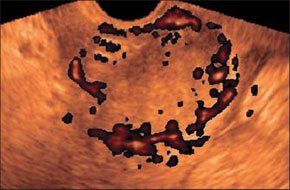
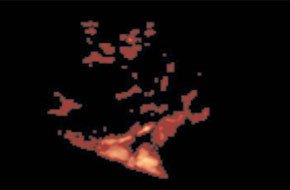
–Ф–ї—П –њ—А–Є–Љ–µ—А–Њ–≤ –њ—А–Є–≤–Њ–і–Є–Љ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П —Б —В—А–µ—Е–Љ–µ—А–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–µ–є –њ—А–Є –Њ–њ—Г—Е–Њ–ї–µ–≤–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є –Њ—В–і–µ–ї—М–љ—Л—Е –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Є—Е –Њ–±–ї–∞—Б—В–µ–є. –£–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б —В—А–µ—Е–Љ–µ—А–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–µ–є –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ —А–∞–Ї–∞ –Љ–Њ—З–µ–≤–Њ–≥–Њ –њ—Г–Ј—Л—А—П (—А–Є—Б. 1, 2). –£–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ —Б —В—А–µ—Е–Љ–µ—А–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–µ–є –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П —П–≤–ї—П–µ—В—Б—П –≤—Л—Б–Њ–Ї–Њ–Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ —А–∞–Ї–∞ –Љ–Њ—З–µ–≤–Њ–≥–Њ –њ—Г–Ј—Л—А—П –Є —Б—В–µ–њ–µ–љ–Є –Љ–µ—Б—В–љ–Њ–≥–Њ –µ–≥–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—П. –Т —А–µ–ґ–Є–Љ–µ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–Є —Б–Њ–Ј–і–∞—О—В—Б—П –≤–Є—А—В—Г–∞–ї—М–љ—Л–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –Њ–њ—Г—Е–Њ–ї–Є, –≤–µ—Б—М–Љ–∞ –±–ї–Є–Ј–Ї–Є–µ –Ї —А–µ–∞–ї—М–љ—Л–Љ, –њ–Њ–ї—Г—З–∞–µ–Љ—Л–Љ –њ—А–Є —Ж–Є—Б—В–Њ—Б–Ї–Њ–њ–Є–Є.
 
|
|
 
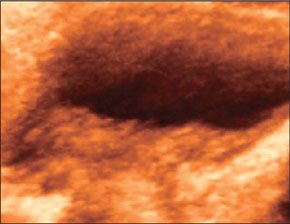
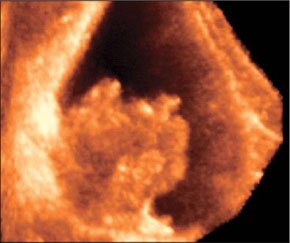
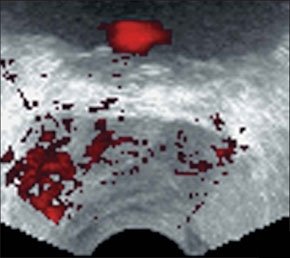
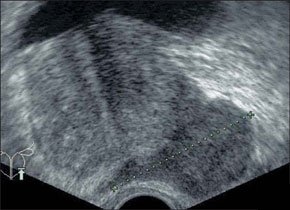
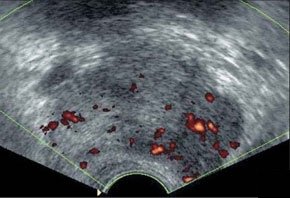
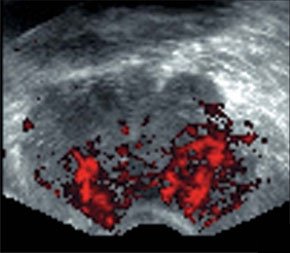
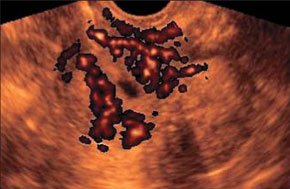
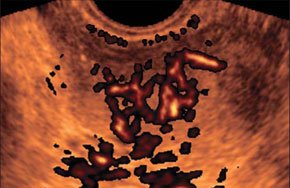
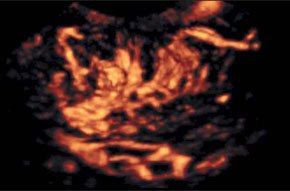
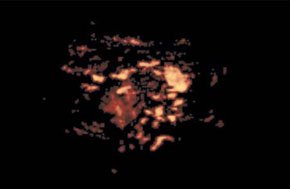
–£–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–∞—П –∞–љ–≥–Є–Њ–≥—А–∞—Д–Є—П –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ —А–∞–Ї–∞ –њ—А–µ–і—Б—В–∞—В–µ–ї—М–љ–Њ–є –ґ–µ–ї–µ–Ј—Л (—А–Є—Б. 3, 4).
 
|
|
 
–Ф–Њ–Ї–∞–Ј–∞–љ–∞ –≤—Л—Б–Њ–Ї–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л—Е –Љ–µ—В–Њ–і–Є–Ї —Б –≤–Ї–ї—О—З–µ–љ–Є–µ–Љ –Ґ–†–£–Ч–Ш –≤ —А–µ–ґ–Є–Љ–µ —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–∞—А—В–Є—А–Њ–≤–∞–љ–Є—П —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є —В—А–µ—Е–Љ–µ—А–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–µ–є –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ —А–∞–Ї–∞ –њ—А–µ–і—Б—В–∞—В–µ–ї—М–љ–Њ–є –ґ–µ–ї–µ–Ј—Л (—А–Є—Б. 5) –љ–∞ —А–∞–Ј–љ—Л—Е —Б—В–∞–і–Є—П—Е —А–∞–Ј–≤–Є—В–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Ґ–†–£–Ч–Ш —Б —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є –∞–љ–≥–Є–Њ–≥—А–∞—Д–Є–µ–є —П–≤–ї—П—О—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ —В–Њ—З–љ—Л–Љ–Є –Љ–µ—В–Њ–і–Є–Ї–∞–Љ–Є –≤ —А–∞–љ–љ–µ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Љ–µ—Б—В–љ–Њ–≥–Њ —А–µ—Ж–Є–і–Є–≤–∞ —А–∞–Ї–∞ –њ—А–µ–і—Б—В–∞—В–µ–ї—М–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –њ–Њ—Б–ї–µ —А–∞–і–Є–Ї–∞–ї—М–љ–Њ–є –њ—А–Њ—Б—В–∞—В—Н–Ї—В–Њ–Љ–Є–Є.
 
|
 
–£–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤ –Њ—Ж–µ–љ–Ї–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Е–Є–Љ–Є–Њ–ї—Г—З–µ–≤–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П —А–∞–Ї–∞ —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є (—А–Є—Б. 6). –Э–∞ –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П—Е —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є –Њ–і–љ–Њ–є –Є —В–Њ–є –ґ–µ –±–Њ–ї—М–љ–Њ–є –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г–µ—В—Б—П —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Њ–±—К–µ–Љ–∞ –Њ–њ—Г—Е–Њ–ї–Є –Є —Б—В–µ–њ–µ–љ–Є –µ–µ –≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–є —Н–љ–і–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є —Е–Є–Љ–Є–Њ—Н–Љ–±–Њ–ї–Є–Ј–∞—Ж–Є–Є –Є —Б–Њ—З–µ—В–∞–љ–љ–Њ–≥–Њ —Е–Є–Љ–Є–Њ–ї—Г—З–µ–≤–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П.
 
|
 
–Ъ–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–µ –£–Ч–Ш —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–∞—А—В–Є—А–Њ–≤–∞–љ–Є—П –Є –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є —В—А–µ—Е–Љ–µ—А–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–µ–є –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –Љ–Њ–ґ–µ—В –±—Л—В—М —Б —Г—Б–њ–µ—Е–Њ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Њ –њ—А–Є –Љ–Њ–љ–Є—В–Њ—А–Є–љ–≥–µ –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —Е–Є–Љ–Є–Њ–ї—Г—З–µ–≤–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е —А–∞–Ї–Њ–Љ —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ–Њ–ї—Г—З–∞—В—М –Њ–±—К–µ–Ї—В–Є–≤–љ—Г—О –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—О –Њ –і–Є–љ–∞–Љ–Є–Ї–µ —А–µ–≥—А–µ—Б—Б–Є–Є –Њ–±—К–µ–Љ–∞ –Є —Б—В–µ–њ–µ–љ–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Ї—А–Њ–≤–Њ—Б–љ–∞–±–ґ–µ–љ–Є—П –Њ–њ—Г—Е–Њ–ї–Є.
 
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ –Њ –Є–Љ–µ—О—Й–Є—Е—Б—П –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є—П—Е —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –і–∞–≤–∞—В—М –њ–Њ—Б–ї–µ —Б–±–Њ—А–∞ –≤—Б–µ–є –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–є –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є, –њ—А–Є —Н—В–Њ–Љ –±–Њ–ї–µ–µ –љ–∞–≥–ї—П–і–љ—Л–µ, —Б–ї–Њ–ґ–љ—Л–µ –Є –Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –Љ–Њ–ґ–љ–Њ –њ–Њ–ї—Г—З–∞—В—М –њ–Њ—Б–ї–µ –Њ–±—А–∞–±–Њ—В–Ї–Є –≤—Б–µ—Е –і–∞–љ–љ—Л—Е –љ–∞ –њ–µ—А—Б–Њ–љ–∞–ї—М–љ–Њ–Љ –Ї–Њ–Љ–њ—М—О—В–µ—А–µ —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ —А–∞–Ј–ї–Є—З–љ—Л—Е —А–µ–ґ–Є–Љ–Њ–≤ –≤–Њ—Б–њ—А–Њ–Є–Ј–≤–µ–і–µ–љ–Є—П –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–є –Њ—Ж–µ–љ–Ї–Њ–є —Б—В–µ–њ–µ–љ–Є –≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –∞–љ–≥–Є–Њ–≥–Є—Б—В–Њ–≥—А–∞–Љ–Љ—Л. –Т —Ж–µ–ї–Њ–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є—П –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е —Б—В—А—Г–Ї—В—Г—А –љ–∞ –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ—Л—Е —Н—Е–Њ—В–Њ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–Ј–∞—Е –њ—А–Є —В—А–µ—Е–Љ–µ—А–љ–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–Є —П–≤–ї—П–µ—В—Б—П –≤–∞–ґ–љ—Л–Љ, –∞ –њ–Њ—А–Њ–є –Є —А–µ—И–∞—О—Й–Є–Љ –њ–Њ —Б–≤–Њ–µ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є –і–Њ–њ–Њ–ї–љ–µ–љ–Є–µ–Љ –Ї –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є, –њ–Њ–ї—Г—З–∞–µ–Љ–Њ–є –њ—А–Є –Њ–±—Л—З–љ–Њ–Љ –і–≤—Г—Е–Љ–µ—А–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є.
 
–°—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ–Љ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л—Е —Б–Ї–∞–љ–µ—А–Њ–≤ –њ–Њ—Б–ї–µ–і–љ–µ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П —П–≤–ї—П–µ—В—Б—П –Є—Е –Њ—Б–љ–∞—Й–µ–љ–Є–µ —Г–і–Њ–±–љ—Л–Љ–Є —Б–Є—Б—В–µ–Љ–∞–Љ–Є –∞—А—Е–Є–≤–∞—Ж–Є–Є –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є, –Њ–±–ї–∞–і–∞—О—Й–Є–Љ–Є —И–Є—А–Њ–Ї–Є–Љ–Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—П–Љ–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –≤—Б–µ–≥–Њ –Њ–±—К–µ–Љ–∞ –і–∞–љ–љ—Л—Е, –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –і—А—Г–≥–Є–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—П–Љ–Є –±–µ–Ј —Г—З–∞—Б—В–Є—П –±–Њ–ї—М–љ—Л—Е, –Є –њ–Њ—Б—В—А–Њ–µ–љ–Є–µ –љ–Њ–≤—Л—Е –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е –£–Ч-–Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є. –° –Њ–і–љ–Њ–є —Б—В–Њ—А–Њ–љ—Л, —Н—В–Њ —Б–Њ–Ї—А–∞—Й–∞–µ—В –≤—А–µ–Љ—П –љ–∞ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Б –і—А—Г–≥–Њ–є - –Љ–Њ–ґ–µ—В –±—Л—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Њ –і–ї—П —Б—В–∞–љ–і–∞—А—В–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –Ї –£–Ч–Ш.
 
–Ь–Њ–ґ–љ–Њ —Г—В–≤–µ—А–ґ–і–∞—В—М, —З—В–Њ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Ї –љ–∞—Б—В–Њ—П—Й–µ–Љ—Г –≤—А–µ–Љ–µ–љ–Є –Њ–±–Њ–≥–∞—В–Є–ї–∞—Б—М –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ –љ–Њ–≤—Л–Љ–Є –Љ–µ—В–Њ–і–Є–Ї–∞–Љ–Є, –љ–µ—Б—Г—Й–Є–Љ–Є —З—А–µ–Ј–≤—Л—З–∞–є–љ–Њ –≤–∞–ґ–љ—Г—О –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї—Г—О –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—О –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –њ—А–Є –ї—О–±—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –Є –Ј–∞—Б—В–∞–≤–ї—П—О—Й–Є–Љ–Є –Ј–∞–љ–Њ–≤–Њ –њ–µ—А–µ—Б–Љ–Њ—В—А–µ—В—М —А–Њ–ї—М —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–µ —Б—А–µ–і—Б—В–≤ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є.
 
–°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –Љ–µ—В–Њ–і—Л —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б –Є—Е –≤—Л—Б–Њ–Ї–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–є –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ–Њ—Б—В—М—О –Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–µ–≤—Л—Б–Њ–Ї–Њ–є —Б—В–Њ–Є–Љ–Њ—Б—В—М—О, –∞ –њ–Њ—В–Њ–Љ—Г –Є –±–Њ–ї–µ–µ –і–Њ—Б—В—Г–њ–љ–Њ–є, –≤–Њ –Љ–љ–Њ–≥–Њ–Љ –Ј–∞–Љ–µ–љ–Є–ї–Є –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ –Љ–∞–≥–љ–Є—В–љ–Њ-—А–µ–Ј–Њ–љ–∞–љ—Б–љ—Г—О –Є —А–µ–љ—В–≥–µ–љ–Њ–≤—Б–Ї—Г—О –Ї–Њ–Љ–њ—М—О—В–µ—А–љ—Г—О —В–Њ–Љ–Њ–≥—А–∞—Д–Є—О –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –њ–∞—В–Њ–ї–Њ–≥–Є–Є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л—Е –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–є, –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –Њ—А–≥–∞–љ–Њ–≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –Є –Љ–∞–ї–Њ–≥–Њ —В–∞–Ј–∞. –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—З–Є—В—Л–≤–∞—В—М, —З—В–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –±–Њ–ї–µ–µ —Б–ї–Њ–ґ–љ—Л—Е —В–µ—Е–љ–Њ–ї–Њ–≥–Є–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є –Ј–∞—В—А—Г–і–љ–µ–љ–Њ, –Є–Ј-–Ј–∞ –≤—Л—Б–Њ–Ї–Њ–є —Б—В–Њ–Є–Љ–Њ—Б—В–Є –∞–њ–њ–∞—А–∞—В—Г—А—Л –Є, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є.
 
–Я—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–µ –≤—Л—И–µ —Б–њ–Њ—Б–Њ–±—Л —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤–љ–µ–і—А–µ–љ—Л –Є —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –≤ –њ–Њ–≤—Б–µ–і–љ–µ–≤–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –¶–Э–Ш–†–†–Ш. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –љ–Њ–≤—Л—Е —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л—Е —В–µ—Е–љ–Њ–ї–Њ–≥–Є–є –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –і—А—Г–≥–Є—Е –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є–є —А–∞–Ј–ї–Є—З–љ—Л—Е –Њ—А–≥–∞–љ–Њ–≤ –Є —Б–Є—Б—В–µ–Љ –∞–Ї—В–Є–≤–љ–Њ –Є–Ј—Г—З–∞—О—В—Б—П –≤ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –љ–∞—Г—З–љ—Л—Е —Ж–µ–љ—В—А–∞—Е –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ –Є –Ј–∞ —А—Г–±–µ–ґ–Њ–Љ. –Ь–Њ–ґ–љ–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ, –±–ї–∞–≥–Њ–і–∞—А—П –њ—А–Њ–≥—А–µ—Б—Б—Г –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є —В–µ—Е–љ–Є–Ї–Є, –Љ–µ—В–Њ–і–Є–Ї–Є –£–Ч–Ш, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –њ–Њ–ї—Г—З–µ–љ–Є–µ–Љ —В—А–µ—Е–Љ–µ—А–љ—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є, –Ї–Њ—В–Њ—А—Л–µ –Њ–±–ї–∞–і–∞—О—В –Ї –љ–∞—Б—В–Њ—П—Й–µ–Љ—Г –≤—А–µ–Љ–µ–љ–Є –љ–∞–≥–ї—П–і–љ–Њ—Б—В—М—О –Є –≤—Л—Б–Њ–Ї–Њ–є —Б—В–µ–њ–µ–љ—М—О –љ–∞–і–µ–ґ–љ–Њ—Б—В–Є, –≤ –±–ї–Є–ґ–∞–є—И–µ–Љ –±—Г–і—Г—Й–µ–Љ –±—Г–і—Г—В –Њ—В–љ–µ—Б–µ–љ—Л –Ї —А–∞–Ј—А—П–і—Г –Њ–±—Л—З–љ—Л—Е.
–Э–∞–≤–Є–≥–∞—Ж–Є–Њ–љ–љ–∞—П —Е–Є—А—Г—А–≥–Є—П –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –£–Ч–Ш
 
–Э–∞–≤–Є–≥–∞—Ж–Є–Њ–љ–љ–∞—П –њ—Г–љ–Ї—Ж–Є–Њ–љ–љ–∞—П —Е–Є—А—Г—А–≥–Є—П –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –£–Ч–Ш вАУ –љ–Њ–≤–Њ–µ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–µ –≤ –Љ–∞–ї–Њ–Є–љ–≤–∞–Ј–Є–≤–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–µ–µ –Є–Ј–ї–µ—З–Є–≤–∞—В—М –љ–µ–Ї–Њ—В–Њ—А—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Њ—А–≥–∞–љ–Њ–≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –±–µ–Ј —А–∞—Б—Б–µ—З–µ–љ–Є—П –њ–Њ–Ї—А–Њ–≤–Њ–≤. –°—Г—В—М –Љ–µ—В–Њ–і–∞ —Б–Њ—Б—В–Њ–Є—В –≤ —В–Њ–Љ, —З—В–Њ —Е–Є—А—Г—А–≥ –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –£–Ч–Ш —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ–є –Є–≥–ї–Њ–є –њ—Г–љ–Ї—В–Є—А—Г–µ—В –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ (–Ї–Є—Б—В–∞, –∞–±—Б—Ж–µ—Б—Б, –њ–Њ–ї–Њ—Б—В—М), –Њ—Б—В–∞–≤–ї—П—П –≤ —В–Ї–∞–љ—П—Е –њ–Њ–ї–Є—Н—В–Є–ї–µ–љ–Њ–≤—Л–є –Ї–∞—В–µ—В–µ—А –і–ї—П –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є —Б–∞–љ–∞—Ж–Є–Є –Є–ї–Є –≤–≤–µ–і–µ–љ–Є—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Я–Њ–Ї–∞–Ј–∞–љ–Є—П –Ї —Н—В–Њ–є –њ—А–Њ—Ж–µ–і—Г—А–µ –і–Њ–≤–Њ–ї—М–љ–Њ –Њ–±—И–Є—А–љ—Л: –ї–Њ–ґ–љ—Л–µ –Ї–Є—Б—В—Л –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л, –њ–∞—А–∞–Ј–Є—В–∞—А–љ—Л–µ –Є –љ–µ–њ–∞—А–∞–Ј–Є—В–∞—А–љ—Л–µ –Ї–Є—Б—В—Л –њ–µ—З–µ–љ–Є, –∞–±—Б—Ж–µ—Б—Б—Л –њ–µ—З–µ–љ–Є, –Ј–∞–±—А—О—И–Є–љ–љ–Њ–≥–Њ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–∞, –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–µ –∞–±—Б—Ж–µ—Б—Б—Л –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є - –њ–Њ–і–і–Є–∞—Д—А–∞–≥–Љ–∞–ї—М–љ—Л–µ, –њ–Њ–і–њ–µ—З–µ–љ–Њ—З–љ—Л–µ, –Љ–µ–ґ–Ї–Є—И–µ—З–љ—Л–µ. –І–∞—Й–µ —В–∞–Ї–Є–µ —Б–Є—В—Г–∞—Ж–Є–Є¬† –≤–Њ–Ј–љ–Є–Ї–∞–ї–Є –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–є –њ–Њ –њ–Њ–≤–Њ–і—Г –Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л—Е —Д–Њ—А–Љ —П–Ј–≤–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –ґ–µ–ї—Г–і–Ї–∞.
 
–Т –†–Њ—Б—Б–Є–Є –њ—Г–љ–Ї—Ж–Є–Њ–љ–љ–∞—П —Е–Є—А—Г—А–≥–Є—П —Б—Г—Й–µ—Б—В–≤—Г–µ—В –≤–Њ –Љ–љ–Њ–≥–Є—Е –≥–Њ—А–Њ–і–∞—Е.¬† –Ю—Б–Њ–±—Л—Е —В—А–µ–±–Њ–≤–∞–љ–Є–є –Ї –∞–њ–њ–∞—А–∞—В–∞–Љ –£–Ч–Ш –љ–µ—В, –љ–Њ —З–µ–Љ –ї—Г—З—И–µ, —В–µ–Љ –ї—Г—З—И–µ. –Т–∞–ґ–љ–µ–µ, –Ї–∞–Ї —З–µ–ї–Њ–≤–µ–Ї —Б–Љ–Њ—В—А–Є—В, –Ї —З–µ–Љ—Г –њ—А–Є–≤—Л–Ї–∞–µ—В.¬†
 
–Ф–ї—П –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Њ–≥–Њ —Е–Є—А—Г—А–≥–∞ –≤—Б–µ–≥–і–∞ –±–µ—Б–њ–Њ–Ї–Њ–є–љ–Њ, –љ–∞—Б–Ї–Њ–ї—М–Ї–Њ —Н—В–Є –њ—Г–љ–Ї—Ж–Є–Є —А–∞–і–Є–Ї–∞–ї—М–љ—Л? –°–µ–є—З–∞—Б –±–Њ–ї—М—И–µ –Ј–∞–љ–Є–Љ–∞—О—В—Б—П –ї–µ—З–µ–љ–Є–µ–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є: –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Є —Б–∞–Љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є. –° —Г–≤–µ—А–µ–љ–љ–Њ—Б—В—М—О –Љ–Њ–ґ–љ–Њ —Б–Ї–∞–Ј–∞—В—М, —З—В–Њ –≤ 70% —Б–ї—Г—З–∞–µ–≤ –њ—Г–љ–Ї—Ж–Є–Њ–љ–љ–∞—П ¬†—Е–Є—А—Г—А–≥–Є—П вАУ —Н—В–Њ –Ј–∞–Ї–Њ–љ—З–µ–љ–љ–∞—П –Њ–њ–µ—А–∞—Ж–Є—П, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–∞—П –і–Њ–±–Є—В—М—Б—П —А–∞–і–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Є–Ј–ї–µ—З–µ–љ–Є—П. –Ш–љ–Њ–≥–і–∞ –њ—А–Є—Е–Њ–і–Є—В—Б—П –≤–Љ–µ—И–Є–≤–∞—В—М—Б—П –њ–Њ–≤—В–Њ—А–љ–Њ. –Я—А–Є –≥–љ–Њ–є–љ—Л—Е –∞–±—Б—Ж–µ—Б—Б–∞—Е –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤–≤–µ–і–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –њ—А–Є –љ–µ–њ–∞—А–∞–Ј–Є—В–∞—А–љ—Л—Е –Ї–Є—Б—В–∞—Е –њ–µ—З–µ–љ–Є вАУ —Б–Ї–ї–µ—А–Њ–Ј–Є—А–Њ–≤–∞–љ–Є–µ 96¬Ї —Б–њ–Є—А—В–Њ–Љ. –Т —Б—А–µ–і–љ–µ–Љ, –Љ–µ—В–Њ–і –≤ 2 —А–∞–Ј–∞ —Б–Њ–Ї—А–∞—Й–∞–µ—В –Є –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–є –њ–µ—А–Є–Њ–і, –Є —Б—А–Њ–Ї–Є —Г—В—А–∞—В—Л —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є. –Ю–±–µ–Ј–±–Њ–ї–Є–≤–∞–љ–Є–µ –њ—А–Є–Љ–µ–љ—П–µ–Љ –Љ–µ—Б—В–љ–Њ–µ, –њ–Њ —Е–Њ–і—Г –≤—Б–µ–≥–Њ –Ї–∞–љ–∞–ї–∞ –≤–≤–Њ–і—П—В –љ–Њ–≤–Њ–Ї–∞–Є–љ –Є–ї–Є –ї–Є–і–Њ–Ї–∞–Є–љ. –С–Њ–ї—М–љ—Л–µ, –і–∞–ґ–µ —Б –Љ–Њ–±–Є–ї—М–љ–Њ–є –њ—Б–Є—Е–Є–Ї–Њ–є, –њ–µ—А–µ–љ–Њ—Б—П—В –Њ–њ–µ—А–∞—Ж–Є—О —Е–Њ—А–Њ—И–Њ. –Ъ–∞—В–µ—В–µ—А –і–µ—А–ґ–∞—В –љ–µ –Љ–µ–љ–µ–µ –Љ–µ—Б—П—Ж–∞, –њ–∞—Ж–Є–µ–љ—В—Л –њ—А–Є—Е–Њ–і—П—В –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ. –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –і–µ–±–Є—В–∞ –Є —А–∞–Ј–Љ–µ—А–Њ–≤ –њ–Њ–ї–Њ—Б—В–Є —А–µ—И–∞—О—В, –Ї–Њ–≥–і–∞ –µ–≥–Њ —Г–і–∞–ї—П—В—М. –Ъ–Є—Б—В—Л –њ–µ—З–µ–љ–Є –ї–µ—З–Є—В—М —В—П–ґ–µ–ї–µ–µ –≤—Б–µ–≥–Њ, –Њ–љ–Є —З–∞—Й–µ —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—В.
–Я—А–Њ–≤–Њ–і–Є—В—М –њ—Г–љ–Ї—Ж–Є–Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –Є –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є —В–Њ–Љ–Њ–≥—А–∞—Д–Є–Є. –Ю–і–љ–∞–Ї–Њ, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П –Љ–∞–љ–Є–њ—Г–ї—П—Ж–Є–є –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –£–Ч–Ш, –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –Ъ–Ґ, –≤ —В–Њ–Љ, —З—В–Њ –њ—А–Њ—Ж–µ–і—Г—А–∞ –њ—А–Њ—Е–Њ–і–Є—В –≤ —А–µ–ґ–Є–Љ–µ —А–µ–∞–ї—М–љ–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є.
 
–Х—Б–ї–Є –≥–Њ–≤–Њ—А–Є—В—М –Њ —Б–Њ–≤–Љ–µ—Й–µ–љ–Є–Є –љ–∞–≤–Є–≥–∞—Ж–Є–Њ–љ–љ–Њ–є –Є —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–є —Е–Є—А—Г—А–≥–Є–Є, —В–Њ —Н—В–Њ –≤–њ–Њ–ї–љ–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ. –Э–∞–њ—А–Є–Љ–µ—А, —Ж–Є—Б—В–Њ–µ—О–љ–Њ–∞–љ–∞—Б—В–Њ–Љ–Њ–Ј –њ—А–Є –Ї–Є—Б—В–µ –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л. –°–µ–є—З–∞—Б –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –£–Ч–Ш¬† –љ–∞–Ї–ї–∞–і—Л–≤–∞–µ—О—В –њ–∞–љ–Ї—А–µ–∞—В–Њ—Ж–Є—Б—В–Њ–≥–∞—Б—В—А–Њ–∞–љ–∞—Б—В–Њ–Љ–Њ–Ј—Л. –Ъ–Њ–≥–і–∞ –µ—Б—В—М —Е–Њ—А–Њ—И–∞—П –Ї–Є—Б—В–∞, –Ї–Њ—В–Њ—А–∞—П –≤—Л–±—Г—Е–∞–µ—В —З–µ—А–µ–Ј –Ј–∞–і–љ—О—О —Б—В–µ–љ–Ї—Г –ґ–µ–ї—Г–і–Ї–∞, –њ—Г–љ–Ї—В–Є—А—Г—О—В –Њ–±–µ —Б—В–µ–љ–Ї–Є –ґ–µ–ї—Г–і–Ї–∞ –Є –Ї–Є—Б—В—Г. –Ш—Б–њ–Њ–ї—М–Ј—Г–µ–Љ –і—А–µ–љ–∞–ґ —Б —Д–Є–Ї—Б–Є—А—Г—О—Й–Є–Љ—Б—П –Ї–Њ–љ—Ж–Њ–Љ, –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ –њ–Њ–і—В—П–≥–Є–≤–∞—П –µ–≥–Њ. –Ю–±—А–∞–Ј—Г–µ—В—Б—П –њ—А–Њ–ї–µ–ґ–µ–љ—М –Љ–µ–ґ–і—Г –њ–µ—А–µ–і–љ–µ–є —Б—В–µ–љ–Ї–Њ–є –Ї–Є—Б—В—Л –Є –Ј–∞–і–љ–µ–є —Б—В–µ–љ–Ї–Њ–є –ґ–µ–ї—Г–і–Ї–∞. –Я—А–Є–Љ–µ—А–љ–Њ —З–µ—А–µ–Ј –љ–µ–і–µ–ї—О —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П –∞–љ–∞—Б—В–Њ–Љ–Њ–Ј 1—Е2,5—Б–Љ. –Ф–µ–Ї–Њ–Љ–њ—А–µ—Б—Б–Є—П –ґ–µ–ї—Г–і–Ї–∞ –љ–∞–Ј–Њ–≥–∞—Б—В—А–∞–ї—М–љ—Л–Љ –Ј–Њ–љ–і–Њ–Љ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Є–Ј–±–µ–ґ–∞—В—М –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –≤ –≤–Є–і–µ, –љ–∞–њ—А–Є–Љ–µ—А, –њ–Њ–і—В–µ–Ї–∞–љ–Є—П –ґ–µ–ї—Г–і–Њ—З–љ–Њ–≥–Њ —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–≥–Њ —З–µ—А–µ–Ј –њ—А–Њ–Ї–Њ–ї –њ–µ—А–µ–і–љ–µ–є —Б—В–µ–љ–Ї–Є.
–Э–∞–≤–Є–≥–∞—Ж–Є–Њ–љ–љ–Њ–є —Е–Є—А—Г—А–≥–Є–µ–є –њ–Њ–ї—М–Ј—Г—О—В—Б—П¬† —Г—А–Њ–ї–Њ–≥–Є. –Ю–љ–Є –і—А–µ–љ–Є—А—Г—О—В –Ї–Є—Б—В—Л, –∞–±—Б—Ж–µ—Б—Б—Л –њ–Њ—З–µ–Ї, –Њ–њ–µ—А–Є—А—Г—О—В –≥–Є–і—А–Њ–љ–µ—Д—А–Њ–Ј, –і—А–µ–љ–Є—А—Г—О—В –ї–Њ—Е–∞–љ–Ї–Є вАУ –њ—Г–љ–Ї—Ж–Є–Њ–љ–љ–∞—П –љ–µ—Д—А–Њ—Б—В–Њ–Љ–Є—П. –Я–Њ—В–Њ–Љ —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—О—В —Б—В–µ–љ—В –≤ –Љ–Њ—З–µ—В–Њ—З–љ–Є–Ї. –Т –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є–Є¬† –њ—Г–љ–Ї—В–Є—А—Г—О—В –Њ—З–µ–љ—М –±–Њ–ї—М—И–Є–µ –Ї–Є—Б—В—Л —П–Є—З–љ–Є–Ї–Њ–≤.